AI trong khám phá thuốc trong nháy mắt
Sự phát triển không ngừng của trí tuệ nhân tạo (AI) đang tác động đáng kể đến các ngành công nghiệp khác nhau, trong đó lĩnh vực dược phẩm và công nghệ sinh học cũng không ngoại lệ. Không có gì đáng ngạc nhiên khi cả các tổ chức dược phẩm lớn và nhỏ đang ngày càng áp dụng các nền tảng khám phá thuốc AI để hợp lý hóa quy trình nghiên cứu và phát triển, giảm thời gian và chi phí khám phá, đồng thời nâng cao hiệu quả tổng thể.
Các công ty dược phẩm hàng đầu như J&J, GSK, AstraZeneca, Novartis, Pfizer, Sanofi và Eli Lilly, trong số những công ty khác, đã đầu tư đáng kể vào AI để khám phá thuốc. Những khoản đầu tư này bao gồm đầu tư vốn cổ phần, mua lại hoặc hợp tác với các công ty tập trung vào AI, phát triển năng lực nội bộ hoặc kết hợp các chiến lược này.
Đồng thời, có sự gia tăng của các công ty công nghệ sinh học và khám phá thuốc mới được thành lập như các tổ chức lấy AI làm trung tâm, thường là ngay từ khi mới thành lập. Được thành lập chủ yếu trong thập kỷ qua, các công ty này đã xây dựng và thử nghiệm các nền tảng khám phá thuốc chuyên biệt dựa trên AI. Các nền tảng này thường kết hợp nhiều mô hình học máy và hiện đang bắt đầu mang lại những lợi ích đáng kể về khả năng phát hiện mục tiêu và thiết kế thuốc nhanh chóng và hiệu quả về chi phí. Kết quả là, họ đang sản xuất các ứng cử viên thuốc tiền lâm sàng và thuốc lâm sàng với tốc độ nhanh. Trong các phần tiếp theo, chúng ta sẽ khám phá một loạt các ứng cử viên thuốc do AI phát triển, bao gồm các phân tử nhỏ, sinh học và các phương thức khác, đã được đưa vào thử nghiệm lâm sàng hoặc sắp được thử nghiệm.
Ngoài ra, một số công ty AI đã đạt được những bước tiến trong việc mô hình hóa sinh học bằng cách sử dụng dữ liệu đa phương thức phức tạp ở quy mô không thể tưởng tượng được chỉ hai thập kỷ trước. Một nhóm công ty khác đã phát triển các nền tảng dựa trên AI để nâng cao hiệu quả hoạt động và thiết kế thí nghiệm trong các thử nghiệm lâm sàng hoặc phân tích dữ liệu trong thế giới thực, chẳng hạn như cảnh giác dược.
Các tập đoàn công nghệ lớn, như Alphabet, Microsoft, Amazon, IBM và Tencent, có chuyên môn về AI và công nghệ dữ liệu lớn, đồng thời cũng đang mạo hiểm tham gia vào lĩnh vực khám phá thuốc. Sự tham gia của họ bao gồm đầu tư, thành lập công ty khởi nghiệp, hợp tác với các công ty khoa học đời sống, thử nghiệm và đổi mới.
Cuối cùng, tiến bộ đáng kể đã đạt được trong các công nghệ tiên tiến khác, chẳng hạn như điện toán lượng tử, Cryo-EM và thư viện mã hóa DNA. Những công nghệ này đang hội tụ với xu hướng AI, dẫn đến không chỉ các loại công cụ, sản phẩm và dịch vụ mới mà còn tạo ra làn sóng khởi nghiệp sáng tạo và thậm chí cả các mô hình kinh doanh mới.
AI là gì và nó được áp dụng như thế nào trong khám phá thuốc?
Trí tuệ nhân tạo là một khái niệm tương đối cũ, được chính thức hóa tại một hội nghị nổi tiếng của Đại học Dartmouth vào năm 1956. Các công nghệ AI trong khám phá thuốc đã phát triển từ các khái niệm và phương pháp tiếp cận máy học (ML), hóa học và tin sinh học trước đó. Ví dụ, ứng dụng học máy để phát triển các mô hình quan hệ cấu trúc-hoạt động định lượng (QSAR) và các hệ thống chuyên gia để dự đoán độc tính đã có một lịch sử lâu dài.
Tuy nhiên, sự ra đời nhanh chóng (trong một số trường hợp - “theo cấp số nhân”) của dữ liệu lớn, phân tích nâng cao, giảm thiểu chi phí tính toán, tăng tốc GPU, điện toán đám mây, phát triển thuật toán (ví dụ: mạng lưới thần kinh sâu và mô hình ngôn ngữ lớn) và “dân chủ hóa” công nghệ AI — tất cả đã dẫn đến sự “bùng nổ” tổng hợp trong thương mại hóa và công nghiệp hóa trí tuệ nhân tạo, đặc biệt là trong ngành dược phẩm và công nghệ sinh học.
Trong sách trắng này, chúng tôi sử dụng thuật ngữ chung “trí tuệ nhân tạo” để chỉ bất kỳ hệ thống mô hình hóa và tính toán tinh vi nào có thể tự động tìm hiểu thông tin chuyên sâu và rút ra các đề xuất thực tế từ “dữ liệu lớn”, dữ liệu có cấu trúc và phi cấu trúc, cũng như dữ liệu đa phương thức.
Mặc dù không có giới hạn đối với một nhóm thuật toán cụ thể mà chúng tôi gọi là “trí tuệ nhân tạo”, nhưng trong hầu hết các trường hợp, chúng tôi hàm ý các hương vị khác nhau của các hệ thống dựa trên máy học (chủ yếu là mạng lưới thần kinh sâu) và xử lý ngôn ngữ tự nhiên lớn (NLP) người mẫu. Các hệ thống AI hiện đại có thể học mà không cần được hướng dẫn rõ ràng (trái ngược với phần mềm hóa tin học truyền thống theo logic “nếu-thì”), chúng có thể cải thiện độ chính xác sau các chu kỳ học mới và khi có thêm dữ liệu được cung cấp cho hệ thống, và - đáng chú ý nhất - chúng có thể xử lý dữ liệu đa phương thức cao với kích thước khổng lồ. Tất cả các thuộc tính như vậy là những gì phân biệt đáng kể các hệ thống trí tuệ nhân tạo thời hiện đại với các gói phần mềm tin sinh học và hóa học cũ. Những khả năng như vậy là trung tâm của những gì thúc đẩy sự phấn khích liên tục về AI (và sự cường điệu).
Trong khi một số thành phần của cái mà chúng tôi gọi là “trí tuệ nhân tạo” - ví dụ: công cụ học máy và mô hình ngôn ngữ - được hầu hết mọi tổ chức dược phẩm và phòng thí nghiệm học thuật sử dụng, một số công ty đã quản lý để xây dựng các đường ống mô hình hóa và tính toán tinh vi, nghiên cứu “nền tảng AI”, bao gồm các quy trình công việc tự động trên hàng chục, thậm chí hàng trăm mô hình và hệ thống khác nhau (học sâu, mô hình ngôn ngữ) và hàng trăm nguồn dữ liệu công khai và độc quyền khác nhau.
Sự tinh vi và tự động hóa cao của một số nền tảng AI đã dẫn đến việc chúng “hàng hóa hóa” đến mức chúng đã đăng ký nhãn hiệu thương mại. Đồng thời, một số trong số chúng được cung cấp dưới dạng phần mềm dưới dạng dịch vụ cho các công ty khác. Các ví dụ bao gồm mRNA DESIGN STUDIO™ của Moderna, Centaur Chemist® của Exscientia, Guardian Angel™ của AI Therapeutics, ConVERGE™ của Verge Genomics, Taxonomy3® của C4X Discovery, v.v.
Dưới đây là một ví dụ về Pharma.AI của Insilico Medicine, một hệ thống mô-đun để khám phá thuốc từ đầu đến cuối bao gồm hàng trăm hệ thống con và mô hình học máy khác nhau — được điều khiển hoàn toàn bởi các thuật toán trừu tượng hóa mô hình cao hơn khác (thông qua một nguyên tắc của “học tập đồng bộ”).
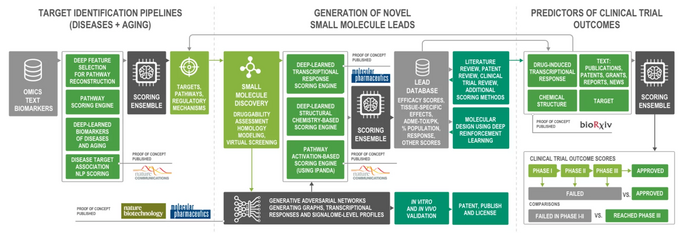
Sơ đồ của nền tảng đầu cuối Pharma.AI. Tín dụng hình ảnh: https://insilico.com
Trí tuệ nhân tạo được sử dụng rộng rãi trong hầu hết mọi khía cạnh của nghiên cứu dược phẩm, từ khai thác dữ liệu, mô hình sinh học và khám phá mục tiêu cho đến nhận dạng và nghiên cứu lâm sàng và tiền lâm sàng. Nó cũng được sử dụng để lập kế hoạch tổng hợp, tìm kiếm thuốc thử thông minh và vật tư tiêu hao nghiên cứu cũng như các tác vụ phụ trợ như sổ ghi chép thông minh trong phòng thí nghiệm và trợ lý ảo.

nguồn: https://www.biopharmatrend.com/m/companies/ai/
Hệ sinh thái Khoa học Đời sống của những người áp dụng AI bao gồm các loại người chơi chính sau:
|
Hơn 400 công ty do AI điều hành (khởi nghiệp/mở rộng quy mô), cung cấp nhiều loại nền tảng và dịch vụ do AI điều khiển — từ mô hình Phần mềm dưới dạng Dịch vụ cổ điển đến các dịch vụ khoa học dữ liệu tùy chỉnh, khám phá thuốc (“Dịch vụ dưới dạng ứng viên thuốc”) và hỗ trợ/quản lý thử nghiệm lâm sàng tài nguyên. |
|
Các nhà cung cấp phần mềm dành riêng cho miền (ví dụ: KNIME, ChemAxon, Dotmatics, MolSoft và các nhà cung cấp khác) chủ yếu tập trung vào phần mềm hóa tin học/tin sinh học nhưng cũng cung cấp các công cụ hỗ trợ máy học. |
|
Các công ty dược phẩm và công nghệ sinh học hàng đầu đang phát triển chuyên môn AI nội bộ như một phần trong chiến lược R&D của họ. Những người chơi như vậy thường hợp tác với các nhà cung cấp AI bên ngoài và các công ty khởi nghiệp công nghệ sinh học do AI điều khiển để khám phá các chương trình thí điểm về khám phá thuốc/sinh học cơ bản/phân tích thử nghiệm lâm sàng. |
|
Các công ty công nghệ hàng đầu như Google, Amazon và Tencent bước vào lĩnh vực dược phẩm, tận dụng các công nghệ AI tiên tiến và cơ sở hạ tầng dữ liệu lớn. |
|
Các tổ chức nghiên cứu hợp đồng (CRO) phát triển chuyên môn về AI để tăng giá trị cung cấp cho khách hàng dược phẩm/công nghệ sinh học |
|
Phòng thí nghiệm học thuật trong không gian dược phẩm/công nghệ sinh học, tiến hành nghiên cứu AI và phát triển các khuôn khổ và công cụ chuyên biệt phù hợp với ngành (thường là cái nôi cho các công ty khởi nghiệp/spin-out AI trong tương lai) |
|
Các nhà cung cấp phần mềm không dành riêng cho miền đang phát triển các gói và mô hình dịch vụ AI phù hợp để ứng dụng trong nghiên cứu dược phẩm (ví dụ: “AI vượt trội”) |
|
Các công cụ và khuôn khổ máy học mã nguồn mở, được các chuyên gia khoa học đời sống khai thác rộng rãi trong các dự án nghiên cứu của họ |
Bối cảnh đầu tư khám phá thuốc AI
Sau năm 2021, năm thành công bất thường đối với ngành công nghệ sinh học về số lượng giao dịch đầu tư mạo hiểm, số lượng chào bán lần đầu ra công chúng kỷ lục, số lượng thoái vốn thành công dồi dào và môi trường nhìn chung rất tích cực trên thị trường chứng khoán, năm 2022 đã chứng minh sự hạ nhiệt đáng kể của hoạt động tài chính và hoạt động kém hoàn toàn của thị trường chứng khoán.
Tuy nhiên, trí tuệ nhân tạo trong lĩnh vực khám phá thuốc đã thể hiện khả năng phục hồi nhất định, ít nhất là trong bối cảnh giao dịch vốn cổ phần tư nhân, với một số công ty đã huy động được hàng trăm triệu đô la vốn mạo hiểm. Một số ví dụ bao gồm Công nghệ MegaRobo có trụ sở tại Bắc Kinh (300 triệu USD Series C), ConcertAI có trụ sở tại Massachusetts (150 triệu USD Series C) và Celsius Therapeutics (83 triệu USD Series A), Insilico Medicine có trụ sở tại Hồng Kông (95 triệu USD Series D), California- dựa trên BigHat Bioscatics ($75 triệu Series B) và DeepCell ($73 triệu Series B) và một số công ty khác — đọc “Các vòng đầu tư mạo hiểm lớn dành cho các công ty AI trong lĩnh vực Khám phá Thuốc và Công nghệ sinh học vào năm 2022".
Bối cảnh mua bán và sáp nhập (M&A) được đánh dấu bằng một thương vụ đáng chú ý gần đây liên quan đến một gã khổng lồ công nghệ sinh học Ginkgo Biowork mua lại Zymergen trong một giao dịch định giá Zymergen ở mức 300 triệu USD. Việc mua lại mang lại khả năng học máy và khoa học dữ liệu của Zymergen cùng với nền tảng sinh học tổng hợp của Ginkgo.
Các quan sát và xu hướng chính của ngành
Sự ra đời của AI và công nghệ dữ liệu, cũng như các công cụ tính toán mới và giải pháp cơ sở hạ tầng (cơ sở dữ liệu, dịch vụ đám mây, v.v.), tất cả đang định nghĩa lại cách thức hoạt động của ngành dược phẩm — ở cấp độ nghiên cứu, lâm sàng và kinh doanh. Dưới đây, chúng ta hãy xem xét một số xu hướng và quan sát trong AI cho không gian khám phá thuốc và sự phát triển của ngành minh họa vào năm 2022.
Mô hình sinh học hỗ trợ AI và khám phá mục tiêu
Trong nghiên cứu khám phá thuốc, việc xác định các mục tiêu thuốc mới là rất quan trọng để phát triển các loại thuốc điều trị hạng nhất mới - những “quả bom tấn” tiềm năng. Theo truyền thống, các nỗ lực khám phá thuốc trong vài thập kỷ qua tập trung vào việc nhắm mục tiêu các protein cụ thể với các “túi” phù hợp để chịu ảnh hưởng của một phân tử phối tử (thường là một phân tử nhỏ). Nhưng trong số toàn bộ protein của con người (hay còn gọi là “proteome”), một số lượng nhỏ protein đã được khám phá làm mục tiêu. Hiện tại có 20,360 protein của con người ở Swiss-Prot, trong đó có khoảng 4,600 được biết là có liên quan đến cơ chế gây bệnh theo cơ sở dữ liệu OMIM, chiếm khoảng 22% protein của con người có vai trò gây bệnh. Những protein này là khu vực rõ ràng của hệ protein của con người có khả năng chứa các mục tiêu thuốc khả thi. Tuy nhiên, a partir de 2017, chỉ có khoảng 890 phân tử sinh học có nguồn gốc từ con người và mầm bệnh (chủ yếu là protein) thực sự được sử dụng bởi các loại thuốc hiện có được FDA chấp thuận. Những phân tử sinh học này bao gồm 667 protein có nguồn gốc từ bộ gen người được nhắm mục tiêu bởi các loại thuốc điều trị bệnh ở người. Ngày nay mọi thứ không khác nhiều, vì vậy vẫn còn nhiều chỗ để xác định các mục tiêu mới trong nhóm này. Các phương pháp tính toán mới dựa trên công nghệ trí tuệ nhân tạo cho phép xác định các túi protein mới có thể uống được ở quy mô lớn, đôi khi cho phép tạo ra các màn hình ảo trên toàn bộ hệ protein.
Nhưng điều thú vị hơn nữa là các công cụ lập mô hình tiên tiến giúp xác định và điều chỉnh các loại mục tiêu mới, chẳng hạn như tương tác protein-protein, mục tiêu có diện tích tiếp xúc lớn, tương tác protein-axit nucleic và các mục tiêu thế hệ tiếp theo, chẳng hạn như khai thác protein của tế bào máy móc xuống cấp.
Rất nhiều công ty do AI điều khiển đang tập trung vào mô hình hóa sinh học, khám phá và xác thực các mục tiêu mới và cung cấp “mô hình bệnh tật dưới dạng dịch vụ” hoặc “khám phá mục tiêu dưới dạng dịch vụ” cho các tổ chức khác. Nhu cầu đối với loại dịch vụ nghiên cứu hợp đồng này đang tăng lên, điều này được phản ánh qua số lượng ngày càng tăng của các quan hệ đối tác khám phá mục tiêu.
Ví dụ: vào tháng 2022 năm 110, CytoReason, một công ty mô hình sinh học có trụ sở tại Israel, đã công bố một khoản hợp tác mở rộng trị giá 2019 triệu đô la với Pfizer. Hai công ty bắt đầu hợp tác vào năm XNUMX khi Pfizer bắt đầu sử dụng các mô hình sinh học của CytoReason trong nghiên cứu nhằm phát triển các loại thuốc mới điều trị các bệnh qua trung gian miễn dịch và liệu pháp miễn dịch ung thư.
Vào tháng 2022 năm 2019, AstraZeneca thông báo rằng họ đã thu thập được mục tiêu xơ hóa phổi thứ hai từ sự hợp tác của mình với BenevolentAI, công ty hàng đầu có trụ sở tại Vương quốc Anh trong lĩnh vực khám phá thuốc dựa trên trí tuệ nhân tạo. Cột mốc đánh dấu mục tiêu mới lạ thứ ba do BenevolentAI phát hiện cho AstraZeneca kể từ khi sự hợp tác bắt đầu vào năm 2022. Chỉ vài tháng sau, vào tháng XNUMX năm XNUMX, BenevolentAI đã quản lý để cung cấp thêm hai mục tiêu do AI tạo ra cho danh mục R&D của AstraZeneca, nhằm vào bệnh thận mãn tính và bệnh vô căn. xơ phổi.
Vào tháng 2022 năm 1.2, Insilico Medicine có trụ sở tại Hồng Kông đã ký một thỏa thuận có khả năng trị giá XNUMX tỷ USD với Sanofi vì đã phát hiện ra tối đa sáu mục tiêu mới tận dụng nền tảng “Pharma.AI” của Insilico Medicine.
Mặc dù các thuật toán tiên tiến như mạng lưới thần kinh sâu yêu cầu khối lượng dữ liệu lớn để mô hình hóa sinh học đúng cách, nhưng vẫn có những mục tiêu có sẵn một lượng dữ liệu nhỏ. Cyclica có trụ sở tại Canada đã phát triển một nền tảng dựa trên AI để sàng lọc đa dược lý và toàn bộ hệ protein, có khả năng hoạt động với các mục tiêu “dữ liệu thấp”. Vào tháng 2022 năm 1.8, Cyclica đã nhận được khoản tài trợ trị giá XNUMX triệu đô la từ Quỹ Bill & Melinda Gates để áp dụng nền tảng khám phá thuốc hỗ trợ AI nhằm khám phá các hợp đồng không có nội tiết tố mới, tận dụng nhiều mục tiêu sinh học ít dữ liệu.
Theo Báo cáo xu hướng dược phẩm sinh học, có ít nhất 182 công ty AI khác trong lĩnh vực khám phá mục tiêu, bao gồm các công ty hàng đầu được tài trợ tốt với nền tảng R&D tiên tiến, chẳng hạn như Insitro, Relay Therapeutics, Valo Health và các công ty khác.
Các công ty khởi nghiệp “có nguồn gốc từ AI” mới liên tục xuất hiện trong không gian mô hình hóa sinh học. Ví dụ: CardiaTec Bioscatics, WhiteLab Genomics, Degron Therapeutics, v.v.
Liên quan: 11 công ty khởi nghiệp khám phá thuốc dựa trên AI được thành lập vào năm 2021
Nói chung, các phương pháp lập mô hình tiên tiến dựa trên trí tuệ nhân tạo giúp xác định lại định nghĩa về mục tiêu sinh học, khi chúng tôi cố gắng liên kết phản ứng của thuốc với biến thể di truyền, hiểu hiệu quả và độ an toàn lâm sàng phân tầng, hợp lý hóa sự khác biệt giữa các loại thuốc trong cùng nhóm trị liệu và dự đoán tiện ích thuốc trong các phân nhóm bệnh nhân.
Bẻ khóa sinh học cấu trúc với AI
Một trong những chủ đề liên quan đến AI được thảo luận nhiều nhất trong cộng đồng Khoa học Đời sống năm nay là thành công gần đây của DeepMind, công ty con của Alphabet có trụ sở tại Vương quốc Anh, đã nhận được sự phủ sóng rộng rãi cho thành công của nó trong việc bẻ khóa vấn đề gấp protein, một vấn đề sinh học tồn tại nửa thế kỷ.
Vào tháng 2022 năm XNUMX, phần mềm học sâu AlphaFold của DeepMind dự đoán và chia sẻ công khai cấu trúc protein của hơn 200 triệu protein, đã chứng minh khả năng đáng kinh ngạc của hệ thống AI trong việc dự đoán chính xác cấu trúc 3D chỉ từ chuỗi axit amin 1D của nó. Trong khi một số người cho rằng khám phá này có thể (chưa) có vai trò biến đổi như vậy trong việc khám phá thuốc như người ta có thể giả định, và AlphaFold đã không thực hiện tốt hơn nhiều so với cơ hội khi dự đoán các tương tác hợp chất kháng khuẩn protein của vi khuẩn, khám phá này chắc chắn sẽ thay đổi mô hình đối với cả sinh học cấu trúc và minh họa tiềm năng của AI trong nghiên cứu sinh học cơ bản.
Vào tháng 2022 năm 600, thành công đột phá của DeepMind trong việc lập mô hình hệ protein đã bị các nhà nghiên cứu tại Meta (trước đây là Facebook, có trụ sở tại Menlo Park, California) cạnh tranh. Nó đã sử dụng AI để dự đoán cấu trúc của khoảng XNUMX triệu protein từ vi khuẩn, vi rút và các vi sinh vật khác chưa được mô tả đặc điểm.
Các nhà khoa học tại Meta đã sử dụng hoàn toàn cách tiếp cận AI khác nhau — sử dụng 'mô hình ngôn ngữ lớn', một loại AI có thể dự đoán văn bản chỉ từ một vài chữ cái hoặc từ. Các mô hình ngôn ngữ tự nhiên (NLP) thường được đào tạo trên khối lượng lớn văn bản. Tuy nhiên, các chuỗi protein 1D về cơ bản là các chuỗi ký tự, vì vậy NLP có thể được áp dụng cho các vấn đề như vậy tương tự như làm việc với ngôn ngữ của con người.
Thật thú vị, những bước nhảy vọt về công nghệ lớn như vậy trong việc gấp protein có thể hữu ích hơn cho thiết kế protein de novo, chứ không chỉ đơn giản là lập mô hình cấu trúc của các protein hiện có để khám phá thuốc. Thời gian sẽ cho biết nơi nào sẽ có tác động lớn nhất, nhưng những thành công trên của DeepMind và Meta không phải là bước phát triển thú vị duy nhất cho các nhà sinh học cấu trúc vào năm 2022.
Gần đây, những tiến bộ nhanh chóng trong cryo-EM, cùng với công nghệ AI, đã sinh ra một làn sóng khởi nghiệp công nghệ sinh học mới chẳng hạn như Gandeeva Therapeutics, Septerna và MOMA Therapeutics. Lĩnh vực cryo-EM đang nóng lên với việc các công ty khởi nghiệp công nghệ sinh học thu hút sự chú ý của nhiều nhà đầu tư, từ các tổ chức mạo hiểm nhỏ hơn đến chủ sở hữu của TikTok và gã khổng lồ công nghệ internet ByteDance, đầu tư vào Shuimu BioSciences. Sự quan tâm không chỉ được thúc đẩy bởi công nghệ mang tính cách mạng từng đoạt giải Nobel mà còn bởi việc tích cực tuyển dụng AI vào quy trình. ấn phẩm gần đây “Một đường dẫn cryo-EM được hỗ trợ bởi AI để nghiên cứu cấu trúc của chiết xuất tế bào” nhấn mạnh vai trò không thể thay thế của AI trong các đường ống cryo-EM phức tạp, bao gồm dự đoán mô hình nguyên tử do AI điều khiển để điều tra nhanh chóng và đồng thời cấu trúc của nhiều thành viên cộng đồng protein de novo. Công nghệ máy học không chỉ giúp tăng tốc và tối ưu hóa quy trình cryo-EM mà còn tránh những sai lầm do thành kiến của người dùng.
Gandeeva Therapeutics, được thành lập vào năm 2021, đã huy động được 40 triệu đô la vào đầu năm nay để phát triển các liệu pháp mới dựa trên hình ảnh chính xác về tương tác thuốc-protein. Công cụ Lựa chọn Mục tiêu của họ cùng với Công cụ Cryo-EM có thể giúp “tránh khỏi ngõ cụt của việc khám phá”, như công ty đã tuyên bố. Đồng thời, ra mắt vào năm 2020 công nghệ sinh học cryo-EM MOMA Therapeutics đã huy động được số tiền khổng lồ 236 triệu đô la chỉ trong hai năm, với mục tiêu đầy tham vọng là phát hành các loại thuốc chính xác mới cho bệnh ung thư. MOMA tập trung vào một loại mục tiêu sinh học duy nhất - “máy phân tử”.
Phát triển các phân tử nhỏ bằng AI
Sau mô hình bệnh tật và khám phá mục tiêu, thiết kế các phân tử hóa học hoặc sinh học là trường hợp sử dụng phổ biến thứ hai để áp dụng trí tuệ nhân tạo trong khám phá thuốc. Hơn 130 công ty dựa trên trí tuệ nhân tạo trong số 384 công ty trong Báo cáo AI của BiopharmaTrend áp dụng trí tuệ nhân tạo để thiết kế các loại thuốc tiềm năng, trong số các trường hợp sử dụng khác.
Thiết kế thuốc dựa trên AI chủ yếu thuộc ba loại chính: thiết kế thuốc mới (ví dụ: tổng quát), sàng lọc ảo các cơ sở dữ liệu hiện có và tái sử dụng thuốc.
Thiết kế thuốc de novo hầu hết được kích hoạt bởi các mô hình học sâu, chẳng hạn như mạng lưới thần kinh đối kháng chung (GAN). Một số ví dụ về nền tảng AI tổng quát bao gồm phần mềm Chemistry42 của Insilico Medicine, Makya của Iktos và De Novo Platform của Ro5. Những người chơi khác trong danh mục này bao gồm Recursion Pharmaceuticals, Deep Cure, Standigm và những người khác.
Việc áp dụng sàng lọc ảo quy mô cực lớn hỗ trợ trí tuệ nhân tạo, sàng lọc hàng tỷ phân tử để tìm ra các lượt truy cập thành công. Vào tháng 2022 năm 1.2, Sanofi hợp tác với Atomwise trong một thỏa thuận thiết kế thuốc trị giá có thể lên tới 20 tỷ USD. Thỏa thuận này cho thấy Sanofi trả trước 3 triệu USD, tập trung vào việc tận dụng nền tảng AtomNet của công ty Hoa Kỳ để nghiên cứu các phân tử nhỏ cho tối đa năm mục tiêu thuốc do Sanofi lựa chọn. AtomNet dựa trên mạng thần kinh tích chập vượt trội trong thiết kế thuốc dựa trên cấu trúc, cho phép “tìm kiếm nhanh chóng, được hỗ trợ bởi AI trong thư viện độc quyền của Atomwise gồm hơn XNUMX nghìn tỷ hợp chất có thể tổng hợp được,” theo báo cáo thông báo.
Đầu năm 2019, Atomwise đã hợp tác với nhà lãnh đạo hóa học Enamine có trụ sở tại Ukraine để tiến hành “màn hình ảo 10 tỷ hợp chất đầu tiên và lớn nhất thế giới”, nhằm xác định các lần truy cập cho bệnh ung thư nhi khoa.
Cuối cùng, một số công ty đang sử dụng các chiến lược tái sử dụng để khám phá thuốc hỗ trợ AI. Các công ty trong danh mục này, bao gồm Healx, BenevolentAI, BioXcel Therapeutics, chủ yếu sử dụng các mô hình xử lý ngôn ngữ tự nhiên (NLP) và máy học và hoạt động thông qua việc phân tích một lượng lớn dữ liệu văn bản phi cấu trúc - các bài báo nghiên cứu và bằng sáng chế, hồ sơ sức khỏe điện tử (EHRs), như cũng như các loại dữ liệu khác — để xây dựng và tìm kiếm “biểu đồ tri thức”. Các bản thể luận có thể tìm kiếm hỗ trợ AI như vậy cho phép chọn các chỉ định mới hoặc quần thể bệnh nhân cho các ứng cử viên thuốc đã biết trước đó hoặc thậm chí các loại thuốc đã được phê duyệt.
Ví dụ, Lantern Pharma, một công ty công nghệ sinh học giai đoạn lâm sàng có trụ sở tại Hoa Kỳ, tập trung vào việc đổi mới quy trình phát triển thuốc điều trị ung thư bằng cách sử dụng bộ gen tiên tiến, học máy và trí tuệ nhân tạo.
Thúc đẩy việc khám phá và phát triển thuốc điều trị ung thư bằng cách sử dụng Nền tảng máy học và trí tuệ nhân tạo RADR®
Nền tảng AI của công ty, RADR®️, hiện bao gồm hơn 25 tỷ điểm dữ liệu và sử dụng phân tích dữ liệu lớn và học máy để nhanh chóng phát hiện ra các dấu hiệu bộ gen có liên quan về mặt sinh học có liên quan đến phản ứng của thuốc, sau đó xác định các phân nhóm bệnh nhân ung thư có liên quan để hưởng lợi từ các ứng cử viên thuốc của Lantern . RADR ®️ cũng được Lantern và các cộng tác viên của nó sử dụng để phát triển và định vị các loại thuốc mới cũng như để tái sử dụng thuốc.
Liên quan: Hé lộ câu chuyện thành công của Lantern Pharma trong lĩnh vực Ung thư chính xác do AI cung cấp
AI đáp ứng các thư viện được mã hóa DNA
Một cách tiếp cận hơi độc đáo để thiết kế thuốc bao gồm sử dụng các thư viện được mã hóa DNA (DEL) làm nguồn phân tử mới để tìm kiếm. Vì công nghệ DEL cung cấp quyền truy cập vào không gian hóa chất lớn nhất hiện có trên thị trường, nên công nghệ dữ liệu lớn này rất phù hợp với các công cụ dựa trên AI.
Một đáng chú ý nhiều diễn ra vào năm 2020, khi Insitro, một trong những công ty đáng chú ý trong lĩnh vực ứng dụng máy học để khám phá thuốc, do Daphne Koller thành lập, mua lại Haystack Science. Nền tảng dựa trên máy học của Haystack đã kết hợp nhiều yếu tố trong công nghệ DEL của họ, bao gồm khả năng tổng hợp các tập hợp phân tử nhỏ, đa dạng, rộng lớn, khả năng thực hiện theo dõi lặp lại và công nghệ sàng lọc bán định lượng độc quyền có tên là nDexer™, tạo ra bộ dữ liệu có độ phân giải cao hơn.
Đến lượt mình, ZebiAI đã được mua lại vào năm 2021 bởi một nhà phát triển đáng chú ý khác của nền tảng khám phá thuốc dựa trên trí tuệ nhân tạo, Relay Therapeutics công nghệ sinh học ở giai đoạn lâm sàng, trong đó Relay đã trả trước 85 triệu đô la. Việc mua lại này cho phép Relay kết hợp công nghệ DEL dựa trên máy học của ZebiAI vào nền tảng nhắm mục tiêu protein Dynamo của họ.
Liên quan: Đánh giá thị trường về công nghệ thư viện được mã hóa DNA trong khám phá thuốc
Vào tháng 2021 năm XNUMX, X-Chem đã mua lại Glamious AI, nhà phát triển giải pháp trí tuệ nhân tạo đa diện dạng mô-đun để khám phá thuốc RosalindAI, bao gồm các khả năng về kỹ thuật và tính năng hóa dữ liệu, phân tích dự đoán, điện toán hiệu suất cao và thiết kế thuốc mới.
Thiết kế thuốc điều khiển bằng AI ngoài các phân tử nhỏ
Xem xét rằng các công cụ trí tuệ nhân tạo hiện đại được áp dụng để khám phá thuốc có nguồn gốc lịch sử sâu xa trong hóa học và các mô hình QSAR dựa trên máy học thời kỳ đầu của thế kỷ trước, không có gì ngạc nhiên khi phần lớn các công ty khởi nghiệp AI trong khám phá thuốc đều tập trung vào các phân tử nhỏ. .
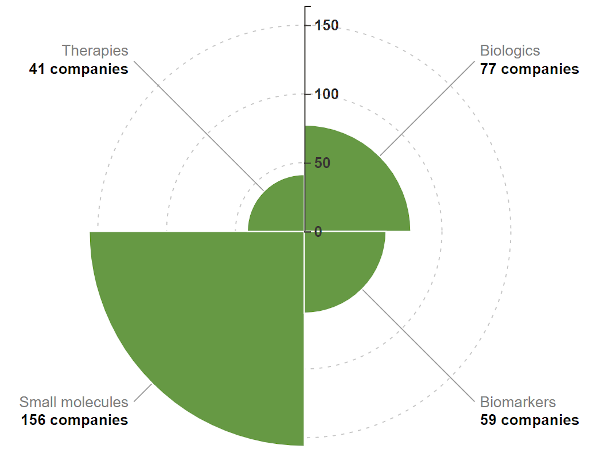
Phân phối các công ty khám phá thuốc AI theo danh mục sản phẩm. Nguồn: Báo cáo AI của BiopharmaTrend.
Tuy nhiên, các loại thuốc sinh học phân tử (hay còn gọi là “sinh học”) và các phương thức hóa học mới đang ngày càng phong phú trong lĩnh vực dược phẩm, và các công ty công nghệ sinh học mới cũng vậy đang áp dụng các phương pháp dựa trên AI để khám phá những loại thuốc đó. Sau khi các nhà khoa học giải mã được bộ gen của con người vào năm 2003, không gian khả năng sử dụng thuốc và khả năng phát triển đã phát triển nhanh chóng. Trong thế kỷ trước, quy tắc năm (Ro5) của Lipinski từng đóng vai trò là “đèn hướng dẫn” cho thiết kế phân tử giống như thuốc để phân phối qua đường miệng trong không gian mục tiêu có thể uống được “truyền thống”.
Ngược lại, các loại mục tiêu mới, chẳng hạn như tương tác protein-protein, mục tiêu có diện tích tiếp xúc lớn, tương tác protein-axit nucleic và các mục tiêu thế hệ tiếp theo, chẳng hạn như khai thác bộ máy phân hủy protein của tế bào, đang thúc đẩy sự ra đời của nhiều loại mục tiêu mới nổi. phương thức phân tử, cụ thể là ngoài các phân tử nhỏ Ro5 (bRo5) (chẳng hạn như bộ điều hòa tương tác protein-protein, thể khảm nhắm mục tiêu protein (PROTAC), kháng thể đơn dòng (mAbs), peptide và peptidomimetic, và phương thức dựa trên axit nucleic (RNA và DNA- based), đã trở thành trọng tâm chính trong khám phá thuốc.
Liên quan: “Sự bùng nổ” của các phương thức trị liệu: Phân tử nhỏ, sinh học và mọi thứ ở giữa,
Chẳng hạn, ngày càng có nhiều công ty áp dụng các phương pháp AI để khám phá các kháng thể đơn dòng mới - phương thức sinh học thành công nhất về mặt thương mại cho đến nay. Đáng chú ý là vào tháng 2022 năm XNUMX, Biolojic Design có trụ sở tại Israel đã công bố kháng thể được thiết kế bằng máy tính đầu tiên của họ. bước vào thử nghiệm lâm sàng. Công ty tận dụng một chiến lược thiết kế dựa trên cấu trúc. Mô hình AI của nó được đào tạo trên hàng triệu cặp kháng thể-kháng nguyên để xác định kháng thể mẫu chống lại mục tiêu quan tâm từ các kháng thể hiện có của con người. Một mô hình học máy bổ sung được sử dụng để dự đoán các đột biến và hướng dẫn tối ưu hóa mẫu để cải thiện các thuộc tính của mẫu.
Vào tháng 2022 năm 2020, AbCellera Biologics có trụ sở tại Canada đã thông báo rằng Regeneron đã chọn thực hiện quyền của mình để thúc đẩy ứng cử viên kháng thể trị liệu đầu tiên của AbCellera nhắm mục tiêu thụ thể kết hợp G-protein chưa được tiết lộ (GPCR) vào bước phát triển tiền lâm sàng tiếp theo. Sự hợp tác bắt đầu vào tháng XNUMX năm XNUMX và cho phép bốn chương trình khám phá do Regeneron lựa chọn, tận dụng công cụ khám phá kháng thể dựa trên AI của AbCellera và chuột VelocImmune® của Regeneron để xác định các kháng thể trị liệu mới.
Hai chục công ty khám phá kháng thể khác đang sử dụng AI, bao gồm AbSci, BigHat Bioscatics, Totient, Nabla Bio và Generate Biomedicine có trụ sở tại Hoa Kỳ; Deep Biologics có trụ sở tại Canada; NeoX có trụ sở tại Trung Quốc; Deep CDR, Natural Antibody và MabSilico có trụ sở tại EU, v.v.
Công ty có trụ sở tại Hoa Kỳ với cái tên hấp dẫn Creyon Bio áp dụng phương pháp kỹ thuật để tạo ra các loại thuốc dựa trên oligonucleotide (OBM) mới. Công ty được thành lập vào năm 2019 và đã huy động được 40 triệu đô la tài trợ vào tháng 2022 năm 2014. Được thành lập vào năm 2022 với tư cách là một công ty con của Phòng thí nghiệm Cold Spring Harbor, Envisagenics là một công ty có trụ sở tại New York tập trung vào việc khám phá các liệu pháp RNA. Theo sứ mệnh đã nêu, họ đặt mục tiêu giảm độ phức tạp của dữ liệu y sinh với sự trợ giúp của các công nghệ AI/ML. Mới gần đây, vào tháng 27.1 năm XNUMX, họ đã nhận được khoản tài trợ từ Viện Ung thư Quốc gia, dẫn đến tổng số tiền gây quỹ được là XNUMX triệu đô la.
Công nghệ dựa trên AI của Envisagenics, SpliceCore, là một nền tảng dựa trên đám mây đã được xác thực bằng thực nghiệm để dự đoán các mục tiêu thuốc và dấu ấn sinh học thông qua phát hiện nối từ dữ liệu giải trình tự RNA. Theo công ty, nó đảm bảo độ chính xác và tốc độ cao hơn so với các phương pháp truyền thống.
Chiến lược dựa trên trí tuệ nhân tạo của Innophore để thiết kế các enzyme trị liệu mới được hiện thực hóa bằng cách kết hợp công nghệ Catalophore™ đã được cấp bằng sáng chế của họ với các phương pháp tin sinh học thông thường tiên tiến nhất và trí tuệ nhân tạo. Innophore có thể khai thác cơ sở dữ liệu cấu trúc và trình tự bằng cách sử dụng các mẫu tìm kiếm ba chiều (3D) được gọi là “catalophores” (tức là chất mang chức năng xúc tác) được xác định bởi các đám mây điểm có các đặc điểm hóa lý. Các enzyme mới được xác định bằng kỹ thuật này không nhất thiết phải chia sẻ cơ sở cấu trúc hoặc trình tự chung với các đối tác được sử dụng của chúng. Do đó, chúng có khả năng làm nổi bật các đặc tính protein bị thay đổi, chẳng hạn như khả năng điều nhiệt, độ bền, phổ cơ chất, tính chọn lọc và tính đặc hiệu.
Bên cạnh việc thiết kế các enzym mới, công nghệ của Innophore có khả năng thay đổi cuộc chơi cho các ứng dụng dịch tễ học, bảo vệ các đột biến nguy hiểm tiềm tàng ở vi rút. Năm 2021, Innophore bắt đầu dự án virus.watch với sự hợp tác của Sáng kiến phát triển chẩn đoán AWS. Mục tiêu của dự án này là triển khai một hệ thống giám sát và đánh giá các biến thể virus corona (SARS-CoV-2) liên quan đến bệnh và thuốc mới nổi. Bài báo chung đầu tiên, công bố trên tạp chí Nature vào tháng 2022 năm 2, mô tả phân tích tin sinh học của các biến thể SARS-CoV-2 cho thấy ái lực liên kết với thụ thể hACE1.1.529 cao hơn đối với RBD tăng đột biến Omicron B.XNUMX so với tham chiếu kiểu hoang dã.

Theo dõi sự phát triển của vi-rút theo thời gian bằng công nghệ Innophore và AWS cho thấy tỷ lệ đột biến phát sinh cao với biến thể Omicron. Các quả cầu mô tả các nguyên tử alpha-C của gốc axit amin tương ứng. Cả màu sắc và kích thước đều tương quan với số lượng đột biến ở mỗi vị trí.
Được thành lập vào năm 2008, Evaxion Biotech có trụ sở tại Đan Mạch là một công ty do AI điều hành, chuyên phát triển vắc-xin chống ung thư và các bệnh truyền nhiễm. Họ sở hữu một nền tảng Miễn dịch học AI ở giai đoạn lâm sàng, kết hợp công nghệ AI với chuyên môn kỹ thuật của họ để tạo ra các mô hình dự đoán, giúp xác định các liệu pháp miễn dịch độc đáo cho bệnh nhân. Evaxion Biotech đã thu hút được tổng cộng 57 triệu đô la, tham gia vòng gọi vốn cổ phần sau IPO vào tháng 2022 năm 40 trị giá XNUMX triệu đô la, do một nhà đầu tư duy nhất là Quỹ Lincoln Park Capital dẫn đầu.
Liên quan: 10 công ty ứng dụng AI để thiết kế sinh học
Một số công ty AI từ “câu lạc bộ phương thức hóa học”, như Exscientia, hiện đang mở rộng sang lĩnh vực khám phá sinh học. Vào tháng 2022 năm XNUMX, công ty đã thông báo rằng nền tảng AI của họ sẽ bao gồm việc thiết kế các kháng thể của con người. Exscientia cũng đang thành lập một phòng thí nghiệm sinh học tự động ở Oxford để tạo ra và xác định các kháng thể mới trong nội bộ.
Một xu hướng đang phát triển là khai thác hệ thống thoái hóa protein của tế bào người để loại bỏ các protein ác tính và chữa bệnh. Một phương thức ở đây đang ngày càng phổ biến là chimera nhắm mục tiêu phân giải protein (PROTAC) đã được giới thiệu vào năm 2001 và nó bao gồm hai phối tử được kết nối bởi một trình liên kết linh hoạt. Kiến trúc hóa học chính của PROTAC hiện đại giống nhau: một phối tử nhắm vào enzyme E3, là thành phần gửi các protein lỗi thời đến proteasome và một phối tử khác nhắm đến một protein quan tâm (POI) phải bị phân hủy. PROTAC liên kết E3 và POI, đưa chúng lại gần nhau hơn để tạo thành một phức hợp lân cận cảm ứng. Trong một số trường hợp, khi các protein sắp xếp phù hợp, POI sẽ được phổ biến khắp nơi, điều này đánh dấu sự xuống cấp của proteasome.
Một cách tiếp cận rộng rãi khác đối với sự phân hủy protein bao gồm cái gọi là “keo phân tử”, một lĩnh vực nghiên cứu đang phát triển tích cực. Trái ngược với PROTAC, là các phân tử nhỏ có chức năng nhị phân tương đối lớn với hai vị trí hoạt động và một chất liên kết, keo phân tử là các phân tử nhỏ hơn và giống thuốc hơn. Loại thứ hai liên kết với một túi protein tổng hợp do hai protein riêng biệt tiến lại gần nhau do tác dụng của phân tử keo phân tử.
Có một làn sóng các công ty trong không gian phân hủy protein (và rộng hơn là điều chế), bao gồm Arvinas, Nurix Trị liệu, Kymera Trị liệu, C4 Therapeutics, Roivant Discovery, Cedilla Therapeutics và Lycia Therapeutics, v.v.
Một số công ty đang áp dụng các thuật toán AI tiên tiến để thiết kế các hợp chất cảm ứng lân cận. Chẳng hạn, Celeris Therapeutics có trụ sở tại Áo và Hoa Kỳ đã xây dựng nền tảng Celeris One, bao gồm ba hệ thống vùng làm việc: Xanthos, Hephaistos và Hades. Các hệ thống này kết hợp các mạng nơ-ron đồ thị để dự đoán các tương tác và mô hình tổng quát nhằm tạo ra chất hóa học mới, chẳng hạn như trình liên kết và tối ưu hóa đa mục tiêu để cải thiện các đặc tính phân tử, động lực học phân tử và tính toán năng lượng tự do. Quy trình làm việc cũng sử dụng khả năng học sâu hình học và khả năng tổng hợp ngược dựa trên máy học. Celeris Therapeutics điều hành một phòng thí nghiệm tự động để tạo dữ liệu sinh học và tiến hành tổng hợp hóa học tùy chỉnh.

Quy trình làm việc trong phòng thí nghiệm khô khan của Xanthos, nền tảng dựa trên AI của Celeris Therapeutics.
Gần đây chúng tôi đã xuất bản một cái nhìn tổng quan về thị trường thoái hóa protein trong một bài viết Chất phân hủy protein chiếm lĩnh ngành công nghiệp như cơn bão, bao gồm một số nghiên cứu điển hình với tổng quan kỹ thuật về các nền tảng tính toán có liên quan.
Làn sóng đầu tiên của các ứng cử viên thuốc do AI phát triển đi vào lâm sàng
Mặc dù có thể còn sớm để nói rằng việc áp dụng AI trong ngành dược phẩm đã cách mạng hóa hoàn toàn việc khám phá thuốc, nhưng một số công ty “có nguồn gốc từ AI” đã đạt được hiệu quả đáng kể trong việc xây dựng các quy trình điều trị của họ một cách nhanh chóng. Một đặc điểm chung của các công ty như vậy là gì? Mỗi bên đều xây dựng một nền tảng AI chuyên biệt, tích hợp cao, bao gồm nhiều mô hình và nguồn dữ liệu. Một số nền tảng cũng có sẵn dưới dạng phần mềm dưới dạng dịch vụ cho các đối tác R&D bên ngoài, chẳng hạn như Chemistry42.
Một trong những ví dụ sinh động nhất về việc hưởng lợi từ chiến lược “ưu tiên kỹ thuật số” mà ngành đã thấy là Moderna Therapeutics, công ty không chỉ quản lý để kết hợp các phân tích AI tiên tiến trong nghiên cứu của mình mà còn số hóa và tích hợp mọi khía cạnh của quy trình R&D, bao gồm sản xuất và phân phối. Khi đại dịch COVID-19 tấn công thế giới vào đầu năm 2020, Moderna là một trong những công ty đầu tiên có thể tạo ra vắc-xin dựa trên mRNA hiệu quả chỉ trong vòng 2 ngày (!) và đưa nó ra thị trường trong vòng một năm .
Một làn sóng khám phá thành công các phương pháp trị liệu được kích hoạt bởi AI cho thấy khả năng của các công ty dựa trên AI trong việc đưa ra các ứng cử viên thuốc nhanh hơn so với các chương trình tương tự thường được sử dụng.

Xem “Lộ trình của các ứng cử viên ma túy được thiết kế bởi AI,”
Kháng thể đơn dòng LY-CoV555 của AbCellera được phát triển trong vòng ba tháng và được FDA cho phép sử dụng khẩn cấp.
Sơ đồ tri thức của BenevolentAI đã giúp công ty xác định Baricitinib là thuốc kháng vi-rút COVID-19 hiệu quả trong vòng vài ngày (hiện đã được FDA chấp thuận sử dụng). Một phân tử nhỏ khác BEN-8744, một chất ức chế mới để điều trị Viêm loét đại tràng và Viêm da, đã được đưa vào các nghiên cứu tiền lâm sàng muộn trong vòng chưa đầy 24 tháng.
Chất ức chế phân tử nhỏ EXS-21546 của Exscientia đã đánh dấu phân tử đầu tiên do AI thiết kế cho ung thư miễn dịch được đưa vào thử nghiệm lâm sàng ở người (hiện đang ở Giai đoạn I) và được phát hiện chỉ sau XNUMX tháng. Công ty có một số phân tử khác trong các thử nghiệm lâm sàng.
Chất ức chế phân tử nhỏ ISM001-055 của Insilico Medicine, để điều trị Xơ phổi vô căn, được thiết kế mới và đưa vào các nghiên cứu tiền lâm sàng muộn trong vòng 18 tháng (hiện đang ở Giai đoạn I).
Schrodinger có trụ sở tại New York đã phát triển một phân tử nhỏ SGR-1505 để điều trị ung thư hạch tế bào B trong vòng mười tháng và hiện đang trong quá trình ứng dụng IND.
Recursion Pharmaceuticals có trụ sở tại Thành phố Salt Lake đã phát triển một ứng cử viên thuốc cho một căn bệnh hiếm gặp không xác định trong vòng 18 tháng. Công ty có một danh mục lớn và đa dạng gồm các ứng cử viên thuốc lâm sàng và tiền lâm sàng được thiết kế với sự trợ giúp của nền tảng sinh học kỹ thuật số.
Deep Genomics có trụ sở tại Toronto đã sử dụng nền tảng AI Workbench của mình để phát triển một mục tiêu di truyền mới và một ứng cử viên thuốc oligonucleotide tương ứng DG12P1 để điều trị bệnh Wilson di truyền hiếm gặp.
Để theo dõi các ứng cử viên hàng đầu về thuốc lâm sàng do AI phát triển, chúng tôi đã tạo “Lộ trình của các ứng cử viên ma túy được thiết kế bởi AI,” sẽ được cập nhật thường xuyên.
Cần lưu ý rằng sự chú ý liên tục của giới truyền thông đối với AI để khám phá thuốc nên được xem xét một cách thận trọng. Chẳng hạn, kế hoạch của BenevolentAI để cấp phép ngoài ứng cử viên thuốc trị viêm da dị ứng, BEN-2293, đã gặp phải thất bại do chất ức chế pan-Trk hỗ trợ AI không cải thiện được các triệu chứng chàm hoặc ngứa trong thử nghiệm giai đoạn 2a. Công ty trước đây đã xác định kinase thụ thể tropomyosin (Trk) là chất trung gian gây ngứa và viêm trong viêm da dị ứng, dẫn đến sự phát triển của chất ức chế Trk. Mặc dù BEN-2293 đã chứng minh xu hướng hướng tới tác dụng có ý nghĩa lâm sàng trong thử nghiệm giai đoạn 1b, nhưng thử nghiệm giai đoạn 2a cho thấy rằng nó không tốt hơn giả dược trong việc cải thiện mức độ ngứa hoặc mức độ nghiêm trọng của bệnh chàm. Kết quả đặt ra câu hỏi về nền tảng hỗ trợ AI đã đề xuất phương pháp này. Bất chấp thất bại, BenevolentAI vẫn không từ bỏ ứng cử viên thuốc, viện dẫn bằng chứng cho thấy phương pháp điều trị hoạt động tốt hơn ở những bệnh nhân mắc bệnh ở mức độ nặng hơn lúc ban đầu. Công ty hiện đang xem xét dữ liệu trước khi xác định các bước tiếp theo.
Hai mươi công ty AI “năng suất” nhất trong không gian khám phá thuốc
Sau khi lọt vào danh sách rút gọn khoảng 130 công ty từ hơn 380 công ty AI trong Báo cáo BiopharmaTrend AI, chúng tôi đã chọn thêm 20 công ty — sử dụng công thức đánh giá đơn giản nhưng hiệu quả có tính đến các quy trình lâm sàng và tiền lâm sàng của các công ty, khả năng khám phá mục tiêu và thời gian trong kinh doanh. 20 công ty được lựa chọn đã thành lập BPT20: Trí tuệ nhân tạo trong Chỉ số năng suất khám phá thuốc — điểm tham chiếu đầu tiên của ngành để làm nổi bật các công ty đi đầu trong việc ứng dụng AI cho thiết kế thuốc mới, sàng lọc ảo hoặc tái sử dụng thuốc.

AI và phòng thí nghiệm robot của tương lai
Các mô hình học sâu (ví dụ: dựa trên mạng lưới thần kinh sâu) cực kỳ “ngốn dữ liệu”, nghĩa là dù AI có tốt đến đâu thì chất lượng và kích thước của dữ liệu cũng quan trọng không kém đối với các dự đoán nghiên cứu có ý nghĩa. Cách hiệu quả nhất để tạo dữ liệu sinh học chất lượng cao là sử dụng robot. Nếu chúng ta coi quá trình chuyển đổi phát hiện thuốc dựa trên AI hiện đại là một quy trình từng bước, có sẵn rộng rãi và tương đối hiệu quả về chi phí robotics-as-a-service sẽ là phần cuối cùng và quan trọng trong hỗ trợ AI công nghiệp hóa nghiên cứu dược phẩm và công nghệ sinh học. Theo một báo cáo của Arctoris, “Robotics là chìa khóa để cho phép mô hình khám phá vòng kín trở thành hiện thực – đây sẽ là một không gian thú vị để theo dõi trong những năm tới.”
Một số công ty đang xây dựng các cơ sở phòng thí nghiệm được tiêu chuẩn hóa, tự động hóa cao, có thể mở rộng và ngày càng tương thích với sự hướng dẫn của các hệ thống kiểm soát thử nghiệm dựa trên AI và được bổ sung bởi khả năng phân tích và khai thác dữ liệu dựa trên AI. Các cơ sở phòng thí nghiệm “thế hệ tiếp theo” như vậy đang trở nên khả dụng từ xa cho các nhà thực nghiệm nghiên cứu thuốc tiền lâm sàng, làm cho quá trình thử nghiệm tiền lâm sàng trở thành một quy trình tiêu chuẩn hóa và có thể mở rộng hơn. Các nhà cung cấp phòng thí nghiệm từ xa hàng đầu trong danh sách là Automata Labs, Strateos, Emerald Labs và Culture Bioscatics, v.v.
Không gian đang thu hút vốn đầu tư mạo hiểm và khách hàng. Ví dụ: vào tháng 2022 năm 50, Automata Labs có trụ sở tại Vương quốc Anh đã huy động được 2021 triệu đô la để tự động hóa quy trình nghiên cứu trong phòng thí nghiệm. Vào tháng 56 năm 100, Strateos đã huy động được 80 triệu đô la để cải thiện hơn nữa nền tảng SmartLab và công nghệ tự động, rô-bốt từ xa, dành cho các nhà nghiên cứu tiền lâm sàng trên toàn cầu. Culture Bioscatics đã huy động được tổng cộng hơn 2021 triệu đô la, với Series B trị giá 90 triệu đô la mới nhất được công bố vào tháng XNUMX năm XNUMX. Emerald Cloud Labs (ECL) có trụ sở tại San Francisco đã huy động được hơn XNUMX triệu đô la trong những năm qua. Những người dùng đầu tiên loại bỏ nền tảng robot của ECL báo cáo cải thiện 300% đến 700% trong năng suất nghiên cứu. Vào tháng 2022 năm 300, MegaRobo có trụ sở tại Bắc Kinh đã huy động được XNUMX triệu đô la để mở rộng phạm vi đa dạng của các dịch vụ phòng thí nghiệm từ xa do AI điều khiển tự động và các cơ sở rô-bốt.
Sự gia tăng của các phòng thí nghiệm tự động hóa từ xa là một xu hướng dài hạn của ngành, một cách mới để cung cấp các dịch vụ nghiên cứu theo hợp đồng sẽ cực kỳ có lợi cho việc áp dụng lâu dài các chiến lược nghiên cứu “ưu tiên AI” lấy dữ liệu làm trung tâm.
Một số công ty khám phá thuốc dựa trên AI, chẳng hạn như Arctoris, Recursion Pharmaceuticals, Insitro và Generative Bio, đang tiếp cận xu hướng này thông qua một mô hình kinh doanh khác — họ đã xây dựng các cơ sở phòng thí nghiệm được rô-bốt hóa nội bộ để cải thiện năng lực tạo dữ liệu nội bộ cho việc đào tạo của họ. Mô hình AI và xây dựng đường ống của các ứng cử viên thuốc điều trị.
Ví dụ: Arctoris có trụ sở tại Oxford, được thành lập vào năm 2016, đã xây dựng một phòng thí nghiệm ướt hoàn toàn tự động để tạo ra dữ liệu chất lượng cao trên quy mô lớn, đưa vào hồ dữ liệu của Arctoris và cung cấp năng lượng cho nền tảng ra quyết định dựa trên AI của công ty, Ulysses đang cung cấp năng lượng cho nghiên cứu của công ty từ mục tiêu để đánh, dẫn đầu và đến giai đoạn ứng dụng IND.
Sử dụng tự động hóa phòng thí nghiệm ướt từ đầu đến cuối kết hợp với học máy để công nghiệp hóa việc khám phá thuốc
Hệ thống của Arctoris hiện bao gồm một số chương trình tiền lâm sàng về Ung thư và Thần kinh. Arctoris đã huy động được tổng cộng 10.3 triệu đô la trong nhiều vòng từ các nhà đầu tư, bao gồm Future Planet Capital, RT Ventures và Formic Ventures.
Một số công ty khám phá thuốc AI hàng đầu, chẳng hạn như Exscientia và Insilico Medicine, hiện cũng đang xây dựng các phòng thí nghiệm tự động hóa trong nhà để xây dựng “cơ bắp” tạo dữ liệu nội bộ của họ.
Recursion Pharmaceuticals có trụ sở tại Thành phố Salt Lake là một trong những công ty hàng đầu trong lĩnh vực thí nghiệm sinh học được rô-bốt hóa. Cơ sở hạ tầng do AI điều khiển của công ty, được gọi là Hệ thống vận hành đệ quy, là một hệ thống vòng kín tích hợp kết hợp việc tạo dữ liệu nội bộ độc quyền và các công cụ tính toán tiên tiến để tạo ra những hiểu biết mới nhằm bắt đầu hoặc tăng tốc các chương trình trị liệu. Công ty đang tự động hóa thử nghiệm sinh học tiền lâm sàng trên quy mô lớn. Chẳng hạn, hình ảnh kính hiển vi tế bào ghi lại những thay đổi tổng hợp về hình thái tế bào và được xử lý bởi hệ thống thị giác máy tính hỗ trợ AI của công ty. Kể từ năm 2017, Recursion Pharmaceuticals đã tăng khoảng gấp đôi công suất của nền tảng hiện tượng mỗi năm và tăng số lượng thử nghiệm hiện tượng được thực hiện lên tới 2.2 triệu mỗi tuần, dẫn đến ~19 petabyte dữ liệu chiều cao độc quyền.
Điều hướng các nút thắt thử nghiệm lâm sàng với AI
Thử nghiệm lâm sàng là một giai đoạn quan trọng trong quy trình phát triển thuốc, với tỷ lệ thành công trung bình ước tính khoảng 11% cho các ứng cử viên thuốc chuyển từ Giai đoạn 1 sang phê duyệt. Ngay cả khi ứng cử viên thuốc an toàn và hiệu quả, các thử nghiệm lâm sàng có thể thất bại do không đủ tài chính, đăng ký không đủ hoặc thiết kế nghiên cứu kém.
Trí tuệ nhân tạo (AI) là ngày càng được coi là một nguồn cơ hội để cải thiện hiệu quả hoạt động của các thử nghiệm lâm sàng và giảm thiểu chi phí phát triển lâm sàng. Thông thường, các nhà cung cấp AI cung cấp dịch vụ và kiến thức chuyên môn của họ trong ba lĩnh vực chính. Các công ty khởi nghiệp AI trong lĩnh vực đầu tiên giúp mở khóa thông tin từ các nguồn dữ liệu khác nhau, chẳng hạn như bài báo khoa học, hồ sơ y tế, đăng ký bệnh và thậm chí cả yêu cầu y tế, bằng cách áp dụng Xử lý ngôn ngữ tự nhiên (NLP). Điều này có thể hỗ trợ tuyển dụng và phân tầng bệnh nhân, lựa chọn địa điểm và cải thiện thiết kế nghiên cứu lâm sàng cũng như hiểu biết về cơ chế bệnh tật. Ví dụ, khoảng 18% nghiên cứu lâm sàng thất bại do tuyển dụng không đủ, vì một nghiên cứu 2015 báo cáo.
Một khía cạnh khác của sự thành công trong các thử nghiệm lâm sàng là cải thiện sự phân tầng bệnh nhân. Vì bệnh nhân thử nghiệm đắt tiền – chi phí trung bình để đăng ký một bệnh nhân là $ 15,700-26,000 vào năm 2017 — điều cần thiết là có thể dự đoán bệnh nhân nào sẽ có nhiều lợi ích hoặc rủi ro đáng kể hơn từ việc điều trị. Các công ty do AI điều khiển hoạt động với nhiều loại dữ liệu, chẳng hạn như Hồ sơ sức khỏe điện tử (EHR), omics và dữ liệu hình ảnh, để giảm tính không đồng nhất của dân số và tăng sức mạnh nghiên cứu lâm sàng. Các nhà cung cấp có thể sử dụng dấu ấn sinh học giọng nói để xác định tiến triển bệnh thần kinh, phân tích hình ảnh để theo dõi tiến trình điều trị hoặc dấu ấn sinh học di truyền để xác định bệnh nhân có triệu chứng nghiêm trọng hơn.
AI cũng đang hợp lý hóa các quy trình hoạt động của các thử nghiệm lâm sàng. Các nhà cung cấp AI giúp theo dõi sức khỏe bệnh nhân từ nhà của họ, theo dõi phản ứng điều trị và sự tuân thủ của bệnh nhân với các quy trình thử nghiệm. Bằng cách đó, các công ty AI giảm nguy cơ bệnh nhân bỏ học, chiếm tỷ lệ 30% Trung bình. Thông thường, giai đoạn nghiên cứu lâm sàng Giai đoạn 3 yêu cầu 1000-3000 những người tham gia, với một phần trong số họ dùng giả dược. Chính vì vậy sự phát triển của cánh tay điều khiển tổng hợp – Các mô hình AI có thể thay thế các nhóm cá nhân kiểm soát giả dược, do đó giảm số lượng cá nhân cần thiết cho các thử nghiệm lâm sàng – có thể trở thành một xu hướng mới.
Có hơn 80 công ty trong cả ba loại, theo Báo cáo AI của BiopharmaTrend, bao gồm Owkin, PathAI, GNS Healthcare, Neurcuit, AICure và Unlearn.ai.
Liên quan: 8 công ty AI đáng chú ý trong nghiên cứu lâm sàng sẽ theo dõi vào năm 2022
Nhu cầu về các nền tảng thử nghiệm lâm sàng hỗ trợ AI cũng như nhu cầu đầu tư vào lĩnh vực này rất cao, bất chấp môi trường đầu tư lạnh lùng nói chung vào công nghệ sinh học.
Vào tháng 2022 năm 1.9, ConcertAI được định giá 150 tỷ đô la sau khi gửi ngân hàng một vòng Series C trị giá XNUMX triệu đô la để mở rộng các giải pháp phần mềm và dữ liệu trong thế giới thực (RWD) cho nghiên cứu ung thư.
Saama là một công ty có trụ sở tại Thung lũng Silicon được thành lập vào năm 1997 nhưng đã huy động được khoản vốn đầu tư mạo hiểm đầu tiên vào năm 2015. Công ty đã huy động được hơn 500 triệu đô la vốn đầu tư mạo hiểm, bao gồm cả vòng gọi vốn lớn mới nhất trị giá 430 triệu đô la vào tháng 2022 năm XNUMX — từ Carlyle và quỹ đầu tư mạo hiểm từ Merck, Pfizer, Amgen, McKesson và các quỹ khác.
Saama là một trong những công ty hàng đầu trong lĩnh vực phân tích thử nghiệm lâm sàng do AI điều khiển, cung cấp một bộ giải pháp đa dạng: thử nghiệm lâm sàng tăng tốc thông qua trung tâm kiểm soát và phân tích dữ liệu tập trung, bao gồm khả năng xử lý dữ liệu theo thời gian thực; khả năng chất lượng dữ liệu tự động; sắp xếp hợp lý các khả năng đệ trình theo quy định, bao gồm phân tích và đệ trình cảnh giác dược.
Vào tháng 2022 năm 50, Unlearn.AI, một công ty khởi nghiệp đang phát triển dịch vụ 'song sinh kỹ thuật số' cho các thử nghiệm lâm sàng, đã huy động được XNUMX triệu USD.
Vào tháng 2022 năm XNUMX, Bristol Myers Squib đã đầu tư $ 80 triệu trong OWKIN – để giúp tăng cường thiết kế các thử nghiệm thuốc tim mạch, với những cải tiến đối với định nghĩa điểm cuối, xác định các phân nhóm bệnh nhân và ước tính hiệu quả điều trị. OWKIN “kỳ lân” có trụ sở tại Paris và New York đang tận dụng khả năng truy cập dữ liệu đa phương thức chất lượng cao và công nghệ máy học tiên tiến nhất để dự đoán chính xác các tác động điều trị khác nhau đối với các nhóm bệnh nhân nhằm cải thiện kết quả và thiết kế thí nghiệm thử nghiệm lâm sàng. OWKIN cũng đang áp dụng nền tảng AI của mình để khám phá thuốc.
Vào tháng 2022 năm XNUMX, Bristol Myers Squibb cũng đã công bố một thỏa thuận hợp tác mở rộng trong nhiều năm với chuyên gia bệnh lý AI PathAI. Công việc ban đầu trong thỏa thuận mở rộng này sẽ tập trung vào nghiên cứu tịnh tiến quan trọng về ung thư, xơ hóa và miễn dịch học, với mục tiêu tổng thể là chuyển tiếp những nghiên cứu này thành các thử nghiệm lâm sàng. Hai tháng trước đó, PathAI đã ký kết quan hệ đối tác chiến lược kéo dài nhiều năm với GlaxoSmithKline để đẩy nhanh các chương trình nghiên cứu khoa học và phát triển thuốc trong ung thư và viêm gan nhiễm mỡ không do rượu (NASH) bằng cách tận dụng các công nghệ của PathAI trong bệnh lý kỹ thuật số, bao gồm cả việc sử dụng công cụ AIM-NASH của PathAI.
Đáng chú ý, Akkure Genomics của Dublin vừa công bố họ đã huy động vốn từ cộng đồng 1 triệu euro trong một tuần để hỗ trợ các thử nghiệm lâm sàng thông qua nền tảng AI, giúp mọi người tham gia vào các thử nghiệm lâm sàng phù hợp nhất dựa trên dữ liệu về bản thân và tình trạng của họ.
AI trong ngành nghiên cứu hợp đồng
Sự xuất hiện của các công ty nghiên cứu hợp đồng gốc AI mới trong không gian tiền lâm sàng và lâm sàng thách thức hiện trạng của các tổ chức nghiên cứu hợp đồng lớn (CRO) được thiết lập tốt. Họ phản hồi bằng cách kết hợp AI trong các dịch vụ cung cấp cho dược phẩm hoặc hợp tác với các công ty AI để bổ sung cho năng lực nghiên cứu của họ.
Liên quan: Ngành công nghiệp gia công phần mềm R&D dược phẩm đang phát triển: Toàn cảnh.
Ví dụ, Charles River Labs, một tổ chức nghiên cứu hợp đồng giai đoạn đầu có trụ sở tại Hoa Kỳ, đang tìm hiểu sâu hơn về AI bằng cách thiết lập một quan hệ đối tác nhiều năm với Valo Health. Charles River bổ sung công nghệ Opal của Valo có khả năng học hỏi tích cực khi các chương trình được phát triển. Charles River hy vọng việc sử dụng nền tảng học sâu Opal sẽ dẫn đến quy trình nhanh hơn và hiệu quả hơn từ thiết kế phân tử de novo thông qua tối ưu hóa khách hàng tiềm năng. Năm ngoái, Charles River đã thành lập một quan hệ đối tác chiến lược với Valence Discovery cho phép khách hàng của CRO truy cập vào nền tảng trí tuệ nhân tạo của Valence để dự đoán thuộc tính phân tử, hóa học tổng quát và tối ưu hóa đa thông số.
IQVIA đã đầu tư vào khả năng AI trong nhiều năm để gia tăng giá trị cho các thử nghiệm lâm sàng và hoạt động thương mại mà họ đang cung cấp cho khách hàng. Ví dụ, để cải thiện các thử nghiệm lâm sàng, IQVIA phát động Avacare Clinical Research Network™ vào năm 2020, cho phép các trang web so khớp bệnh nhân cho các thử nghiệm nhanh hơn và hiệu quả hơn. Nền tảng này được hỗ trợ bởi các thuật toán AI và có thể hoạt động trên 19 khu vực bệnh tật. Trước đó, một nền tảng Xử lý ngôn ngữ tự nhiên (NLP) Ngôn ngữ học khác của IQVIA đã giành được Giải thưởng Sáng tạo Khốc liệt năm 2019 của Questex. Nền tảng này có thể có nhiều ứng dụng trong chăm sóc sức khỏe và khoa học đời sống, bao gồm xác định mục tiêu, lập bản đồ gen, dự đoán kết quả của bệnh nhân, v.v.
Một xu hướng quan trọng trong ngành nghiên cứu lâm sàng đang chạy thử nghiệm lâm sàng ảo, một thị trường trị giá 8 tỷ đô la. Đại dịch COVID-19 đã buộc các công ty dược phẩm phải chuyển sang giám sát từ xa, cải thiện việc đăng ký bệnh nhân, ứng dụng để theo dõi sự tham gia của bệnh nhân, khám bệnh từ xa, phân cấp và các biện pháp khác để duy trì hoạt động thử nghiệm. Vì nhu cầu về các giải pháp như vậy tăng lên đáng kể, CRO đã gấp rút bổ sung các khả năng ảo và phi tập trung vào các dịch vụ của họ. Công nghệ AI tỏ ra vô giá trong việc tạo và chạy các dự án như vậy để giúp tổng hợp dữ liệu và tăng tốc quá trình thử nghiệm lâm sàng.
Những gã khổng lồ công nghệ theo đuổi khám phá thuốc và công nghệ sinh học
Những thành công đã đề cập trước đó của DeepMind và Meta của Alphabet trong việc giải các câu đố nghiên cứu sinh học cơ bản, như dự đoán cấu trúc protein ở quy mô lớn bằng cách sử dụng các mô hình ngôn ngữ và học sâu, chỉ là phần nổi của tảng băng chìm: hầu hết mọi gã khổng lồ công nghệ hàng đầu hiện nay đều kinh doanh khoa học đời sống , bằng cách nào đó.
Alphabet (công ty mẹ của Google) có hàng chục khoản đầu tư vào các dự án khoa học đời sống, bao gồm công cụ tìm kiếm thuốc thử dựa trên AI BenchSci, AI và vật lý lượng tử có trụ sở tại Trung Quốc trong công ty khám phá thuốc XtalPi, công ty nghiên cứu gen cá nhân 23andMe và phát triển thuốc dựa trên AI. kỳ lân OWKIN để kể tên một số. Vào năm 2021, Alphabet cùng với DeepMind đã ra mắt Phòng thí nghiệm Isomorphic để tập trung vào việc áp dụng trí tuệ nhân tạo để khám phá sinh học cơ bản và khám phá thuốc.
Ngoài nhiều dự án và hoạt động khác trong nghiên cứu dược phẩm và công nghệ sinh học, Alphabet còn có một thực thể toàn diện, Verily, dành riêng cho Khoa học Đời sống và MedTech.
Microsoft, một nhà phát triển phần mềm toàn cầu, có dấu ấn sâu sắc trong Khoa học đời sống, với hàng chục hợp tác nghiên cứu với các hãng dược phẩm lớn, cung cấp cơ sở hạ tầng để xử lý dữ liệu lớn bằng cách sử dụng các mô hình máy học quy mô lớn. Trong số những sáng kiến mới nhất của Microsoft là Mô hình MoLeR, một công cụ mới đang được phát triển bởi nhóm hóa học tổng quát của công ty với sự cộng tác của Novartis. Mô hình MoLeR – không giống như các công cụ tổng quát khác – sử dụng học sâu để đưa ra các cấu trúc mới dựa trên một giàn giáo nhất định đóng vai trò là cơ sở ban đầu cho quy trình tổng quát. Một ví dụ khác là AI4Khoa học, một liên doanh mới của Microsoft kết hợp hóa học tính toán, vật lý lượng tử, học máy, sinh học phân tử, động lực học chất lỏng và công nghệ phần mềm để hiện thực hóa tầm nhìn về cái gọi là “mô hình thứ năm” của khoa học.
Liên quan: Làm thế nào “Big Tech” đang dần giành được thị trường dược phẩm
Một công ty đặc biệt tích cực trong bối cảnh này là nhà sản xuất phần cứng cho ngành công nghiệp trò chơi và máy tính cá nhân, NVIDIA. Công ty công nghệ này đã ra mắt Clara Discovery, một tập hợp các khuôn khổ, ứng dụng và mô hình AI cho phép khám phá thuốc tăng tốc bằng GPU, với sự hỗ trợ cho nghiên cứu về bộ gen, protein, kính hiển vi, sàng lọc ảo, hóa học điện toán, trực quan hóa, hình ảnh lâm sàng và xử lý ngôn ngữ tự nhiên (NLP). Và vào tháng 2022 năm XNUMX, công ty đã giới thiệu Clara Holoscan MGX™, một nền tảng dành cho ngành thiết bị y tế để phát triển và triển khai các ứng dụng AI thời gian thực ở vùng biên, được thiết kế đặc biệt để đáp ứng các tiêu chuẩn quy định bắt buộc. Clara Holoscan nhắm đến một kiến trúc tham chiếu cấp độ y tế, tất cả trong một, cũng như hỗ trợ phần mềm dài hạn, để đẩy nhanh sự đổi mới trong ngành thiết bị y tế.
Tương lai của AI trong khám phá thuốc: mọi thứ “lượng tử”
Hầu hết các công cụ phần mềm được sử dụng để khám phá thuốc và nghiên cứu sinh học đều dựa trên cơ học phân tử - một biểu diễn đơn giản hóa của các phân tử, về cơ bản là rút gọn chúng thành “quả bóng và cây gậy”: các nguyên tử và liên kết giữa chúng. Bằng cách này, nó dễ dàng hơn để tính toán, nhưng độ chính xác bị ảnh hưởng rất nhiều. Để đạt được độ chính xác đầy đủ, người ta phải tính đến hành vi điện tử của các nguyên tử và phân tử, tức là xem xét các hạt hạ nguyên tử - electron và proton. Đây chính là nội dung của các phương pháp cơ học lượng tử (QM) — và lý thuyết này không phải là mới, đã có từ những thập kỷ đầu của thế kỷ 20.
Tuy nhiên, các phương pháp lượng tử đặc biệt tốn kém về mặt tính toán - và cho đến những thập kỷ gần đây, nó là một rào cản ngăn cản lý thuyết lượng tử ảnh hưởng đến khía cạnh thực tế của mọi thứ. Do sự tăng trưởng theo cấp số nhân của sức mạnh tính toán sẵn có, các phương pháp lượng tử cuối cùng đã trở thành công cụ có giá trị trong tay các nhà khoa học.
Một số công ty đang hợp nhất học máy và lý thuyết lượng tử để cải thiện đáng kể khả năng lập mô hình của các hệ thống khám phá thuốc của họ. Ví dụ: các nhà khoa học tại XtalPi, một công ty công nghệ có trụ sở tại Trung Quốc và Hoa Kỳ được hỗ trợ bởi Sequoia China, Tencent và Google, đã xây dựng nền tảng Phát hiện và Phát triển Thuốc Kỹ thuật số Thông minh (ID4) của họ, kết hợp cơ học lượng tử, trí tuệ nhân tạo và hiệu suất cao. thuật toán điện toán đám mây. ID4 cho phép dự đoán với độ chính xác cao các đặc tính hóa lý và dược phẩm của các ứng cử viên thuốc phân tử nhỏ, cũng như cấu trúc tinh thể của chúng — các yếu tố quan trọng trong R&D thuốc.
Một công ty khác đang phát triển lĩnh vực này là Aqemia có trụ sở tại Paris. Công ty tập trung vào de novo, thiết kế dựa trên cấu trúc của các phân tử giống chì bằng cách kết hợp lượng tử và trí tuệ nhân tạo (AI). Một thuật toán cơ học thống kê lấy cảm hứng từ lượng tử độc đáo dự đoán mối quan hệ giữa hợp chất và mục tiêu điều trị một cách chính xác và nhanh hơn 10,000 lần so với đối thủ cạnh tranh. AI của Aqemia có thể tạo ra các hợp chất với độ chính xác ngày càng cao bằng cách nhận phản hồi từ bộ dự đoán mối quan hệ.
Cuối cùng là Pharmacelera có trụ sở tại Barcelona, một công ty máy tính áp dụng lý thuyết lượng tử để tăng cường thiết kế thuốc thông qua hai gói phần mềm chính của họ: PharmScreen và PharmQSAR. Công cụ đầu tiên cho phép sàng lọc ảo dựa trên phối tử chính xác bằng cách sử dụng thuật toán căn chỉnh phối tử 3D có độ chính xác cao dựa trên các trường tương tác. Nó có thể tạo ra tỷ lệ đa dạng cao hơn giữa các khách hàng tiềm năng so với các phương pháp và công cụ cổ điển. Công cụ thứ hai — PharmQSAR, là một công cụ định lượng mối quan hệ cấu trúc-hoạt động (QSAR) 3D cho phép kết hợp nhiều lĩnh vực tương tác để thực hiện các nghiên cứu CoMFA/CoMSIA.
Liên quan: 12 công ty sử dụng thuyết lượng tử để tăng tốc khám phá thuốc
Một xu hướng công nghệ khác - tương lai hơn - khai thác lý thuyết lượng tử, liên quan đến việc tạo ra một máy tính lượng tử. Với nhiều thập kỷ tiến bộ trong lý thuyết lượng tử và tiến bộ đồng thời trong một số lĩnh vực phần mềm và phần cứng, cuối cùng chúng ta cũng bước vào kỷ nguyên máy tính lượng tử trở nên khả thi trên thực tế.
Trong khi chúng ta đang ở những ngày đầu tiên của điện toán lượng tử, một số công ty đã tích hợp các yếu tố của điện toán lượng tử vào khám phá thuốc điện toán.
Chẳng hạn, POLARISqb là nhà phát triển phần mềm khám phá thuốc đầu tiên trên thế giới có trụ sở tại Vương quốc Anh được xây dựng cho máy tính lượng tử, kết hợp trí tuệ nhân tạo và phương pháp tiếp cận lượng tử. Trọng tâm của công nghệ POLARISqb là nền tảng thiết kế thuốc Tachyon, được sử dụng để thực hiện công việc thiết kế phân tử phân tán trên đám mây, được quản lý bởi một quy trình tự động cho phép tìm kiếm các thư viện hóa chất lớn trong khi chạy song song nhiều dự án. Bằng cách phát triển phần mềm độc quyền cho các hệ thống lượng tử, công ty tuyên bố rằng họ có thể tăng tốc đáng kể việc thiết kế thuốc và đạt được chất lượng cao hơn. Do “thuyết bất khả tri” vốn có của hệ thống Tachyon, nó có thể hoạt động trong nhiều bệnh và chỉ định.
Menten AI là một công ty khởi nghiệp của Canada được thành lập vào năm 2018 chuyên phát triển nền tảng phần mềm để thiết kế protein được hỗ trợ bởi máy học và điện toán lượng tử. Công ty sử dụng các thuật toán tối ưu hóa lượng tử độc quyền mà họ tin rằng có thể cải thiện đáng kể độ chính xác của việc khám phá thuốc đồng thời giảm chi phí và thời gian phát triển.
Để tóm tắt bài đăng này, chúng ta hãy tham khảo dự đoán của Tiến sĩ Christopher Savoie, Đồng sáng lập và Giám đốc điều hành tại Zapata Computing, một công ty phần mềm lượng tử của Mỹ, về nghiên cứu tiên tiến trong lĩnh vực này, mà ông đã trình bày trong một cuộc phỏng vấn cho BiopharmaTrend:
“Lượng tử sẽ là một phần của mọi hoặc gần như mọi quy trình khoa học dữ liệu và học máy trong dược phẩm sinh học trong tương lai. Tôi tin rằng nó sẽ là một phần không thể thiếu của nó. Nếu bạn có thể có được một mô hình chính xác hơn bằng cách sử dụng công nghệ lượng tử - thì tại sao bạn lại không làm điều đó?”
Các mô hình ngôn ngữ lớn đạt được những bước tiến trong khám phá thuốc
Các mô hình ngôn ngữ lớn (LLM) như ChatGPT của OpenAI đang được các công ty công nghệ sinh học sử dụng, chẳng hạn như Thuốc Insilico, ngây thơvà Ngoại lệ, để hỗ trợ khám phá thuốc.
ChatGPT giúp các nhà khoa học tương tác với AI và các công cụ máy học, giúp dữ liệu dễ tiếp cận hơn. Chẳng hạn, Insilico Medicine sử dụng ChatGPT để tương tác với nền tảng khám phá mục tiêu của họ, PandaOmics, trong khi người sáng lập Ainnocence Lương P. hình dung các phiên bản chuyên biệt như Bio ChatGPT hoặc Med ChatGPT. Exscientia sử dụng LLM để tạo ra các xác nhận cơ học, có cấu trúc cho biểu đồ tri thức của họ.
LLM cũng đóng vai trò là công cụ tìm kiếm nâng cao trong khoa học sinh học. Google và DeepmindChatbot Med-PaLM của Med-PaLM cung cấp câu trả lời cho các câu hỏi về y tế, đồng thời Nhân từ có vẻ hào hứng với tính năng plug-in truy xuất của ChatGPT, tính năng này có thể giúp tùy chỉnh chức năng trò chuyện dựa trên dữ liệu của chính họ.
Bất chấp tiềm năng của LLM trong khám phá thuốc, một số công ty như Công ty trị liệu BioXcel và đường ruột vẫn thận trọng về việc áp dụng công nghệ, với lý do lo ngại về tính chính xác và quyền riêng tư.
Điều rõ ràng là sự gia tăng của ChatGPT và các mô hình AI tổng quát khác, chẳng hạn như AlphaFold của DeepMind, đã nâng cao nhận thức về các ứng dụng tiềm năng của chúng trong công nghệ sinh học, khuyến khích các công ty khám phá lợi ích của chúng trong khám phá và phát triển thuốc.
Chủ đề: Xu hướng công nghiệp
- Phân phối nội dung và PR được hỗ trợ bởi SEO. Được khuếch đại ngay hôm nay.
- PlatoData.Network Vertical Generative Ai. Trao quyền cho chính mình. Truy cập Tại đây.
- PlatoAiStream. Thông minh Web3. Kiến thức khuếch đại. Truy cập Tại đây.
- Trung tâmESG. Ô tô / Xe điện, Than đá, công nghệ sạch, Năng lượng, Môi trường Hệ mặt trời, Quản lý chất thải. Truy cập Tại đây.
- BlockOffsets. Hiện đại hóa quyền sở hữu bù đắp môi trường. Truy cập Tại đây.
- nguồn: https://www.biopharmatrend.com/post/615-pharmaceutical-artificial-intelligence-key-developments-in-2022/



