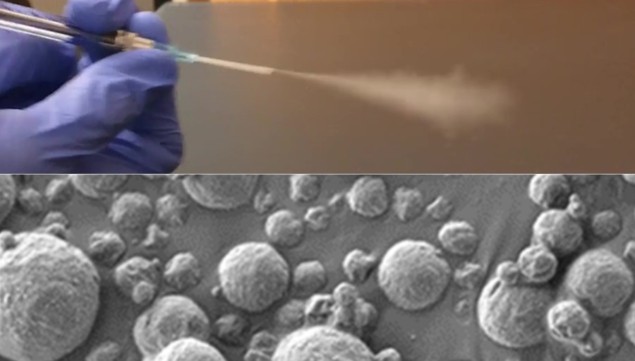
リスクのあるグループの肺がんを診断するための標準的な技術である低線量CTは、臨床試験で肺がんによる死亡を20~25%減少させました。しかし、資源が乏しい環境ではこのスクリーニング技術へのアクセスが制限される可能性があり、そのような地域では肺がんによる死亡率が不釣り合いに高くなります。マサチューセッツ工科大学の研究者 (マサチューセッツ工科大学(MIT)) は、ナノ粒子センサーの吸入に基づく簡単な検査を開発することで、肺がんの早期発見におけるこの不公平に対処したいと考えています。
新しいスクリーニング検査については、 科学の進歩は、PATROL と呼ばれる無針診断プラットフォームで、次の 3 つのモジュールを統合しています。携帯用吸入ユニットと、そして多重化可能な紙ベースの側方流動アッセイ (LFA) です。
ABN は、ペプチド基質を介して合成 DNA バーコードなどのレポーターと結合したポリマー ナノ粒子から作られます。高い予測力を持つ最小限のプローブセットを特定するために、研究者らは、癌関連プロテアーゼに曝露されると切断される候補ペプチドのライブラリーを調べた。彼らは、潜在的なナノセンサーとして20のペプチドを選択し、正確な診断結果が得られる可能性が高いXNUMXつのABNの組み合わせを特定するためにマウスでテストを実施した。
スクリーニング検査を受けるために、患者は肺への沈着を最適化するためにミクロンサイズのエアロゾルに配合されたABNを吸入します。これらのナノセンサーが肺がん関連プロテアーゼなどのがんバイオマーカーに遭遇すると、DNA バーコードが粒子から切断されて循環中に放出され、最終的に尿中に濃縮されます。これらのレポーターは、LFA ベースの尿検査を使用して検出できます。
複雑な実験装置を必要とせずに尿サンプルを迅速に分析するために、チームは室温で 1 枚の紙ストリップ上の 4 つの異なる DNA バーコードを定量できる LFA を開発しました。また、ナノセンサーはネブライザーまたは手持ち式吸入器を使用して送達されるため、患者は自宅で PATROL テストを自分で行うことができます。
「私たちは、このアッセイを低リソース環境で利用できるポイントオブケアとして推進していました。そのため、サンプル処理や増幅を行わず、単にサンプルを紙の上に正確に配置できるようにするという考えでした。 20 分で読み上げられます」と上級著者は言います サンジータバティア プレス文で
研究者らは、CTスキャナーが広く普及していない低・中所得国においてPATROLが特に重大な影響を与える可能性があると指摘している。 「私たちの目標は、高い特異性と感度でがんを検出できる方法を提供し、アクセシビリティの閾値を下げることであり、それによって肺がんの早期発見における資源の格差と不公平を改善できることを期待しています」と共同主著者は付け加えた。 銭忠.
生体内 評価
研究者らは、ナノセンサーがマウスの肺がんを検出できるかどうかをテストし、腫瘍が形成され始めてから7.5週間後に動物を検査した(おそらくヒトのステージ1または2のがんと相関している)。彼らは、ドライパウダー吸入器は人間では肺深部への優れた沈着を提供するが、呼吸で作動するため齧歯動物には適さないと指摘している。そこで代わりに、マウスを吸入タワーに入れ、噴霧されたナノセンサーに曝露した。
ABN 吸入の 2 時間後、研究者らは動物から尿サンプルを収集し、質量分析法を使用してレポーターを定量しました。彼らは、腫瘍微小環境に曝露された基質がDNAバーコードを循環中に放出すること、および4つのレポーターすべてからの尿シグナルが腫瘍を有するマウスと健康なマウスで異なることを発見した。教師なしアルゴリズム手法の使用により、すべての腫瘍担持マウスを健康な対応マウスから区別することが可能になりました。
彼らは、吸入可能なABNが「マウス自生肺腺癌の早期検出に強力な威力を発揮する」と結論付けた。
吸入して検知する
最後に、研究者らは「吸入および検出」PATROL プラットフォーム全体のパフォーマンスをテストしました。彼らは、直径約 15 nm の DNA コード化 ABN を合成し、同じ肺がんマウス モデルとネブライザー送達を使用して、LFA を使用した尿中 DNA レポーター検出を検証しました。
各バーコードの尿中濃度を比較すると、報告されたプローブのうち 3 つ (4 つ目は除く) の切断において、健康なマウスと担癌マウスの間で有意な差があることが明らかになりました。 LFA で検出された尿の読み取り値は、質量分析測定と同様の信号対雑音比を示しました。ここでも、教師なしクラスタリング アルゴリズムを使用すると、すべてのマウスを初期段階の肺がんに分類できます。
受信者動作特性(ROC)分析により、プローブのうち 0.82 つが有能な単一分類器として機能し、ROC 曲線下面積(AUC)値が 0.88、0.85、0.93 であることが示されました。 100 つのプローブを組み合わせると、AUC は 75.2 に増加しました。 LFA は XNUMX% の特異性で、マイクロ CT に匹敵する XNUMX% の感度で DNA レポーターを検出しました。

肺がん検診で長期生存率が劇的に向上
研究チームはまた、吸入可能な ABN の安全性プロファイルを調べたところ、噴霧による ABN の単回投与から 7 日後にマウスに一般的な毒性や血管系の詰まりは見られませんでした。
「総合すると、PATROLは早期段階で高感度かつ特異的な肺がん検出を達成するだけでなく、リソースが限られた環境での容易な導入を可能にするという大きな臨床的可能性を秘めている」と研究者らは結論づけている。次に、人間の生検サンプルを分析して、センサーパネルが人間のがんも検出できるかどうかを確認する予定で、できれば人間の患者での臨床試験も続けたいと考えています。
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- PlatoData.Network 垂直生成 Ai。 自分自身に力を与えましょう。 こちらからアクセスしてください。
- プラトアイストリーム。 Web3 インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- プラトンESG。 カーボン、 クリーンテック、 エネルギー、 環境、 太陽、 廃棄物管理。 こちらからアクセスしてください。
- プラトンヘルス。 バイオテクノロジーと臨床試験のインテリジェンス。 こちらからアクセスしてください。
- 情報源: https://physicsworld.com/a/inhalable-nanosensors-could-increase-access-to-lung-cancer-screening/



