Yeni FDA eSTAR şablonunu kullanmak aynı zamanda eSTAR proje yönetiminin 510k ve De Novo başvurularınızı hazırlaması için yeni bir süreç gerektirir.
Yeni FDA eSTAR şablonundan kaynaklanan on (10) büyük değişikliğin özeti
1 Ekim 2023 itibarıyla tümü 510k ve De Novo gönderimleri FDA'ya katılmak için artık yeni FDA eSTAR şablonunun kullanılması gerekiyor ve şablon şu adrese yüklenmelidir: FDA Müşteri İşbirliği Portalı (CCP). Dün FDA, 510k elektronik başvuru gerekliliklerini açıklayan güncellenmiş bir kılavuz yayınladı ancak Tıbbi Cihaz Akademisi'nin başvuru sürecinde yeni eSTAR şablonlarından kaynaklanan on (10) önemli değişiklik var:
- Artık içindekiler tablosuna ihtiyacımız yok.
- Artık cilt ve belge yapısını kullanmıyoruz.
- Artık tüm gönderimin bölümlenmesine veya sayfalandırılmasına uymamız gerekmiyor.
- Artık RTA taraması veya kontrol listesi (mevcut değil) konusunda endişelenmiyoruz.
- Artık yönetici özeti oluşturma zahmetine girmiyoruz (bu isteğe bağlıdır).
- Artık Sınıf 3 cihazlar için bir bölümümüz yok çünkü artık Sınıf 3 510(k) cihaz yok.
- Artık FDA Form 3514'ü kullanmıyoruz çünkü bu içerik artık eSTAR'a dahil edilmiştir.
- Artık bir Uygunluk Beyanı oluşturmuyoruz çünkü eSTAR otomatik olarak bir Uygunluk Beyanı oluşturur.
- Artık 510(k) Özeti oluşturmanızı önermiyoruz çünkü eSTAR otomatik olarak bir tane oluşturuyor
- Artık FedEx'i kullanmıyoruz çünkü bunun yerine FDA CCP'ye elektronik olarak yükleme yapabiliyoruz.
510k gereksinimlerinde farklı olan nedir?
FDA'nın piyasaya arz öncesi bildirim sürecinde (yani 510k süreci) algılanan tüm değişikliklere rağmen, format ve içerik gereklilikleri pek değişmedi. 510k sürecindeki en önemli son değişiklik, şunları içerme zorunluluğuydu: siber güvenlik testi.
eSTAR Proje Yönetiminin Ana Hatları
20k gönderimde 510 bölüm vardı. Tıbbi Cihaz Akademisi'nin danışmanlık ekibi her bölümde yer alacak belgeler için bir şablon oluşturdu. eSTAR proje yönetimi farklıdır çünkü referans verilecek bölüm numaraları yoktur. Her şeyi açıklığa kavuşturmak için, ait olduğu bölümü tanımlamak üzere her dosya adının başında bir veya iki kelime kullanmanızı öneririz. Kelimeler, FDA tarafından kullanılan yer imleriyle eşleşmelidir. Ancak dosya adlarını çok uzun yapmamaya dikkat etmelisiniz. Aşağıda tüm bölümlerin bir listesi bulunmaktadır:
- İdari Bilgiler;
- Cihaz Açıklaması;
- Yüklemler ve Tözsel Eşdeğerlik;
- Faydalar, Riskler ve Azaltma Önlemleri;
- Etiketleme;
- Yeniden İşleme, Sterilite ve Raf Ömrü;
- Biyouyumluluk;
- Yazılım/Ürün Yazılımı ve Siber Güvenlik/Birlikte Çalışabilirlik
- Yazılım;
- EMC, Kablosuz, Elektrik, Mekanik ve Termal Güvenlik;
- Performans testi;
- Kalite Yönetimi; Ve
- İdari Dokümantasyon.
Fayda, Riskler ve Azaltma Önlemleri Bölümü yalnızca De Novo Sınıflandırma Talepleri için geçerlidir. Kalite Yönetimi Bölümü, Kalite Yönetim Sistemi Bilgileri, Tesis Bilgileri, Piyasa Sonrası Çalışmalar ve Referanslar alt bölümlerini içerir. Ancak diğer üç alt bölüm Health Canada eSTAR pilot programının bir parçası olduğundan çoğu gönderimde yalnızca Referanslar alt bölümü görünecektir. Diğer bölümler ve alt bölümler, eSTAR'da seçtiğiniz açılır menü seçimlerine bağlı olarak kısaltılacak veya gizlenecektir. Örneğin, cihazınızda kablosuz işlevsellik veya çıkarılabilir depolama sürücüsü yoksa siber güvenlik bölümü gizli kalacaktır.
510 gönderim için artık İçindekiler tablosuna gerek yok
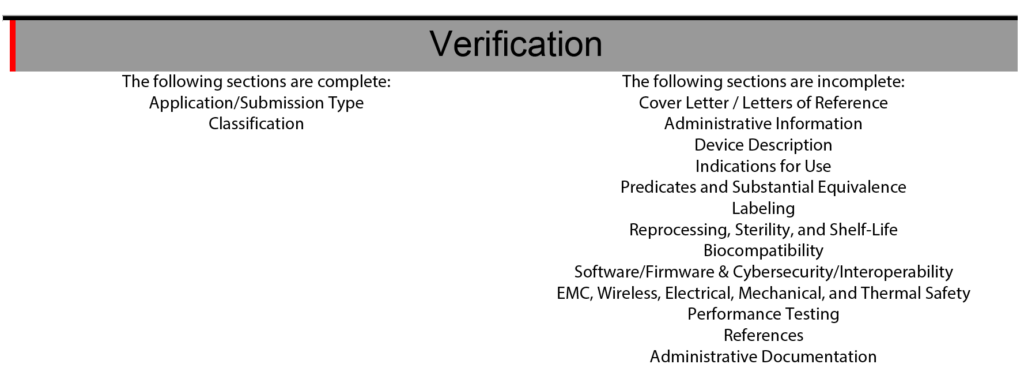
FDA eCopy formatını kullanan 510 başvuru için İçindekiler Tablosu gerekliydi ve Medical Device Academy, İçindekiler Tablosunu bir proje yönetim aracı olarak kullandı. Bazen, atamaları iletmek ve 510k projesini yönetmek için hâlâ İçindekiler şablonumuzu kullanıyoruz. İçindekiler Tablosunun bölümleri de renk kodlu olacaktır yeşil, mavi, Sarı, ve kırmızı Her bölümün durumunu iletmek için. FDA eSTAR proje yönetimi, bölümün eksik, tamamlanmış veya isteğe bağlı olduğunu belirtmek için şablonun yan tarafındaki renkli çubuklarla benzer bir renk kodlama süreci kullanır.

eSTAR'ın ayrıca eSTAR proje yönetimine yardımcı olmak için şablonun sonunda bir doğrulama bölümü vardır. Doğrulama bölümü, FDA eSTAR'ın 13 ana bölümünün her birini listeler. Bölümler tamamlandığında bölümün adı doğrulama bölümünün sağından sol tarafına otomatik olarak taşınır. eSTAR şablonunu uygulamaya geçirdiğim son iki yıl boyunca (2021 – 2023), her bölümün durumunu iletmek için yalnızca eSTAR'a güvenmeyi yavaş yavaş öğrendim. 510k gönderimin her bölümüne sorumluluk atamak için hâlâ İçindekiler basit listelerini ve Asana gibi proje yönetimi araçlarını kullanıyoruz. Her 510k bölümünün durumunu kontrol etmek için eSTAR doğrulama bölümünü kullanmak, ekibimizin eSTAR'ı her kullandığımızda yeterliliğini de artırır.
eSTAR proje yönetimi için Dropbox'ı kullanma
Bir Q-Sub toplantısına yönelik PreSTAR şablonları, bir eSTAR şablonunun yaklaşık yarısı kadar uzunluktadır (yani 15'dan fazla sayfa yerine 30 sayfa) ve 510k gönderimi, Q-Sub'dan çok daha fazla ek gerektirir. Bu nedenle, genellikle PreSTAR'ın gözden geçirilmiş taslağını incelemesi için bir ekip üyesine e-postayla gönderebiliriz, ancak neredeyse tamamlanmış bir eSTAR'ı bir ekip üyesiyle paylaşmak için e-postayı kullanamayız. Bu nedenle Tıbbi Cihaz Akademisi, dropbox eSTAR'ın revizyonlarını ekip üyeleri arasında paylaşmak. Müşterilerimizden bazıları revizyonları paylaşmak için One Drive veya Google Drive kullanıyor. Ayrıca her test türü için alt klasörler oluşturuyoruz. Bu, eSTAR'ın bir bölümüne ilişkin tüm belgeleri ve test raporlarını tek bir yerde tutar. Örneğin, yazılım doğrulama belgeleri bir 510k projesi için Dropbox klasörünün bir alt klasöründe düzenlenecektir.
FDA eSTAR şablonu yerine FDA eKopyalarını kullanırken, 1-20 cilt numaralarına göre etiketlenen ve düzenlenen yirmi alt klasör kullandık. Bu 20 bölümden bazıları artık geçerliliğini yitirmiştir (örneğin, Sınıf III Özet) ve diğerleri (örneğin, Kullanım Endikasyonları) doğrudan eSTAR şablonuna entegre edilmiştir. Bu nedenle, bir ekibin 8k projesi için belgeleri ve test raporlarını düzenlemek için yalnızca 10-510 alt klasöre ihtiyacı olabilir.. Genellikle bu belgeleri ve test raporlarını başvuru hazırlığının sonuna kadar eklemiyoruz çünkü FDA, eSTAR'ın yeni bir versiyonunu yayınlarsa, ekler eski bir eSTAR versiyonundan yeni versiyona aktarılmayacaktır.
Başarılı eSTAR proje yönetimi için ekip işbirliğinin koordinasyonu kritik öneme sahiptir
Geçmişte, Tıbbi Cihaz Akademisi bir FDA e-Kopyası düzenlemek için her zaman bir cilt ve belge yapısı kullanıyordu çünkü bu, farklı ülkelerden bile olsa birden fazla ekip üyesinin aynı 510k başvuru üzerinde aynı anda çalışmasını kolaylaştırıyordu. Birçok müşteri, birden fazla kullanıcının eşzamanlı işbirliğini kolaylaştırmak için SharePoint veya Google Dokümanlar'ı kullanacaktır. Ne yazık ki eSTAR, yalnızca Adobe Acrobat Pro'da düzenlenebilen güvenli bir şablon olduğundan aynı anda iki kullanıcı tarafından düzenlenemez. Bu nedenle, eSTAR şablonu güncellenirken ekibin iletişim kurması ve revizyonları takip etmesi gerekir. İletişim için, anlık mesajlaşma uygulamaları (örn. Slack veya Whatsapp) ve e-postanın bir kombinasyonunu kullanıyoruz; düzeltmeler ise editörün baş harfleri ve tarihinin dosya adına eklenmesiyle takip ediliyor (örn. nIVD 4.3 rvp 12-5-2023. pdf).
Akran değerlendirmelerinin önemi
Başvurunun Müşteri İşbirliği Portalına (CCP) yüklenebilmesi için FDA eSTAR'ın her bölümünün tamamlanması gerekir. FDA eSTAR eksikse, ÇKP dosyayı eksik olarak tanımlayacaktır. Dosyayı yükleyemeyeceksiniz. eSTAR'da soruların yanlış cevaplanması durumunda soruların cevaplanma şekli nedeniyle doldurulması gereken bölümler etkinleştirilemeyebilir. Aşağıda eSTAR sorularının nasıl yanlış cevaplanabileceğine dair iki örnek verilmiştir.
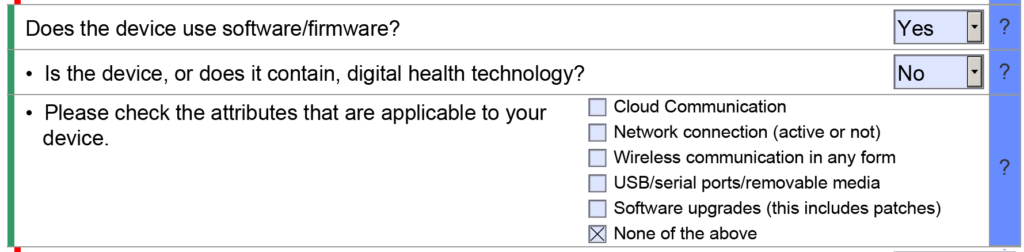
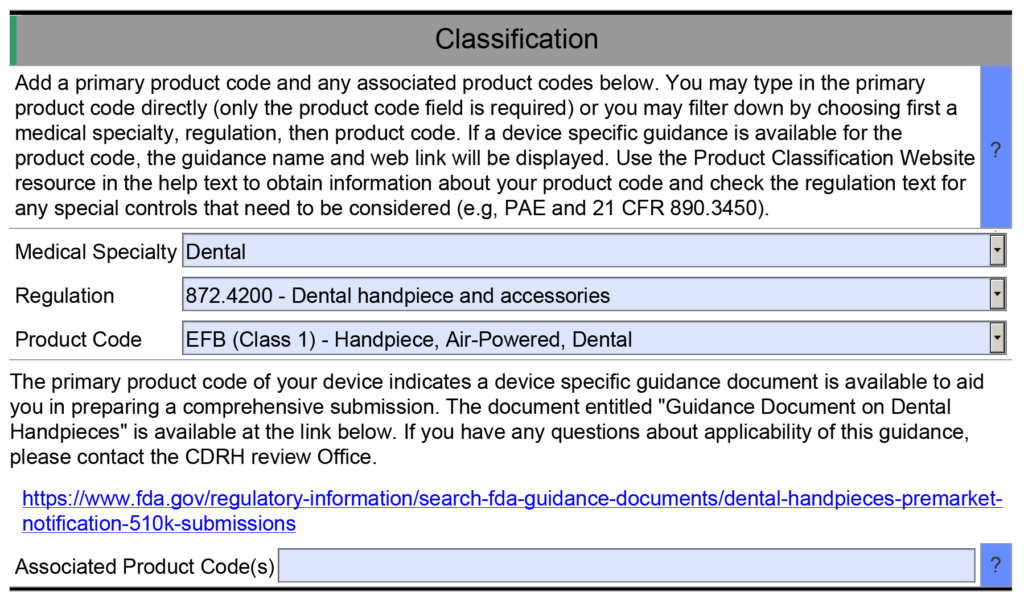
- Örnek 1 – FDA eSTAR'ın yararlı kaynak özelliklerinden biri, birçok alanın açılır yanıt menüsüyle doldurulmuş olmasıdır. Bir örnek eSTAR'ın Sınıflandırma bölümünde bulunmaktadır. Bu bölüm, başvuruyu yapan kişinin üç soruyu yanıtlayarak cihazın sınıflandırmasını tanımlamasını gerektirir: 1) inceleme paneli, 2) sınıflandırma düzenlemesi ve 3) üç harfli ürün kodu. Bu alanların her biri alanı doldurmak için bir açılır menü kullanır ve ikinci ve üçüncü soruların açılır seçenekleri önceki sorunun yanıtlarına bağlıdır. Ancak üçüncü soru için alana ürün kodunu manuel olarak yazarsanız eSTAR, cihazınız için geçerli herhangi bir özel kontrol kılavuzu belgesini tanımlamayacaktır. Halihazırda geçerli bir özel kontroller kılavuz belgesinden haberdar olmadığınız sürece, eSTAR'da özel kontroller hakkındaki soruları "Yok" şeklinde yanıtlayacaksınız. eSTAR, yalnızca açılır menüden bir ürün kodu seçmeniz durumunda cihazınız için özel bir kontrol kılavuzu belgesi tanımlayacaktır, ancak FDA inceleme uzmanı hangi özel kontrol kılavuzu belgelerinin geçerli olduğunu bilir. Bu nedenle FDA, kapsamlı inceleme başlamadan önce eSTAR'ın teknik taramasını gerçekleştirir.
- Örnek 2 – Harici olarak iletişim kuran bir cihaz için kümülatif temas süresini 24 saatten az belirtirseniz, eSTAR şablonu sizden şu biyouyumluluk uç noktalarını değerlendirmenizi bekleyecektir: sitotoksisite, duyarlılık, tahriş, sistemik toksisite ve pirojenite.
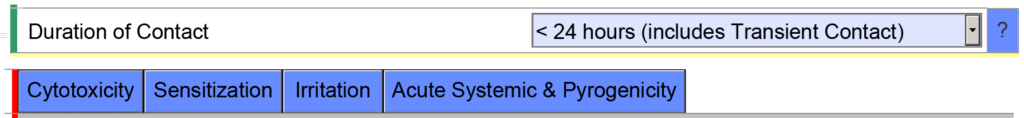
Ancak kümülatif temas süresinin 30 günden az olduğunu belirtirseniz eSTAR şablonu ek biyouyumluluk uç noktalarıyla doldurulacaktır. eSTAR kümülatif kullanım süresinin ne olduğunu bilmiyor ancak FDA incelemecisi bilecek. Bu nedenle FDA, kapsamlı inceleme başlamadan önce eSTAR'ın teknik taramasını gerçekleştirir.

Gönderiminizin tüm bölümlerinin tamamlandığından emin olmak için, her şeyin doğru şekilde tamamlandığından emin olmak amacıyla ikinci bir kişinin tüm yanıtları incelemesini sağlamak faydalı olacaktır. Her hafta 510 bin başvuru hazırlayan deneyimli danışmanlar bile eSTAR alanlarından birinde hata yapıp bir soruyu yanlış cevaplayabiliyor. Bu nedenle bu kritik QC kontrolünü atlamamalısınız.
Ek 510k Eğitimi
510k kitabı, “510K'nızı 100 Günde Nasıl Hazırlarsınız?”2017 yılında tamamlandı, ancak kitap yalnızca projemizin bir parçası olarak mevcut. 510k kursu 58'den fazla web seminerinden oluşan seri. Lütfen ziyaret edin web semineri sayfası bireysel web seminerleri satın almak için.
- SEO Destekli İçerik ve Halkla İlişkiler Dağıtımı. Bugün Gücünüzü Artırın.
- PlatoData.Network Dikey Üretken Yapay Zeka. Kendine güç ver. Buradan Erişin.
- PlatoAiStream. Web3 Zekası. Bilgi Genişletildi. Buradan Erişin.
- PlatoESG. karbon, temiz teknoloji, Enerji, Çevre, Güneş, Atık Yönetimi. Buradan Erişin.
- PlatoSağlık. Biyoteknoloji ve Klinik Araştırmalar Zekası. Buradan Erişin.
- Kaynak: https://medicaldeviceacademy.com/estar-project-management/



