AI in Drug Discovery in een oogopslag
De aanhoudende opkomst van artificiële intelligentie (AI) heeft aanzienlijke gevolgen voor verschillende industrieën, waarbij de farmaceutische en biotechsector geen uitzondering vormen. Het is niet verwonderlijk dat zowel grote als kleine farmaceutische organisaties in toenemende mate gebruikmaken van AI-platforms voor het ontdekken van geneesmiddelen om onderzoeks- en ontwikkelingsprocessen te stroomlijnen, tijdlijnen en kosten voor ontdekking te verkorten en de algehele efficiëntie te verbeteren.
Toonaangevende farmaceutische bedrijven zoals J&J, GSK, AstraZeneca, Novartis, Pfizer, Sanofi en Eli Lilly hebben substantiële investeringen gedaan in AI voor het ontdekken van geneesmiddelen. Deze investeringen omvatten aandeleninvesteringen, overnames of partnerschappen met op AI gerichte bedrijven, het ontwikkelen van interne capaciteiten of een combinatie van deze strategieën.
Tegelijkertijd is er een golf van nieuwe geneesmiddelenontdekkings- en biotechbedrijven die zijn opgericht als AI-centrische organisaties, vaak vanaf het begin. Deze bedrijven, die voornamelijk in het afgelopen decennium zijn opgericht, hebben al gespecialiseerde AI-gestuurde platformen voor het ontdekken van geneesmiddelen gebouwd en getest. Deze platforms bevatten vaak talloze modellen voor machine learning en beginnen nu aanzienlijke voordelen op te leveren in termen van snelle en kosteneffectieve mogelijkheden voor het ontdekken van doelen en het ontwerpen van geneesmiddelen. Als gevolg hiervan produceren ze in een versneld tempo preklinische en klinische kandidaat-geneesmiddelen. In de volgende secties zullen we een selectie van door AI ontwikkelde kandidaat-geneesmiddelen onderzoeken, waaronder kleine moleculen, biologische geneesmiddelen en andere modaliteiten, die al in klinische proeven zijn opgenomen of op het punt staan dat te doen.
Bovendien hebben bepaalde AI-bedrijven vooruitgang geboekt bij het modelleren van biologie met behulp van complexe multimodale gegevens op schalen die slechts twee decennia geleden ondenkbaar waren. Een andere groep bedrijven heeft AI-gestuurde platforms ontwikkeld om de operationele efficiëntie en het ontwerp van experimenten in klinische onderzoeken of real-world data-analyse, zoals geneesmiddelenbewaking, te verbeteren.
Grote technologiebedrijven, zoals Alphabet, Microsoft, Amazon, IBM en Tencent, beschikken over expertise op het gebied van AI en big data-technologieën en wagen zich ook aan de ontdekking van geneesmiddelen. Hun betrokkenheid omvat onder meer investeren, startups oprichten, samenwerken met life science-bedrijven, experimenteren en innoveren.
Ten slotte is er aanzienlijke vooruitgang geboekt in andere geavanceerde technologieën, zoals kwantumcomputing, Cryo-EM en DNA-gecodeerde bibliotheken. Deze technologieën convergeren met de AI-trend, wat niet alleen resulteert in nieuwe soorten tools, producten en diensten, maar ook in een golf van innovatieve start-ups en zelfs nieuwe bedrijfsmodellen.
Wat is AI en hoe wordt het toegepast bij het ontdekken van geneesmiddelen?
Kunstmatige intelligentie is een relatief oud concept, geformaliseerd op een beroemde Dartmouth College-conferentie in 1956. De AI-technologieën bij het ontdekken van geneesmiddelen zijn voortgekomen uit eerdere concepten en benaderingen van machine learning (ML), cheminformatica en bioinformatica. De toepassing van machine learning bij het ontwikkelen van kwantitatieve structuur-activiteitsrelatie (QSAR)-modellen en expertsystemen voor voorspelling van toxiciteit heeft bijvoorbeeld een lange geschiedenis.
De snelle (in sommige gevallen "exponentiële") opkomst van big data, geavanceerde analyses, het minimaliseren van de rekenkosten, GPU-versnelling, cloud computing, de ontwikkeling van algoritmen (bijvoorbeeld diepe neurale netwerken en grote taalmodellen) en de "democratisering" van AI-technologie - dit alles leidde tot een synergetische "boom" in het commercialiseren en industrialiseren van kunstmatige intelligentie, met name in de farmaceutische en biotech-industrie.
In deze whitepaper gebruiken we de verzamelterm 'kunstmatige intelligentie' om te verwijzen naar geavanceerde computer- en modelleringssystemen die automatisch inzichten kunnen leren en praktische suggesties kunnen afleiden uit 'big data', gestructureerde en ongestructureerde data, ook multimodale data.
Hoewel er geen limiet is aan een bepaalde familie van algoritmen die we 'kunstmatige intelligentie' noemen, impliceren we in de meeste gevallen verschillende smaken van op machine learning gebaseerde systemen (voornamelijk diepe neurale netwerken) en grote natuurlijke taalverwerking (NLP) modellen. Moderne AI-systemen kunnen leren zonder expliciete instructies (in tegenstelling tot traditionele cheminformatica-software binnen "als-dan"-logica), ze kunnen de nauwkeurigheid verbeteren na nieuwe leercycli en wanneer er meer gegevens aan het systeem worden ingevoerd, en - met name - ze kunnen verwerken van hoogdimensionale multimodale gegevens van enorme omvang. Al deze attributen onderscheiden moderne kunstmatige-intelligentiesystemen aanzienlijk van verouderde softwarepakketten voor chemi-informatica en bio-informatica. Dergelijke vaardigheden staan centraal in wat de aanhoudende opwinding over AI (en hype) drijft.
Terwijl sommige componenten van wat we "kunstmatige intelligentie" noemen - bijvoorbeeld machine learning-tools en taalmodellen - door vrijwel elke farmaceutische organisatie en academisch laboratorium worden gebruikt, zijn sommige bedrijven erin geslaagd geavanceerde computationele en modelleringspijplijnen te bouwen, "AI-platforms" te onderzoeken, waaronder geautomatiseerde workflows in tientallen en zelfs honderden verschillende modellen en systemen (deep learning, taalmodellen) en honderden verschillende openbare en eigen gegevensbronnen.
De hoge mate van verfijning en automatisering van sommige AI-platforms leidde tot hun "commoditisering" tot het punt dat ze handelsnamen als handelsmerk hebben. Tegelijkertijd worden sommige ervan als software-as-a-service aangeboden aan andere bedrijven. Voorbeelden zijn mRNA DESIGN STUDIO™ van Moderna, Centaur Chemist® van Exscientia, Guardian Angel™ van AI Therapeutics, ConVERGE™ van Verge Genomics, Taxonomy3® van C4X Discovery en vele anderen.
Hieronder ziet u een voorbeeld van Pharma.AI door Insilico Medicine, een modulair systeem voor end-to-end geneesmiddelenontdekking dat honderden verschillende subsystemen en machine learning-modellen omvat - allemaal bestuurd door weer andere algoritmen van hogere modelleringsabstractie (via een principe van “ensemble-leren”).
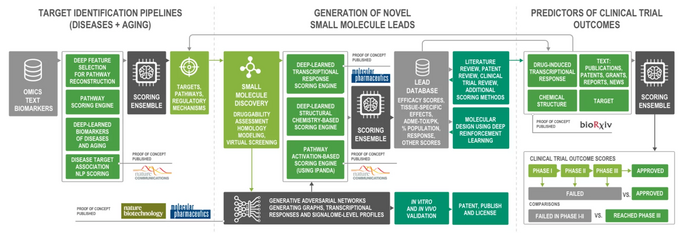
Een schema van Pharma.AI end-to-end platform. Afbeelding tegoed: https://insilico.com
Kunstmatige intelligentie wordt veel gebruikt in bijna elk aspect van farmaceutisch onderzoek, van datamining, biologiemodellering en het ontdekken van doelen tot identificatie van leads en preklinisch en klinisch onderzoek. Het wordt ook gebruikt voor syntheseplanning, intelligent zoeken naar reagentia en verbruiksartikelen voor onderzoek, en hulptaken zoals slimme laboratoriumnotitieboekjes en virtuele assistenten.

Bron: https://www.biopharmatrend.com/m/companies/ai/
Het Life Science-ecosysteem van AI-gebruikers omvat de volgende belangrijke categorieën spelers:
|
400+ AI-gedreven bedrijven (startups/scale-ups), met een breed scala aan AI-gestuurde platforms en diensten — van het klassieke Software-as-a-Service-model tot op maat gemaakte datawetenschapsdiensten, medicijnontdekking ("Drug candidate-as as service") en ondersteuning/beheer van klinische proeven bronnen. |
|
Domeinspecifieke softwareleveranciers (bijv. KNIME, ChemAxon, Dotmatics, MolSoft en anderen) richten zich voornamelijk op chemi-informatica/bio-informatica-software, maar bieden ook door machine learning aangestuurde tools. |
|
Farmaceutische en biotechbedrijven van het hoogste niveau die interne AI-expertise ontwikkelen als onderdeel van hun R&D-strategie. Dergelijke spelers werken vaak samen met externe AI-leveranciers en AI-gestuurde biotech-startups om proefprogramma's te onderzoeken op het gebied van medicijnontdekking/basisbiologie/klinische proefanalyse. |
|
Toptechnologiebedrijven zoals Google, Amazon en Tencent betreden de farmaceutische ruimte en maken gebruik van geavanceerde AI-technologieën en big data-infrastructuren. |
|
Contractonderzoeksorganisaties (CRO's) die expertise op het gebied van AI ontwikkelen om hun waardeaanbod voor farmaceutische/biotechklanten te vergroten |
|
Academische laboratoria in de farma/biotech-ruimte, die AI-onderzoek uitvoeren en gespecialiseerde kaders en tools ontwikkelen die relevant zijn voor de industrie (meestal een bakermat voor toekomstige AI-startups/spin-outs) |
|
Niet-domeinspecifieke softwareleveranciers die AI-as-a-service-pakketten en -modellen ontwikkelen die geschikt zijn voor toepassing in farmaceutisch onderzoek (bijv. "out of the box AI") |
|
Open-source machine learning-tools en -frameworks, die op grote schaal worden gebruikt door life science-professionals in hun onderzoeksprojecten |
Investeringslandschap voor AI-geneesmiddelenontdekking
Na 2021, het abnormaal succesvolle jaar voor de biotech-industrie in termen van het aantal durfkapitaaldeals, het recordaantal beursintroducties, een overvloed aan succesvolle exits en een over het algemeen zeer positief klimaat op de aandelenmarkt, liet het jaar 2022 zien aanzienlijke afkoeling van de financiële activiteit en ronduit slechte prestaties van de aandelenmarkt.
Kunstmatige intelligentie in de sector voor het ontdekken van geneesmiddelen toonde echter een zekere veerkracht, althans in het landschap van private equity-transacties, waarbij verschillende bedrijven honderden miljoenen aan durfkapitaal ophaalden. Enkele voorbeelden zijn het in Beijing gevestigde MegaRobo Technologies ($ 300 miljoen Series C), het in Massachusetts gevestigde ConcertAI ($ 150 miljoen Series C) en Celsius Therapeutics ($ 83 miljoen Series A), het in Hong Kong gevestigde Insilico Medicine ($ 95 miljoen Series D), Californië- op basis van BigHat Biosciences ($ 75 miljoen Series B) en DeepCell ($ 73 miljoen Series B), en verschillende anderen - lees "Grote VC-rondes voor AI-bedrijven in Drug Discovery en Biotech in 2022'.
Een landschap van fusies en overnames (M&A) werd gekenmerkt door een recente opmerkelijke deal met een biotechgigant Ginkgo Bioworks neemt Zymergen over in een transactie ter waarde van Zymergen op $ 300 miljoen. De overname brengt Zymergen's machine learning en data science-mogelijkheden samen met Ginkgo's platform voor synthetische biologie.
Belangrijkste observaties en trends in de branche
De komst van AI- en datatechnologieën, evenals nieuwe computertools en infrastructurele oplossingen (databases, cloudservices, enz.), herdefiniëren allemaal de manier waarop de farmaceutische industrie werkt - op onderzoeks-, klinische en zakelijke niveaus. Laten we hieronder enkele van de trends en observaties in de AI voor de ruimte voor het ontdekken van geneesmiddelen en illustratieve ontwikkelingen in de sector in 2022 bekijken.
AI-ondersteunde biologiemodellering en doeldetectie
Bij onderzoek naar geneesmiddelenontdekking is het identificeren van nieuwe medicijndoelen van cruciaal belang voor het ontwikkelen van nieuwe eersteklas therapeutische medicijnen - potentiële "blockbusters". Inspanningen voor het ontdekken van geneesmiddelen gedurende de afgelopen decennia concentreerden zich traditioneel rond het richten op specifieke eiwitten met geschikte "pockets" om te worden beïnvloed door een ligandmolecuul (vaak een klein molecuul). Maar van alle menselijke eiwitten (ook wel "proteoom" genoemd) werd een klein aantal eiwitten als doelwit onderzocht. Er zijn momenteel 20,360 menselijke eiwitten in Swiss-Prot, waarvan bekend is dat ongeveer 4,600 betrokken zijn bij ziektemechanismen volgens de OMIM-database, wat neerkomt op ongeveer 22% van de menselijke eiwitten met een rol bij ziekte. Deze eiwitten zijn het voor de hand liggende gebied van het menselijke proteoom dat waarschijnlijk levensvatbare doelwitten voor geneesmiddelen bevat. Echter, op 2017, werden slechts ongeveer 890 menselijke en van ziekteverwekkers afgeleide biomoleculen (meestal eiwitten) daadwerkelijk gebruikt door de bestaande door de FDA goedgekeurde medicijnen. Deze biomoleculen omvatten 667 van het menselijk genoom afgeleide eiwitten die het doelwit zijn van geneesmiddelen voor ziekten bij de mens. Tegenwoordig is het niet veel anders, dus er is nog veel ruimte voor het identificeren van nieuwe doelen in deze pool. Nieuwe computationele benaderingen op basis van kunstmatige-intelligentietechnologieën maken het mogelijk om nieuwe, voor medicijnen geschikte eiwitpockets op schaal te identificeren, waardoor soms proteoom-brede virtuele schermen mogelijk zijn.
Maar wat nog spannender is, is dat geavanceerde modelleringstools helpen bij het identificeren en moduleren van nieuwe soorten doelwitten, zoals eiwit-eiwitinteracties, doelwitten met grote contactgebieden, eiwit-nucleïnezuurinteracties en doelwitten van de volgende generatie, zoals het exploiteren van het eiwit van de cel. degradatie machines.
Veel AI-gestuurde bedrijven richten zich op het modelleren van biologie, het ontdekken en valideren van nieuwe doelen en het aanbieden van "disease model-as-a-service" of "target-discovery-as-a-service" aan andere organisaties. De vraag naar dit soort contractonderzoeksdiensten neemt toe, wat tot uiting komt in het groeiende aantal samenwerkingsverbanden op het gebied van target discovery.
In september 2022 kondigde een in Israël gevestigd bedrijf voor biologiemodellering, CytoReason, bijvoorbeeld een uitgebreide samenwerking van $ 110 miljoen met Pfizer aan. De twee bedrijven begonnen samen te werken in 2019 toen Pfizer de biologische modellen van CytoReason begon te gebruiken voor onderzoek gericht op de ontwikkeling van nieuwe geneesmiddelen voor immuungemedieerde ziekten en kankerimmunotherapieën.
In mei 2022 kondigde AstraZeneca aan dat het een tweede doelwit voor longfibrose had verzameld uit zijn samenwerking met BenevolentAI, een in het VK gevestigde leider op het gebied van door AI aangestuurde medicijnontdekking. De mijlpaal markeerde een derde nieuw doelwit dat door BenevolentAI voor AstraZeneca werd ontdekt sinds de samenwerking in 2019 begon. Slechts enkele maanden later, in oktober 2022, slaagde BenevolentAI erin om twee extra door AI gegenereerde doelen te leveren voor AstraZeneca's R&D-portfolio, gericht op chronische nierziekte en idiopathische longfibrose.
In november 2022 tekende het in Hong Kong gevestigde Insilico Medicine een deal ter waarde van mogelijk $ 1.2 miljard met Sanofi voor het ontdekken van maximaal zes nieuwe doelen die gebruikmaken van het "Pharma.AI" -platform van Insilico Medicine.
Hoewel geavanceerde algoritmen zoals diepe neurale netwerken grote hoeveelheden gegevens nodig hebben om de biologie correct te modelleren, zijn er doelen met een kleine hoeveelheid gegevens beschikbaar. Een in Canada gevestigde Cyclica ontwikkelde een AI-gestuurd platform voor polyfarmacologie en proteoombrede screening, in staat om te werken met "low-data" -doelen. In november 2022 ontving Cyclica een subsidie van $ 1.8 miljoen van de Bill & Melinda Gates Foundation om haar op AI gebaseerde platform voor het ontdekken van geneesmiddelen toe te passen om nieuwe niet-hormonale contracten te ontdekken, gebruikmakend van meerdere biologische doelen met weinig gegevens.
Volgens de BiopharmaTrend-rapport, zijn er minstens 182 andere AI-bedrijven in de target discovery-ruimte, waaronder toonaangevende, goed gefinancierde bedrijven met geavanceerde R&D-platforms, zoals Insitro, Relay Therapeutics, Valo Health en anderen.
Nieuwe "AI-native" startups duiken voortdurend op in de ruimte voor biologiemodellering. Bijvoorbeeld CardiaTec Biosciences, WhiteLab Genomics, Degron Therapeutics om er maar een paar te noemen.
VERWANT: 11 AI-aangedreven Drug Discovery-startups opgericht in 2021
Al met al helpen geavanceerde modelleringsmethoden op basis van kunstmatige intelligentie om de definitie van biologische doelwitten te herdefiniëren, terwijl we proberen de respons van geneesmiddelen te koppelen aan genetische variatie, de gestratificeerde klinische werkzaamheid en veiligheid begrijpen, de verschillen tussen geneesmiddelen in dezelfde therapeutische klasse rationaliseren en voorspellen medicijngebruik in subgroepen van patiënten.
Structurele biologie kraken met AI
Een van de meest besproken AI-gerelateerde onderwerpen in de Life Sciences-gemeenschap dit jaar was het recente succes van Alphabet's Britse dochteronderneming DeepMind, die veel aandacht kreeg voor het succes ervan bij het oplossen van het probleem van het vouwen van eiwitten, een biologisch probleem van een halve eeuw oud.
In juli 2022, DeepMind's deep learning-software AlphaFold voorspeld en publiekelijk gedeeld eiwitstructuren van meer dan 200 miljoen eiwitten, nadat het het verbazingwekkende vermogen van zijn AI-systeem heeft aangetoond om 3D-structuren nauwkeurig te voorspellen, gewoon op basis van zijn 1D-aminozuursequentie. Hoewel sommigen beweren dat deze ontdekking (nog) niet zo'n transformerende rol speelt bij de ontdekking van geneesmiddelen als men zou denken, en dat AlphaFold presteerde niet veel beter dan toeval bij het voorspellen van interacties tussen bacterieel eiwit en antibacteriële verbinding, is de ontdekking zeker paradigmaveranderend voor zowel structurele biologie als het illustreren van het potentieel van AI in fundamenteel biologisch onderzoek.
In november 2022 werd het baanbrekende succes van DeepMind bij het modelleren van het proteoom geëvenaard door onderzoekers van Meta (voorheen Facebook, met hoofdkantoor in Menlo Park, Californië). Het gebruikte AI om de structuren te voorspellen van zo'n 600 miljoen eiwitten van bacteriën, virussen en andere micro-organismen die nog niet zijn gekarakteriseerd.
De wetenschappers van Meta gebruikten een geheel andere AI-aanpak — met behulp van een 'groot taalmodel', een type AI dat tekst kan voorspellen op basis van slechts enkele letters of woorden. Natuurlijke taalmodellen (NLP's) worden meestal getraind op grote hoeveelheden tekst. 1D-eiwitsequenties zijn echter in wezen letterreeksen, dus NLP's kunnen op dergelijke problemen worden toegepast, net zoals bij het werken met menselijke talen.
Interessant is dat dergelijke grote technologische sprongen in het vouwen van eiwitten nuttiger kunnen blijken te zijn voor de novo eiwitontwerp, dan simpelweg het modelleren van structuren van bestaande eiwitten voor het ontdekken van geneesmiddelen. De tijd zal leren waar de impact het grootst zal zijn, maar bovenstaande successen van DeepMind en Meta zijn niet de enige opwindende ontwikkeling voor structuurbiologen in 2022.
Onlangs hebben de snelle vorderingen in cryo-EM, in combinatie met AI-technologieën, geleid tot een nieuwe golf van biotech-startups zoals Gandeeva Therapeutics, Septerna en MOMA Therapeutics. Het cryo-EM-veld warmt op met biotech-startups die de aandacht trekken van een breed scala aan investeerders, van de kleinere venture-organisaties tot de eigenaar van TikTok en internettechnologiegigant ByteDance, die investeert in Shuimu BioSciences. De interesse wordt niet alleen gedreven door de revolutionaire Nobelprijswinnende technologie, maar ook door de actieve werving van AI in het proces. De recente publicatie "Een door AI ondersteunde cryo-EM-pijplijn voor structurele studies van cellulaire extracten" benadrukte de niet-vervangbare rol van AI in complexe cryo-EM-pijplijnen, inclusief AI-gestuurde atoommodelvoorspelling om snel en gelijktijdig de structuur van meerdere leden van de eiwitgemeenschap de novo te onderzoeken. Machine learning helpt niet alleen om de cryo-EM-pijplijn te versnellen en te optimaliseren, maar ook om valkuilen voor gebruikersvooroordelen te vermijden.
Gandeeva Therapeutics, opgericht in 2021, haalde begin dit jaar $ 40 miljoen op om nieuwe therapieën te ontwikkelen op basis van nauwkeurige beeldvorming van eiwit-geneesmiddelinteracties. Hun Target-Selection Engine kan samen met de Cryo-EM Engine helpen om "weg te blijven van doodlopende wegen", zoals het bedrijf verklaarde. Tegelijkertijd, gelanceerd in 2020, haalde cryo-EM biotech MOMA Therapeutics maar liefst $ 236 miljoen op in slechts twee jaar tijd, met een ambitieus doel om nieuwe precisiegeneesmiddelen voor kanker vrij te geven aan klinieken. MOMA richt zich op een unieke klasse van biologische doelen: 'moleculaire machines'.
Kleine moleculen ontwikkelen met behulp van AI
Na het modelleren van ziekten en het ontdekken van doelwitten, is het ontwerpen van chemische of biologische moleculen de tweede meest voorkomende use case voor het toepassen van kunstmatige intelligentie bij het ontdekken van geneesmiddelen. Meer dan 130 door kunstmatige intelligentie aangestuurde bedrijven van de 384 bedrijven in het BiopharmaTrend AI-rapport passen kunstmatige intelligentie toe voor het ontwerpen van kandidaat-geneesmiddelen, naast andere use cases.
Door AI aangestuurd medicijnontwerp valt hoofdzakelijk in drie hoofdcategorieën: de novo (bijv. generatief) medicijnontwerp, virtuele screening van bestaande databases en herbestemming van medicijnen.
Het nieuwe medicijnontwerp wordt meestal mogelijk gemaakt door deep learning-modellen, zoals generatieve vijandige neurale netwerken (GAN's). Enkele voorbeelden van generatieve AI-platforms zijn Chemistry42-software van Insilico Medicine, Makya van Iktos en De Novo Platform van Ro5. Andere spelers in deze categorie zijn Recursion Pharmaceuticals, Deep Cure, Standigm en anderen.
De toepassing van kunstmatige intelligentie maakte ultragrootschalige virtuele screening mogelijk, waarbij miljarden moleculen werden doorzocht om succesvolle hits te vinden. In augustus 2022 werkte Sanofi samen met Atomwise in een deal voor het ontwerpen van geneesmiddelen ter waarde van mogelijk $ 1.2 miljard. De deal, waarbij Sanofi vooraf 20 miljoen dollar betaalt, draait om het gebruik van het AtomNet-platform van het Amerikaanse bedrijf om onderzoek te doen naar kleine moleculen voor maximaal vijf door Sanofi geselecteerde medicijndoelen. Een op convolutioneel neuraal netwerk gebaseerd AtomNet blinkt uit in op structuur gebaseerd medicijnontwerp, waardoor "de snelle, door AI aangedreven doorzoeking van Atomwise's eigen bibliotheek van meer dan 3 biljoen synthetiseerbare verbindingen mogelijk wordt", aldus de aankondiging.
Eerder in 2019 werkte Atomwise samen met de in Oekraïne gevestigde chemische leider Enamine om 's werelds eerste en grootste virtuele scherm van 10 miljard verbindingen uit te voeren, gericht op het identificeren van hits voor pediatrische oncologie.
Tot slot gebruikt een aantal bedrijven herbestemmingsstrategieën voor het ontdekken van medicijnen op basis van AI. Bedrijven in deze categorie, waaronder Healx, BenevolentAI, BioXcel Therapeutics, maken grotendeels gebruik van modellen voor natuurlijke taalverwerking (NLP) en machine learning en werken via het analyseren van enorme hoeveelheden ongestructureerde tekstuele gegevens - onderzoeksartikelen en patenten, elektronische medische dossiers (EHR's), zoals evenals andere gegevenstypen - om "kennisgrafieken" te bouwen en te doorzoeken. Dergelijke door AI ondersteunde doorzoekbare ontologieën maken het mogelijk om nieuwe indicaties of patiëntenpopulaties te kiezen voor eerder bekende kandidaat-geneesmiddelen of zelfs goedgekeurde geneesmiddelen.
Zo richtte Lantern Pharma, een in de VS gevestigd biotechnologiebedrijf in de klinische fase, zich op het innoveren van het ontwikkelingsproces van geneesmiddelen tegen kanker door gebruik te maken van geavanceerde genomica, machine learning en kunstmatige intelligentie.
Het AI-platform van het bedrijf, RADR®️, bevat momenteel meer dan 25 miljard datapunten en maakt gebruik van big data-analyse en machine learning om snel biologisch relevante genomische handtekeningen te ontdekken die verband houden met de respons op geneesmiddelen, en vervolgens om relevante subgroepen van kankerpatiënten te identificeren die kunnen profiteren van de kandidaat-geneesmiddelen van Lantern. . RADR ®️ wordt ook gebruikt door Lantern en zijn medewerkers om nieuwe geneesmiddelen te ontwikkelen en te positioneren, evenals voor herbestemming van geneesmiddelen.
VERWANT: Onthulling van het succesverhaal van Lantern Pharma in AI-aangedreven precisie-oncologie
AI ontmoet DNA-gecodeerde bibliotheken
Een enigszins unieke benadering van het ontwerpen van geneesmiddelen bestaat uit het gebruik van DNA-gecodeerde bibliotheken (DEL's) als een bron van nieuwe moleculen om doorheen te zoeken. Aangezien DEL-technologie toegang biedt tot in wezen de grootste chemische ruimte die op de markt beschikbaar is, past deze big data-technologie perfect bij AI-gebaseerde tools.
een opmerkelijke transactie vond plaats in 2020, toen Insitro, een van de opmerkelijke spelers in de toepassing van machine learning voor het ontdekken van geneesmiddelen, opgericht door Daphne Koller, Haystack Sciences overnam. Het op machine learning gebaseerde platform van Haystack combineerde meerdere elementen van hun DEL-technologie, waaronder de mogelijkheid om brede, diverse collecties van kleine moleculen te synthetiseren, de mogelijkheid om iteratieve follow-up uit te voeren en een gepatenteerde semi-kwantitatieve screeningtechnologie genaamd nDexer™, die genereert datasets met een hogere resolutie.
Op zijn beurt werd ZebiAI in 2021 overgenomen door een andere opmerkelijke ontwikkelaar van een door kunstmatige intelligentie aangedreven platform voor het ontdekken van geneesmiddelen, een klinische biotech Relay Therapeutics, waar Relay vooraf $ 85 miljoen betaalde. Door deze overname kon Relay ZebiAI's op machine learning gebaseerde DEL-technologie integreren in hun platform voor eiwittargeting Dynamo.
VERWANT: Een marktoverzicht van DNA-gecodeerde bibliothekentechnologie bij het ontdekken van geneesmiddelen
In oktober 2021 nam X-Chem Glamorous AI over, een ontwikkelaar van een modulaire veelzijdige kunstmatige intelligentie-oplossing voor het ontdekken van geneesmiddelen RosalindAI, inclusief mogelijkheden voor data-engineering en parametrisatie, voorspellende analyse, high-performance computing en de-novo medicijnontwerp.
AI-gestuurd medicijnontwerp dat verder gaat dan kleine moleculen
Gezien het feit dat moderne hulpmiddelen voor kunstmatige intelligentie die worden gebruikt voor het ontdekken van geneesmiddelen diepe historische wortels hebben in cheminformatica en vroege op machine learning gebaseerde QSAR-modellen van de afgelopen eeuw, is het niet verwonderlijk dat de overgrote meerderheid van AI-startups bij het ontdekken van geneesmiddelen gericht is op kleine moleculen. .
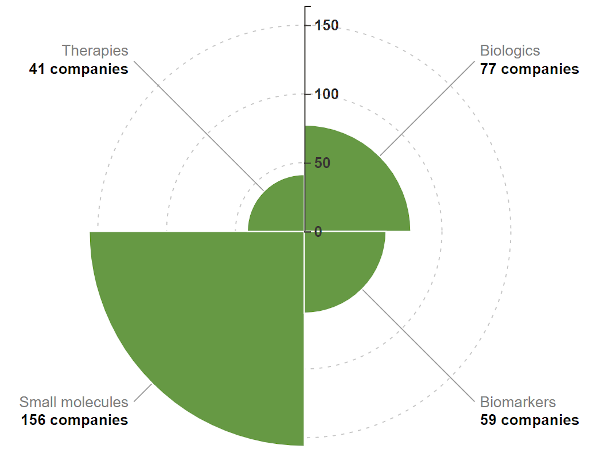
Verdeling van AI-geneesmiddelenontdekkingsbedrijven per productcategorie. Bron: BiopharmaTrend AI-rapport.
Biomoleculegeneesmiddelen (ook wel "biologische geneesmiddelen" genoemd) en nieuwe chemische modaliteiten komen echter steeds vaker voor in de farmaceutische ruimte, en dat geldt ook voor de nieuwe biotechbedrijven die op AI gebaseerde methoden toepassen om die te ontdekken. Nadat wetenschappers in 2003 het menselijk genoom hadden gekraakt, evolueerde de ruimte voor medicijnbaarheid en ontwikkelbaarheid snel. In de afgelopen eeuw diende Lipinski's regel van vijf (Ro5) als een "leidraad" voor het ontwerp van medicijnachtige moleculen voor orale toediening in de "traditionele" medicijnbare doelruimte.
Daarentegen zorgen nieuwe typen doelwitten, zoals eiwit-eiwitinteracties, doelwitten met grote contactgebieden, eiwit-nucleïnezuurinteracties en doelwitten van de volgende generatie, zoals het exploiteren van de eiwitafbraakmachinerie van cellen, voor de komst van een verscheidenheid aan opkomende moleculaire modaliteiten, namelijk buiten de Ro5 (bRo5) kleine moleculen (zoals eiwit-eiwit interactie modulatoren, op eiwit gerichte chimaera's (PROTAC's), monoklonale antilichamen (mAbs), peptiden en peptidomimetica, en op nucleïnezuur gebaseerde modaliteiten (RNA en DNA- gebaseerd), zijn een belangrijk aandachtspunt geworden bij het ontdekken van geneesmiddelen.
Er is bijvoorbeeld een groeiend aantal bedrijven dat AI-methoden toepast om nieuwe monoklonale antilichamen te ontdekken – de commercieel meest succesvolle biologische modaliteit tot nu toe. Met name in april 2022 kondigde het in Israël gevestigde Biolojic Design hun allereerste computationeel ontworpen antilichaam aan ging de klinische proef in. Het bedrijf maakt gebruik van een op structuur gebaseerde ontwerpstrategie. Het AI-model is getraind op miljoenen antilichaam-antigeenparen om een template-antilichaam te identificeren tegen het beoogde doelwit van bestaande menselijke antilichamen. Een extra machine learning-model wordt gebruikt om mutaties te voorspellen en de optimalisatie van de sjabloon te begeleiden om de eigenschappen ervan te verbeteren.
In november 2022 kondigde het in Canada gevestigde AbCellera Biologics aan dat Regeneron ervoor had gekozen zijn recht uit te oefenen om de eerste van AbCellera's therapeutische antilichaamkandidaten gericht op een niet bekendgemaakte G-proteïne-gekoppelde receptor (GPCR) door te voeren naar verdere preklinische ontwikkeling. De samenwerking, die in maart 2020 van start ging en vier door Regeneron geselecteerde ontdekkingsprogramma's mogelijk maakt, maakt gebruik van AbCellera's op AI gebaseerde antilichaamdetectie-engine en Regenerons VelocImmune®-muizen om nieuwe therapeutische antilichamen te identificeren.
Twee dozijn andere bedrijven die antilichamen ontdekken, gebruiken AI, waaronder het in de VS gevestigde AbSci, BigHat Biosciences, Totient, Nabla Bio en Generate Biomedicine; Het in Canada gevestigde Deep Biologics; NeoX uit China; In de EU gevestigde Deep CDR, Natural Antibody en MabSilico, enz.
Het in de VS gevestigde bedrijf met de pakkende naam Creyon Bio past een technische benadering toe bij het creëren van nieuwe op oligonucleotiden gebaseerde geneesmiddelen (OBM's). Het bedrijf werd opgericht in 2019 en haalde in maart 40 $ 2022 miljoen aan financiering op. Envisagenics, opgericht in 2014 als een spin-out van Cold Spring Harbor Laboratory, is een in New York gevestigd bedrijf dat zich richt op het ontdekken van RNA-therapieën. Volgens hun verklaarde missie streven ze ernaar de complexiteit van biomedische gegevens te verminderen met behulp van AI/ML-technologieën. Onlangs, in augustus 2022, ontvingen ze een beurs van het National Cancer Institute, wat resulteerde in een totale ingezamelde financiering van $ 27.1 miljoen.
De AI-gestuurde technologie van Envisagenics, SpliceCore, is een cloudgebaseerd platform dat experimenteel is gevalideerd om medicijndoelen en biomarkers te voorspellen door middel van splicing-ontdekking van RNA-sequencinggegevens. Volgens het bedrijf zorgt het voor een hogere precisie en snelheid in vergelijking met traditionele methodes.
De AI-gestuurde strategie van Innophore om nieuwe therapeutische enzymen te ontwerpen, wordt gerealiseerd door hun gepatenteerde Catalophore™-technologie te koppelen aan de modernste conventionele bio-informatica-benaderingen en kunstmatige intelligentie. Innophore kan structurele en sequentiedatabases ontginnen met behulp van driedimensionale (3D) zoeksjablonen die "cataloforen" worden genoemd (dwz drager van de katalytische functie) gedefinieerd door puntenwolken van fysisch-chemische kenmerken. Door deze techniek geïdentificeerde nieuwe enzymen delen niet noodzakelijkerwijs een gemeenschappelijke structuur of sequentiebasis met hun gebruikte tegenhangers. Daarom hebben ze mogelijk veranderde eiwiteigenschappen, zoals thermostabiliteit, robuustheid, substraatspectrum, selectiviteit en specificiteit.
Naast het ontwerpen van nieuwe enzymen, kan de technologie van Innophore mogelijk een game changer zijn voor epidemiologische toepassingen, waarbij potentieel gevaarlijke mutaties in virussen worden beschermd. In 2021 startte Innophore het virus.watch-project in samenwerking met het AWS Diagnostic Development Initiative. Het doel van dit project was de implementatie van een monitoring- en evaluatiesysteem voor opkomende geneesmiddelen- en ziekterelevante varianten van het coronavirus (SARS-CoV-2). Het eerste gezamenlijke document, gepubliceerde in Nature van augustus 2022, beschrijft bio-informatica-analyse van SARS-CoV-2-varianten die een hogere bindingsaffiniteit voor de hACE2-receptor voor Omicron B.1.1.529 spike RBD aan het licht brengen in vergelijking met een wildtype-referentie.

Het volgen van het evoluerende virus in de loop van de tijd met behulp van Innophore-technologie en AWS toont een hoge mate van mutaties die ontstaan bij de Omicron-variant. Bollen verbeelden alfa-C-atomen van het overeenkomstige aminozuurresidu. Zowel kleur als grootte correleren met het aantal mutaties op elke positie.
Het in Denemarken gevestigde Evaxion Biotech, opgericht in 2008, is een AI-gedreven bedrijf dat zich toelegt op het ontwikkelen van vaccins tegen kanker en infectieziekten. Ze bezitten een AI-Immunology-platform in de klinische fase, waarbij AI-technologie wordt gecombineerd met hun technische expertise om voorspellende modellen te genereren, waarmee unieke immunotherapieën voor patiënten kunnen worden geïdentificeerd. Evaxion Biotech trok in totaal $ 57 miljoen aan en betrad in juni 2022 de post-IPO equity-financieringsronde ter waarde van $ 40 miljoen, geleid door een enkele investeerder Lincoln Park Capital Fund.
VERWANT: 10 bedrijven die AI toepassen voor het ontwerpen van biologische geneesmiddelen
Sommige AI-bedrijven van de 'club voor chemische modaliteiten', zoals Exscientia, breiden nu uit naar het ontdekken van biologische producten. In november 2022 kondigde het bedrijf aan dat zijn AI-platform het ontwerp van menselijke antilichamen zou omvatten. Exscientia richt ook een geautomatiseerd biologisch laboratorium op in Oxford om intern nieuwe antilichamen te genereren en te profileren.
Een groeiende trend is om het eiwitafbraaksysteem van menselijke cellen te benutten om kwaadaardige eiwitten te verwijderen en ziekten te genezen. Een modaliteit hier die steeds populairder wordt, is proteolyse gericht op chimera (PROTAC) die in 2001 werd geïntroduceerd en bestaat uit twee liganden die zijn verbonden door een flexibele linker. De primaire chemische architectuur van moderne PROTAC's is hetzelfde: één ligand richt zich op het E3-enzym, een component die verouderde eiwitten naar het proteasoom stuurt, en een andere ligand richt zich op een eiwit van interesse (POI) dat moet worden afgebroken. Een PROTAC bindt E3 en POI, waardoor ze dichter bij elkaar komen om een geïnduceerd nabijheidscomplex te vormen. In sommige gevallen, wanneer de eiwitten op de juiste manier zijn uitgelijnd, wordt de POI alomtegenwoordig, wat het markeert voor afbraak door het proteasoom.
Een andere brede benadering van eiwitafbraak omvat zogenaamde "moleculaire lijmen", een actief groeiend onderzoeksgebied. In tegenstelling tot PROTAC's, die relatief grote bifunctionele kleine moleculen zijn met twee actieve sites en een linker, zijn moleculaire lijmen kleinere en meer medicijnachtige moleculen. Deze laatste binden zich aan een geaggregeerde eiwitpocket die het resultaat is van twee afzonderlijke eiwitten die in elkaars buurt komen vanwege het effect van het moleculaire lijmmolecuul.
Er is een golf van bedrijven binnen de ruimte voor eiwitafbraak (en, meer in het algemeen - modulatie), waaronder Arvinas, Nurix Therapeutica, Kymera Therapeutica, C4 Therapeutics, Roivant Discovery, Cedilla Therapeutics en Lycia Therapeutics, om er maar een paar te noemen.
Sommige bedrijven passen geavanceerde AI-algoritmen toe om nabijheidsinducerende verbindingen te ontwerpen. Het in Oostenrijk en de VS gevestigde Celeris Therapeutics heeft bijvoorbeeld het Celeris One-platform gebouwd, inclusief drie werkzonesystemen: Xanthos, Hephaistos en Hades. De systemen bevatten graafneurale netwerken om interacties en generatieve modellen te voorspellen om nieuwe chemische materie te creëren, zoals linker- en multi-objectieve optimalisatie om moleculaire eigenschappen, moleculaire dynamica en berekeningen met vrije energie te verbeteren. De workflow maakt ook gebruik van geometrisch deep learning en door machine learning aangestuurde retrosynthesemogelijkheden. Celeris Therapeutics beheert een geautomatiseerd laboratorium om biologische gegevens te genereren en aangepaste chemische synthese uit te voeren.

De dry lab-workflow van het AI-gestuurde platform Xanthos van Celeris Therapeutics.
We hebben onlangs een breed overzicht van de markt voor eiwitafbraak in een post gepubliceerd Eiwitafbrekers veroveren de industrie stormenderhand, inclusief verschillende casestudy's met een technisch overzicht van de betrokken rekenplatforms.
De eerste golf van door AI ontwikkelde kandidaat-geneesmiddelen gaat klinisch
Hoewel het waarschijnlijk vroeg is om te zeggen dat de acceptatie van AI in de farmaceutische industrie een revolutie teweeg heeft gebracht in de ontdekking van geneesmiddelen, zijn verschillende "AI-native" bedrijven erin geslaagd om opmerkelijke efficiëntie te behalen bij het snel bouwen van hun therapeutische pijplijnen. Wat is een gemeenschappelijk kenmerk van dergelijke bedrijven? Elk bouwde een gespecialiseerd, sterk geïntegreerd AI-platform, inclusief veel modellen en gegevensbronnen. Sommige platformen zijn ook beschikbaar als software-as-a-service voor externe R&D-partners, zoals Chemistry42.
Een van de meest levendige voorbeelden van het profiteren van een "digital-first"-strategie die de industrie heeft gezien, is Moderna Therapeutics, dat er niet alleen in slaagde om geavanceerde AI-analyses in zijn onderzoek op te nemen, maar ook elk aspect van zijn R&D-workflow digitaliseerde en integreerde, inclusief productie en distributie. Toen de COVID-19-pandemie begin 2020 de wereld toesloeg, was Moderna een van de eerste bedrijven die binnen slechts 2 dagen (!) een efficiënt mRNA-gebaseerd vaccin kon bedenken en binnen een jaar op de markt kon brengen .
Een golf van successen op het gebied van therapeutische ontdekkingen, mogelijk gemaakt door AI, toont het vermogen van AI-native bedrijven om sneller met kandidaat-geneesmiddelen te komen dan gewoonlijk het geval was voor vergelijkbare programma's.

Bekijk "De routekaart van kandidaat-geneesmiddelen ontworpen door AI,"
AbCellera's monoklonale antilichaam LY-CoV555 werd binnen drie maanden ontwikkeld en kreeg toestemming voor gebruik in noodgevallen door de FDA.
De Knowledge Graph van BenevolentAI hielp het bedrijf om Baricitinib binnen enkele dagen te identificeren als een efficiënt antiviraal middel tegen COVID-19 (nu goedgekeurd voor gebruik door de FDA). Een ander klein molecuul BEN-8744, een nieuwe remmer voor de behandeling van colitis ulcerosa en dermatitis, werd in minder dan 24 maanden naar laat preklinisch onderzoek gebracht.
Exscientia's remmer van kleine moleculen EXS-21546 markeerde het eerste door AI ontworpen molecuul voor immuno-oncologie dat deelnam aan klinische proeven bij mensen (nu in fase I) en werd ontdekt in slechts acht maanden. Het bedrijf heeft verschillende andere moleculen in klinische proeven.
De kleinmoleculaire remmer ISM001-055 van Insilico Medicine, voor de behandeling van idiopathische longfibrose, was de novo ontworpen en binnen 18 maanden ontwikkeld tot late preklinische studies (nu in fase I).
Het in New York gevestigde Schrödinger ontwikkelde een klein molecuul SGR-1505 om B-cellymfoom binnen tien maanden te behandelen en is nu bezig met de aanvraag bij de IND.
Het in Salt Lake City gevestigde Recursion Pharmaceuticals ontwikkelde binnen 18 maanden een kandidaat-geneesmiddel voor een niet-gespecificeerde zeldzame ziekte. Het bedrijf heeft een groot en divers portfolio van preklinische en klinische kandidaat-geneesmiddelen, ontworpen met behulp van zijn digitale biologieplatform.
Het in Toronto gevestigde Deep Genomics gebruikte zijn AI Workbench-platform om een nieuw genetisch doelwit en een overeenkomstig oligonucleotide-geneesmiddel DG12P1 te ontwikkelen voor de behandeling van een zeldzame erfelijke ziekte van Wilson.
Om de toonaangevende door AI ontwikkelde klinische kandidaat-geneesmiddelen bij te houden, hebben we een "De routekaart van kandidaat-geneesmiddelen ontworpen door AI," die regelmatig zal worden bijgewerkt.
Opgemerkt moet worden dat de aanhoudende media-aandacht voor de AI voor het ontdekken van geneesmiddelen door een lens van voorzichtigheid moet worden beschouwd. Zo kreeg het plan van BenevolentAI om zijn kandidaat-geneesmiddel voor atopische dermatitis, BEN-2293, een licentie te geven, een tegenslag omdat de AI-geactiveerde pan-Trk-remmer er niet in slaagde de eczeemsymptomen of jeuk te verbeteren in een fase 2a-onderzoek. Het bedrijf had eerder tropomyosinereceptorkinasen (Trk) geïdentificeerd als bemiddelaars van jeuk en ontsteking bij atopische dermatitis, wat leidde tot de ontwikkeling van Trk-remmers. Hoewel BEN-2293 een trend liet zien in de richting van een klinisch relevant effect in een fase 1b-studie, onthulde de fase 2a-studie dat het niet beter was dan een placebo bij het verbeteren van de ernst van eczeem of jeuk. De uitkomst roept vragen op over het AI-platform dat de aanpak heeft voorgesteld. Ondanks de tegenslag heeft BenevolentAI het kandidaat-geneesmiddel niet opgegeven, daarbij verwijzend naar bewijs dat de behandeling bij aanvang beter presteerde bij patiënten met een grotere mate van ziekte. Het bedrijf beoordeelt momenteel de gegevens voordat het de volgende stappen bepaalt.
Twintig meest "productieve" AI-bedrijven op het gebied van medicijnontdekking
Na een shortlist van ongeveer 130 bedrijven uit meer dan 380 AI-bedrijven in het BiopharmaTrend AI-rapport, hebben we verder 20 bedrijven geselecteerd - met behulp van een eenvoudige maar robuuste evaluatieformule die rekening houdt met klinische en preklinische pijplijnen van bedrijven, het vermogen om doelwitten te ontdekken en de tijd in zaken. De 20 geselecteerde bedrijven vormden de BPT20: kunstmatige intelligentie bij de productiviteitsindex voor het ontdekken van geneesmiddelen — het eerste referentiepunt van de industrie om bedrijven te markeren die voorstander zijn van de toepassing van AI voor de novo medicijnontwerp, virtuele screening of herbestemming van medicijnen.

AI en gerobotiseerde laboratoria van de toekomst
Deep learning-modellen (bijvoorbeeld gebaseerd op diepe neurale netwerken) zijn extreem "data-hongerig", wat betekent dat hoe goed AI ook is, het de kwaliteit en omvang van data is die net zo belangrijk zijn voor zinvolle onderzoeksvoorspellingen. De meest efficiënte manier om biologische gegevens van hoge kwaliteit te genereren, is door gebruik te maken van robotica. Als we de moderne AI-gestuurde transformatie van medicijnontdekking beschouwen als een stapsgewijs proces, een algemeen beschikbaar en relatief kostenefficiëntabotics-as-a-service zou het laatste en kritieke stuk zijn in de AI-enabled industrialisatie van farmaceutisch en biotechnologisch onderzoek. Volgens een rapport van Arctoris: "Robotica is de sleutel om het paradigma van ontdekking in een gesloten lus werkelijkheid te laten worden - wat de komende jaren een opwindende ruimte zal zijn om naar te kijken."
Sommige bedrijven bouwen gestandaardiseerde, sterk geautomatiseerde, schaalbare en in toenemende mate compatibele laboratoriumfaciliteiten, geleid door op AI gebaseerde experimentcontrolesystemen en aangevuld met door AI aangestuurde datamining en analysemogelijkheden. Dergelijke "next-gen" laboratoriumfaciliteiten worden op afstand beschikbaar voor preklinische onderzoekers op het gebied van geneesmiddelenonderzoek, waardoor preklinische experimenten een meer schaalbare en gestandaardiseerde routine worden. De toonaangevende leveranciers van externe laboratoria op de lijst zijn Automata Labs, Strateos, Emerald Labs en Culture Biosciences, om er maar een paar te noemen.
De ruimte trekt durfkapitaal en klanten aan. In februari 2022 haalde het in het VK gevestigde Automata Labs bijvoorbeeld $ 50 miljoen op om het laboratoriumonderzoeksproces te automatiseren. In juli 2021 haalde Strateos $ 56 miljoen op voor de verdere verbetering van zijn SmartLab-platform en zijn op afstand gerobotiseerde, geautomatiseerde technologie, beschikbaar voor preklinische onderzoekers over de hele wereld. Culture Biosciences heeft in totaal meer dan $ 100 miljoen opgehaald, waarvan de laatste Series B van $ 80 miljoen in november 2021 is aangekondigd. Het in San Francisco gevestigde Emerald Cloud Labs (ECL) heeft in de loop der jaren meer dan $ 90 miljoen opgehaald. Vroege gebruikers van ECL's verwijderen robotplatform rapporteerde verbeteringen van 300% tot 700% in onderzoeksproductiviteit. In juni 2022 haalde het in Peking gevestigde MegaRobo $ 300 miljoen op om zijn diverse aanbod van geautomatiseerde AI-gestuurde externe laboratoriumdiensten en gerobotiseerde faciliteiten uit te breiden.
De opkomst van gerobotiseerde laboratoria op afstand is een langetermijntrend in de sector, een nieuwe manier om contractonderzoeksdiensten aan te bieden die buitengewoon gunstig zouden zijn voor de langetermijnacceptatie van datagerichte "AI-first" onderzoeksstrategieën.
Verschillende AI-gestuurde bedrijven voor het ontdekken van geneesmiddelen, zoals Arctoris, Recursion Pharmaceuticals, Insitro en Generative Bio, benaderen deze trend via een ander bedrijfsmodel: ze hebben interne gerobotiseerde laboratoriumfaciliteiten gebouwd om hun interne capaciteiten voor het genereren van gegevens te verbeteren voor het trainen van hun AI-modellen en het bouwen van pijplijnen van kandidaat-geneesmiddelen.
Het in Oxford gevestigde Arctoris, opgericht in 2016, bouwde bijvoorbeeld een volledig geautomatiseerd wet lab dat gegevens van superieure kwaliteit op schaal genereert, invoert in het datameer van Arctoris en het AI-gestuurde besluitvormingsplatform Ulysses van het bedrijf aandrijft, dat het onderzoek van het bedrijf aandrijft vanuit target to hit, lead, en naar IND aanvraagfase.
De pijplijn van Arctoris omvat nu verschillende preklinische programma's in oncologie en neurologie. Arctoris haalde in verschillende rondes in totaal $ 10.3 miljoen op bij investeerders, waaronder Future Planet Capital, RT Ventures en Formic Ventures.
Sommige toonaangevende AI-bedrijven voor het ontdekken van geneesmiddelen, zoals Exscientia en Insilico Medicine, bouwen nu ook in-house gerobotiseerde laboratoria voor het bouwen van hun interne gegevensgeneratie-'spieren'.
Het in Salt Lake City gevestigde Recursion Pharmaceuticals is een van de leiders op het gebied van gerobotiseerde biologie-experimenten. De AI-gestuurde infrastructuur van het bedrijf, genaamd Recursion Operation System, is een geïntegreerd closed-loop-systeem dat bedrijfseigen datageneratie combineert met geavanceerde computationele tools om nieuwe inzichten te genereren om therapeutische programma's te starten of te versnellen. Het bedrijf automatiseert op grote schaal preklinische biologie-experimenten. Cellulaire microscopiebeelden leggen bijvoorbeeld samengestelde veranderingen in cellulaire morfologie vast en worden verwerkt door de AI-aangedreven computervisiesystemen van het bedrijf. Sinds 2017 heeft Recursion Pharmaceuticals de capaciteit van het fenomics-platform elk jaar ongeveer verdubbeld en het aantal uitgevoerde fenomics-experimenten opgeschaald tot 2.2 miljoen per week, resulterend in ~19 petabyte aan eigen hoogdimensionale data.
Navigeren door knelpunten in klinische onderzoeken met AI
De klinische proef is een kritieke fase in de workflow voor geneesmiddelenontwikkeling, met een geschat gemiddeld slagingspercentage van ongeveer 11% voor kandidaat-geneesmiddelen die van fase 1 naar goedkeuring gaan. Zelfs als het kandidaat-geneesmiddel veilig en werkzaam is, kunnen klinische proeven mislukken als gevolg van onvoldoende financiering, onvoldoende inschrijving of slecht studieontwerp.
Kunstmatige Intelligentie (AI) is steeds meer gezien als een bron van kansen om de operationele efficiëntie van klinische proeven te verbeteren en de kosten voor klinische ontwikkeling te minimaliseren. Doorgaans bieden AI-leveranciers hun diensten en expertise aan op drie hoofdgebieden. AI-startups op het eerste gebied helpen informatie te ontsluiten uit ongelijksoortige gegevensbronnen, zoals wetenschappelijke artikelen, medische dossiers, ziekteregisters en zelfs medische claims, door Natural Language Processing (NLP) toe te passen. Dit kan de rekrutering en stratificatie van patiënten, de selectie van locaties ondersteunen en het ontwerp van klinische onderzoeken en het begrip van ziektemechanismen verbeteren. Zo mislukken ongeveer 18% van de klinische onderzoeken als gevolg van onvoldoende rekrutering een 2015 studie gerapporteerd.
Een ander aspect van succes in klinische onderzoeken is verbeterde patiëntstratificatie. Aangezien proefpatiënten duur zijn, waren de gemiddelde kosten voor het inschrijven van één patiënt dat ook $ 15,700-26,000 in 2017 — het is essentieel om te kunnen voorspellen welke patiënt meer voordeel of risico zal hebben van de behandeling. AI-gestuurde bedrijven werken met meerdere gegevenstypen, zoals elektronische medische dossiers (EHR), omics en beeldvormingsgegevens, om de heterogeniteit van de bevolking te verminderen en de klinische studiekracht te vergroten. Verkopers zouden spraakbiomarkers kunnen gebruiken om neurologische ziekteprogressie te identificeren, beeldvormingsanalyses om behandelingsprogressie te volgen, of genetische biomarkers om patiënten met ernstigere symptomen te identificeren.
AI stroomlijnt ook de operationele processen van klinische proeven. AI-leveranciers helpen de gezondheid van de patiënt vanuit hun huis te volgen, de respons op de behandeling en de naleving van de proefprocedures door de patiënt te bewaken. Door dat te doen, verkleinen AI-bedrijven het risico op uitval van patiënten 30% gemiddeld. Gewoonlijk vereist de fase 3 klinische studiefase 1000-3000 deelnemers, waarvan een deel een placebo slikte. Daarom is de ontwikkeling van synthetische draagarmen – AI-modellen die de placebogecontroleerde groepen van individuen kunnen vervangen, waardoor het aantal individuen dat nodig is voor klinische proeven wordt verminderd – zou een nieuwe trend kunnen worden.
Volgens het BiopharmaTrend AI-rapport zijn er meer dan 80 bedrijven in alle drie de categorieën, waaronder Owkin, PathAI, GNS Healthcare, Neurcuit, AICure en Unlearn.ai.
VERWANT: 8 opmerkelijke AI-bedrijven in klinisch onderzoek om in de gaten te houden in 2022
De vraag naar AI-ondersteunde platforms voor klinische proeven is groot, evenals investeringen op dit gebied, ondanks het algehele koude investeringsklimaat in biotech.
In maart 2022 kreeg ConcertAI een waardering van $ 1.9 miljard na het bankieren van een serie C-ronde van $ 150 miljoen om zijn software en real-world data (RWD) -oplossingen voor kankeronderzoek op te schalen.
Saama is een in Silicon Valley gevestigd bedrijf dat in 1997 is opgericht, maar in 2015 zijn eerste durfkapitaal heeft opgehaald. Het bedrijf heeft meer dan $ 500 miljoen aan durfkapitaal opgehaald, waaronder de laatste megaronde van $ 430 miljoen in augustus 2022 - van Carlyle en venture-fondsen van Merck, Pfizer, Amgen, McKesson en anderen.
Saama is een van de leidende spelers op het gebied van AI-gestuurde analyse van klinische onderzoeken en biedt een diverse reeks oplossingen: versnelde klinische onderzoeken via gecentraliseerde gegevensanalyse en controlecentrum, inclusief real-time gegevensverwerkingsmogelijkheden; geautomatiseerde gegevenskwaliteitsmogelijkheden; gestroomlijnde wettelijke indieningsmogelijkheden, inclusief analyse en indiening van geneesmiddelenbewaking.
In april 2022 haalde Unlearn.AI, een startup die een 'digital twin'-service voor klinische proeven ontwikkelt, $ 50 miljoen op.
In juni 2022, Bristol Myers Squib investeerde $ 80 miljoen in OWKIN - om het ontwerp van cardiovasculaire geneesmiddelenonderzoeken te helpen verbeteren, met verbeteringen aan eindpuntdefinities, identificatie van subgroepen van patiënten en schatting van behandelingseffecten. Het in Parijs en New York gevestigde "unicorn" OWKIN maakt gebruik van onze hoogwaardige multimodale gegevenstoegang en ultramoderne machine learning om verschillende behandelingseffecten op subpopulaties van patiënten nauwkeurig te voorspellen om het ontwerp en de resultaten van klinische proefexperimenten te verbeteren. OWKIN past zijn AI-platform ook toe voor het ontdekken van geneesmiddelen.
In augustus 2022 kondigde Bristol Myers Squibb ook een meerjarige uitgebreide samenwerkingsovereenkomst aan met AI-pathologiespecialist PathAI. De eerste werkzaamheden binnen deze verlengde overeenkomst zullen gericht zijn op belangrijk translationeel onderzoek op het gebied van oncologie, fibrose en immunologie, met als algemeen doel deze door te sturen naar klinische onderzoeken. Twee maanden eerder sloot PathAI een strategische meerjarige samenwerking met GlaxoSmithKline om wetenschappelijke onderzoeks- en geneesmiddelenontwikkelingsprogramma's in oncologie en niet-alcoholische steatohepatitis (NASH) te versnellen door gebruik te maken van PathAI's technologieën in digitale pathologie, inclusief het gebruik van PathAI's AIM-NASH-tool.
Met name Akkure Genomics uit Dublin net aangekondigd het heeft in één week € 1 miljoen gecrowdfund ter ondersteuning van klinische onderzoeken via zijn AI-platform, dat mensen helpt deel te nemen aan de meest relevante klinische onderzoeken op basis van gegevens over zichzelf en hun aandoening.
AI in de contractonderzoeksindustrie
De opkomst van nieuwe AI-native contractonderzoeksbedrijven in preklinische en klinische ruimtes vormt een uitdaging voor de status quo van grote gevestigde contractonderzoeksorganisaties (CRO's). Ze reageren door AI op te nemen in hun dienstenaanbod voor farma of door samen te werken met AI-bedrijven om hun onderzoekscapaciteit aan te vullen.
VERWANT: De evoluerende farmaceutische R&D outsourcing-industrie: een vogelvlucht.
Charles River Labs, een in de VS gevestigde organisatie voor contractonderzoek in een vroeg stadium, duikt bijvoorbeeld dieper in AI door een meerjarige samenwerking met Valo Health. Charles River voegt Valo's Opal-technologie toe die actief leert terwijl programma's worden ontwikkeld. Charles River hoopt dat het gebruik van het Opal deep learning-platform zal resulteren in een sneller en effectiever proces van de novo molecuulontwerp tot leadoptimalisatie. Vorig jaar richtte Charles River een strategisch partnerschap met Valence Discovery die de klanten van de CRO toegang gaf tot het kunstmatige-intelligentieplatform van Valence voor voorspelling van moleculaire eigenschappen, generatieve chemie en multiparameteroptimalisatie.
IQVIA investeert al jaren in AI-mogelijkheden om waarde toe te voegen aan klinische proeven en commerciële activiteiten die het aan klanten aanbiedt. Om klinische proeven te verbeteren, bijvoorbeeld IQVIA gelanceerd Avacare Clinical Research Network™ in 2020, waardoor sites patiënten sneller en efficiënter konden matchen voor de onderzoeken. Het platform wordt aangedreven door AI-algoritmen en kan werken in 19 ziektegebieden. Eerder won een ander IQVIA's Linguamatics Natural Language Processing (NLP)-platform Questex's 2019 Fierce Innovation Awards. Het platform kan enorme toepassingen hebben in de gezondheidszorg en biowetenschappen, waaronder doelidentificatie, het in kaart brengen van genen, het voorspellen van patiëntresultaten, enzovoort.
Er is een belangrijke trend gaande in de klinische onderzoeksindustrie virtuele klinische proeven, een markt ter waarde van 8 miljard dollar. De COVID-19-pandemie dwong farmaceutische bedrijven om over te schakelen op monitoring op afstand, verbeterde patiëntregistratie, apps om de betrokkenheid van patiënten bij te houden, telegeneeskunde, decentralisatie en andere maatregelen om onderzoeken door te laten gaan. Omdat de vraag naar dergelijke oplossingen aanzienlijk toenam, haastten CRO's zich om virtuele en gedecentraliseerde mogelijkheden aan hun dienstenaanbod toe te voegen. AI-technologie bleek van onschatbare waarde bij het opzetten en uitvoeren van dergelijke projecten om gegevens te synthetiseren en klinische proefprocessen te versnellen.
Technologiereuzen gaan achter medicijnontdekking en biotech aan
De eerder genoemde successen van de DeepMind en Meta van Alphabet bij het oplossen van fundamentele biologieonderzoekraadsels, zoals het op schaal voorspellen van eiwitstructuren met behulp van deep learning en taalmodellen, zijn slechts het topje van de ijsberg: bijna elke toonaangevende technologische gigant is nu werkzaam in de life sciences-business , op de een of andere manier.
Alphabet (een moederbedrijf van Google) heeft tientallen investeringen in life science-projecten, waaronder de op AI gebaseerde reagenszoekmachine BenchSci, de in China gevestigde AI en kwantumfysica in XtalPi, het bedrijf voor het ontdekken van geneesmiddelen, het bedrijf voor persoonlijke genomica 23andMe en de door AI aangestuurde geneesmiddelenontwikkeling eenhoorn OWKIN om er maar een paar te noemen. In 2021 lanceerde Alphabet samen met DeepMind Isomorphic Labs om zich te concentreren op het toepassen van kunstmatige intelligentie om basisbiologie en medicijnontdekking te doorbreken.
Naast meerdere andere projecten en activiteiten op het gebied van farmaceutisch onderzoek en biotech, heeft Alphabet een volledige entiteit, Verily, die zich toelegt op Life Sciences en MedTech.
Microsoft, een wereldwijde softwareontwikkelaar, heeft een diepe voetafdruk in Life Sciences, met tientallen onderzoekssamenwerkingen met big pharma, en levert zijn infrastructuren om big data te verwerken met behulp van grootschalige machine learning-modellen. Een van de nieuwste Microsoft-initiatieven is MoLeR-model, een nieuwe tool die wordt ontwikkeld door het generatieve chemieteam van het bedrijf in samenwerking met Novartis. Het MoLeR-model maakt - in tegenstelling tot andere generatieve tools - gebruik van deep learning om nieuwe structuren te bedenken op basis van een bepaalde steiger die fungeert als een eerste basis voor het generatieve proces. Een ander voorbeeld is AI4Wetenschap, een nieuwe onderneming van Microsoft die computationele chemie, kwantumfysica, machine learning, moleculaire biologie, vloeistofdynamica en software-engineering combineert om een visie van het zogenaamde "vijfde paradigma" van de wetenschap te realiseren.
VERWANT: Hoe "Big Tech" langzaam de farmaceutische markten wint
Een bijzonder actief bedrijf in deze context is een hardwareproducent voor de game-industrie en personal computers, NVIDIA. Dit technologiebedrijf heeft Clara Discovery gelanceerd, een verzameling frameworks, applicaties en AI-modellen die GPU-versnelde medicijnontdekking mogelijk maken, met ondersteuning voor onderzoek op het gebied van genomica, proteomica, microscopie, virtuele screening, computationele chemie, visualisatie, klinische beeldvorming en natuurlijke taalverwerking (NLP). En in maart 2022 introduceerde het bedrijf Clara Holoscan MGX™, een platform voor de medische apparatuurindustrie om real-time AI-applicaties aan de rand te ontwikkelen en te implementeren, speciaal ontworpen om te voldoen aan de vereiste wettelijke normen. Clara Holoscan streeft naar een alles-in-één referentiearchitectuur van medische kwaliteit, evenals softwareondersteuning op lange termijn, om innovatie in de medische hulpmiddelenindustrie te versnellen.
De toekomst van AI bij het ontdekken van medicijnen: alles wat met 'kwantum' te maken heeft
De meeste softwaretools die worden gebruikt voor het ontdekken van geneesmiddelen en biologisch onderzoek, zijn gebaseerd op moleculaire mechanica - een vereenvoudigde weergave van moleculen, waardoor ze in wezen worden gereduceerd tot "ballen en stokjes": atomen en verbindingen ertussen. Op deze manier is het gemakkelijker te berekenen, maar de nauwkeurigheid lijdt er enorm onder. Om voldoende nauwkeurigheid te krijgen, moet men rekening houden met het elektronische gedrag van atomen en moleculen, dwz subatomaire deeltjes overwegen - elektronen en protonen. Dit is waar kwantummechanische (QM) methoden over gaan - en de theorie is niet nieuw, ze dateert uit de eerste decennia van de 20e eeuw.
Kwantummethoden zijn echter buitengewoon rekenkundig duur - en tot de afgelopen decennia vormde het een belemmerende barrière voor de kwantumtheorie om de praktische kant van de zaak te beïnvloeden. Door de exponentiële groei van beschikbare rekenkracht worden kwantummethoden eindelijk waardevolle hulpmiddelen in de handen van wetenschappers.
Verschillende bedrijven combineren machine learning en kwantumtheorie om de modelleringsmogelijkheden van hun systemen voor het ontdekken van geneesmiddelen aanzienlijk te verbeteren. Wetenschappers van XtalPi, een in China en de VS gevestigd technologiebedrijf dat wordt ondersteund door Sequoia China, Tencent en Google, hebben bijvoorbeeld hun Intelligent Digital Drug Discovery and Development (ID4)-platform gebouwd, waarin kwantummechanica, kunstmatige intelligentie en krachtige cloud computing-algoritmen. Met ID4 kunnen met hoge precisie de fysisch-chemische en farmaceutische eigenschappen van kandidaat-geneesmiddelen met een klein molecuul worden voorspeld, evenals hun kristalstructuren - cruciale elementen in O&O op het gebied van geneesmiddelen.
Een ander bedrijf dat op dit gebied vooruitgang boekt, is het in Parijs gevestigde Aqemia. Het bedrijf richt zich op de novo, op structuur gebaseerd ontwerp van loodachtige moleculen door kwantum- en kunstmatige intelligentie (AI) te combineren. Een uniek op kwantum geïnspireerd algoritme voor statistische mechanica dat de affiniteit tussen een verbinding en een therapeutisch doelwit nauwkeurig en 10,000 keer sneller voorspelt dan de concurrentie. De AI van Aqemia kan verbindingen met toenemende nauwkeurigheid genereren door feedback te krijgen van de affiniteitsvoorspeller.
Ten slotte is er het in Barcelona gevestigde Pharmacelera, een computationeel bedrijf dat kwantumtheorie toepast om het ontwerpen van geneesmiddelen te stimuleren via hun twee primaire softwarepakketten: PharmScreen en PharmQSAR. De eerste tool maakt een nauwkeurige, op ligand gebaseerde virtuele screening mogelijk met behulp van een zeer nauwkeurig 3D-ligand-uitlijningsalgoritme op basis van de interactievelden. Het kan een hoger diversiteitspercentage onder leads genereren dan klassieke methoden en tools. De tweede - PharmQSAR, is een 3D kwantitatieve structuur-activiteitsrelatie (QSAR) tool die een combinatie van meerdere interactievelden mogelijk maakt om CoMFA/CoMSIA-onderzoeken uit te voeren.
VERWANT: 12 bedrijven die kwantumtheorie gebruiken om de ontdekking van geneesmiddelen te versnellen
Een andere, meer futuristische, technologische trend, waarbij gebruik wordt gemaakt van de kwantumtheorie, betreft het creëren van een kwantumcomputer. Met tientallen jaren vooruitgang in de kwantumtheorie en gelijktijdige vooruitgang op verschillende software- en hardwaregebieden, gaan we eindelijk het tijdperk in waarin kwantumcomputers praktisch levensvatbaar worden.
Hoewel we ons in de begindagen van quantum computing bevinden, integreren verschillende bedrijven al elementen van quantum computing in computationele medicijnontdekking.
POLARISqb is bijvoorbeeld een in het VK gevestigde ontwikkelaar van 's werelds eerste software voor het ontdekken van geneesmiddelen die is gebouwd voor kwantumcomputers, waarbij kunstmatige intelligentie en een kwantumbenadering worden gecombineerd. De kern van POLARISqb-technologie is het Tachyon-platform voor het ontwerpen van geneesmiddelen, dat wordt gebruikt voor het uitvoeren van gedistribueerd moleculair ontwerpwerk in de cloud, beheerd door een geautomatiseerd proces dat het mogelijk maakt om grote chemische bibliotheken te doorzoeken terwijl meerdere projecten parallel worden uitgevoerd. Door eigen software voor kwantumsystemen te ontwikkelen, beweert het bedrijf dat het het ontwerp van geneesmiddelen aanzienlijk kan versnellen en leads van hogere kwaliteit kan krijgen. Vanwege het inherente "agnosticisme" van het Tachyon-systeem, kan het bij meerdere ziekten en indicaties werken.
Menten AI is een Canadese start-up, opgericht in 2018, die een softwareplatform ontwikkelt voor het ontwerpen van eiwitten, mogelijk gemaakt door machine learning en quantum computing. Het bedrijf gebruikt eigen algoritmen voor kwantumoptimalisatie, die volgens het bedrijf de nauwkeurigheid van de ontdekking van geneesmiddelen aanzienlijk kunnen verbeteren en tegelijkertijd de kosten en ontwikkelingstijd kunnen verminderen.
Laten we, om dit bericht samen te vatten, verwijzen naar een voorspelling van Dr. Christopher Savoie, medeoprichter en CEO van Zapata Computing, een Amerikaans kwantumsoftwarebedrijf, over baanbrekend onderzoek op dit gebied, dat hij uitdrukte in een interview voor BiopharmaTrend:
“Quantum zal in de toekomst deel uitmaken van elke of bijna elke workflow voor datawetenschap en machine learning in de biofarmaceutische sector. Ik denk dat het er een integraal onderdeel van zal zijn. Als je een nauwkeuriger model kunt krijgen door kwantumtechnologie te gebruiken, waarom zou je dat dan niet doen?”
Grote taalmodellen boeken vooruitgang bij het ontdekken van geneesmiddelen
Grote taalmodellen (LLM's) zoals OpenAI's ChatGPT worden gebruikt door biotechbedrijven, zoals Insilico geneeskunde, Onschuld en exscientia, om medicijnontdekking te helpen.
ChatGPT helpt wetenschappers om te gaan met AI en machine learning-tools, waardoor gegevens toegankelijker worden. Insilico Medicine gebruikt bijvoorbeeld ChatGPT om te communiceren met hun platform voor het ontdekken van doelen, PandaOmics, terwijl de oprichter van Ainnocence Lurong P. voorziet gespecialiseerde versies zoals Bio ChatGPT of Med ChatGPT. Exscientia gebruikt LLM's om gestructureerde, mechanistische beweringen te genereren voor hun kennisgrafieken.
LLM's dienen ook als geavanceerde zoekmachines in de biologische wetenschap. Google en DeepMind's Med-PaLM-chatbot geeft antwoord op medische vragen, terwijl Welwillende AI lijkt enthousiast over de ophaalplug-infunctie van ChatGPT, die zou kunnen helpen de chatfunctie aan te passen op basis van hun eigen gegevens.
Ondanks het potentieel van LLM's bij het ontdekken van geneesmiddelen, houden sommige bedrijven ervan BioXcel Therapeutics, Inc. en Enteroom voorzichtig blijven met het toepassen van de technologie, daarbij verwijzend naar zorgen over nauwkeurigheid en privacy.
Het is duidelijk dat de opkomst van ChatGPT en andere generatieve AI-modellen, zoals DeepMind's AlphaFold, het bewustzijn van hun potentiële toepassingen in de biotechnologie heeft vergroot, waardoor bedrijven worden aangemoedigd om hun voordelen bij het ontdekken en ontwikkelen van geneesmiddelen te onderzoeken.
Onderwerpen: Industry Trends
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoData.Network Verticale generatieve AI. Versterk jezelf. Toegang hier.
- PlatoAiStream. Web3-intelligentie. Kennis versterkt. Toegang hier.
- PlatoESG. Automotive / EV's, carbon, CleanTech, Energie, Milieu, Zonne, Afvalbeheer. Toegang hier.
- BlockOffsets. Eigendom voor milieucompensatie moderniseren. Toegang hier.
- Bron: https://www.biopharmatrend.com/post/615-pharmaceutical-artificial-intelligence-key-developments-in-2022/



