米国国立標準技術研究所(NIST)は8月XNUMX日、権利におけるMarchの使用についてコメントを募るガイドラインを発表した。 SpicyIP のインターン Jyotpreet Kaur は、これらの権利、ガイドラインで提案されている変更、同様の取り決めに対するインドの立場について書いています。この投稿は Swaraj からの情報をもとに書かれています。 Jyotpreet はデリー国立法科大学の法学部 XNUMX 年生で、知的財産権と競争法に興味があり、それらの相互作用を研究したいと考えています。彼女の以前の投稿にアクセスできます こちら.

米国による進入権の見直しとインドの対応者に対するいくつかの疑問
ジョットプリート・カウル著
多くの読者が知っているように、米国政府は、多くの司法的精査を経て単一の強制ライセンスが与えられた後、特に米国通商代表部を通じて、何年にもわたってインドを追い詰めてきた。それができたのは新型コロナウイルス感染症(COVID-19)の時だけでした。 この圧力は露骨に加えられなくなりました (代わりに「企業秘密」への移行とともに)。非常に興味深い出来事の展開として、米国は現在、独自のバージョンの強制ライセンス、別名「マーチイン」権を国内で適用する方法を拡大するガイドラインに向けて前進しているようです。増え続ける医療費に起因する国内の圧力が、ついに特許制度が医療費にどのような影響を与えているかを再検討する段階に達したようだ。 8月XNUMX日、米国標準技術研究所(NIST)は草案を発表した。 ガイドライン 薬価引き下げというバイデン政権の目標を促進するための「マーチ・イン」権の使用についてのコメントを募集している。 NIST によると、米国政府はさまざまな大学、非営利団体、企業を通じて研究開発に約 115 億ドルを投資しています。マーチ・イン権は、一定の条件が満たされた場合に、政府がこの投資から生じる発明のライセンスを要求できるようにする条項です。注目すべきは、マーチ・イン権の「脅威」は以前にも取り上げられたことがあるが、準拠法が制定されて以来 44 年間、実際には行使されていないことである。これらのガイドライン草案の目的は、マーチインの権利を行使できる基準を拡大することにあるようだ。米国保健福祉長官 歓迎 これは「アメリカの納税者が投資から公正な利益を得られるようにするための強力なツール」です。
イノベーションと公益のバランス: マーチ・イン権と対比したバイ・ドール法の目的
1980年に制定されたバイ・ドール法は、とりわけ連邦政府の「進入」権を前面に押し出した。前述したように、マーチイン権は、政府の資金提供を受けた研究から知的財産を開発している企業がその知的財産を適切に商業化していない場合に政府が利用できる固有の措置に似ています。この権限を行使する場合、政府は介入して知的財産権の使用を指示したり、第三者にライセンスを供与したりすることが許可されます。特許の所有権は研究所にあります。政府がこの権利を行使することを選択した場合に、政府に有利に発生する、第三者にライセンスを供与する権利のみです。この権利の目的は、問題の公的資金による知的財産権が発明者機関によって十分に活用されていない場合に、その可能性を政府が十分に実現できるようにすることです。
バイ・ドール法に基づく進入権の行使は、合衆国法典第 35 条に基づいて想定されている。 § 203 では、4 つの法定基準を満たす必要があります。これらは、(i) 主題のイノベーションを効果的に実現できていない。 (ii) 未対処の健康または安全のニーズを軽減する必要性。 (iii) 発明の公共利用の要件を満たしていない場合。 (iv) 特に以下に基づく契約上の義務の不履行。 204. これは、特許製品が商業的に不可能になるまで大幅に米国内で製造されることを義務付けています。
現在まで、進入権を求める請願にもかかわらず、米国政府は進入権を行使していない。マーチ・イン権の行使を求める申し立てが初めて提出されたのは、 CellProについて 政府がこの権利の行使を拒否した場合。からもわかるように、この傾向は現在も続いています。 8つの請願 これらはNIHに提出され、処分されました。
マーチ・インの権利の刷新: 災難への処方箋か、それとも成功への処方か?
ガイドラインを通じて導入された変更の 60 つは、マーチイン権の行使に先立って請負業者との非公式な代理店協議プロセスを明確にし、非公式協議後に代理店が請負業者に応答しなければならない許容時間を 120 日から延長することです。日から XNUMX 日まで。
これとは別に、新しいガイドラインでは、マーチイン権を行使するプロセスを明確にするための3段階の方法が導入されています(画像を参照)。まず、バイ・ドール法が問題の発明に適用されるかどうかが確認されます。ここでは、当該発明が「主題発明」であるかどうか、また政府の資金提供を受けているかどうかがチェックされます。第二に、上記の 4 つの法定基準のいずれかが本件に適用されるかどうか、そして最後に、マーチイン権の行使がバイ・ドール法の全体的な精神とその目的に従っているかどうかです。
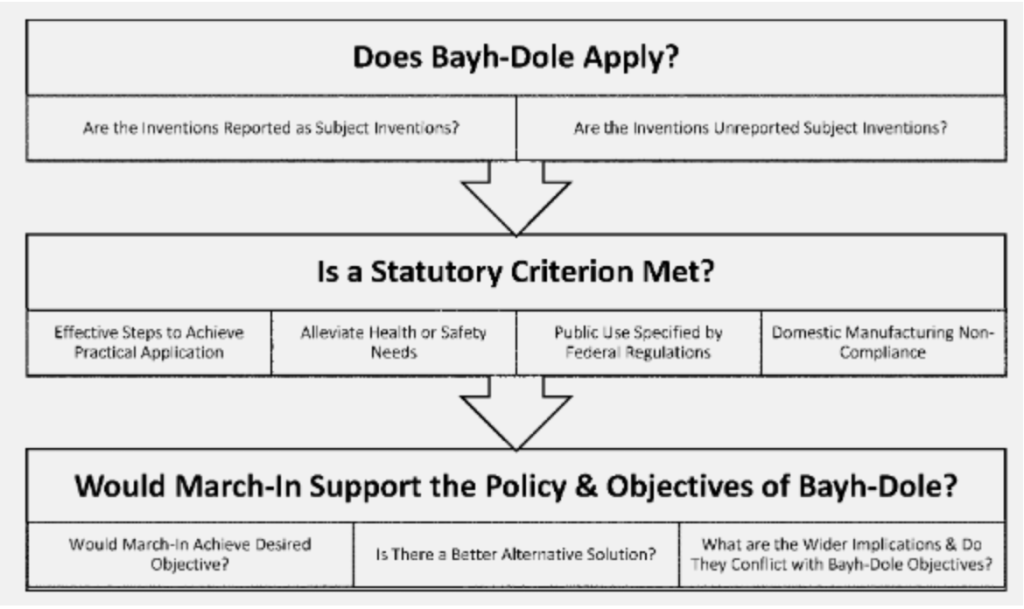
おそらく最も重要な変化は、第 1 法定基準を援用しながらの第 XNUMX ステップ、つまり、特許受領者がその使用分野における「主題のイノベーション」の実現に向けた効果的な措置を講じることができなかった、または今後取らないであろう場合に見られます。このガイドラインには、「発明の公衆への利用を不当に制限する」可能性のある要因の考慮が追加されています。ここで、ガイドラインは、以前は「マーチイン」権利の行使の基準として認識されていなかった、合理的な価格設定の要件を導入しました。このガイドラインでは、「請負業者またはライセンシーが、価格が高いために、一部の消費者または顧客のみに製品を提供したのか」という質問をすることが求められています。
これは、マーチインを行使する根拠としての高価格設定との過去のやり取りから証明できる政府の初期のスタンスとは対照的である。 2004年、請願者は、NIHと呼ばれるHIV治療薬の価格が高いことを理由に、この措置を発動するようNIHに訴えた。 Norvir というタイトルの緑内障治療薬です。 キサラタン。 2012 年には、 Norvir NIHの前に再び提起されました。 2016年にも、請願者らは、その価格の高さをめぐる懸念を提起した。 タンディ 他の高所得国と比較して、98錠あたり約XNUMXドルの薬の値段がします。しかし、これらすべてのケースにおいて、NIHは単に価格設定を理由にマーチイン権の行使を拒否し、他の拒否理由を挙げた。
ガイドラインでは合理的な価格設定について言及していますが、「合理的な」価格とは何かについては言及しておらず、これは連邦政府の裁量に委ねられています。
支持者たちは、これらのガイドラインを、法外な薬物を一般のアメリカ国民がより入手しやすくし、連邦政府の資金による研究は基本的に納税者のお金で賄われているため、「正当に」彼らのものであるものを国民に還元するための進歩的な措置であると歓迎している。
一方、ガイドラインに反対する人々は、価格設定が「マーチ・イン」権行使の根拠として想定されていなかったため、これらはバイ・ドール法の目的に反するものであると主張している。米国商工会議所は、これらのガイドラインを「政府による没収」の一形態と呼んでいる。このような条項は、この法の主な目的である技術革新と競争を阻害するだろうと主張する人もいます。 いくつかは主張している 同法の目標は、現在のガイドラインが達成しようとしているものとは異なり、医薬品アクセスの問題と市場の非効率性の軽減という新しいアイデアを市場に導入することを目的として官民の協力を促進することであると述べた。 ジョセフ・アレン また、これらのガイドラインは「大手製薬会社」をターゲットにすることを目的としているが、最終的には実際にバイ・ドール法の適用を受ける小規模発明者に損害を与えることになるため、「毒薬」であると主張している。研究は政府の資金提供を受けていない。同時に、これらのガイドラインは高い薬価(のみ)を念頭に置いて組み立てられており、バイ・ドールが今後影響を受けるであろうエネルギー、農業、環境保護などの他の産業も対象としているということを無視している、と彼は主張する。このガイドラインの逆境。
インド戦線で何が起きているのか?
現在、この議論は米国でより真剣に受け止められているが、インドにも波及効果はあるだろうか?インドの紙面上の特許の柔軟性は非常に堅牢であり、セクション 3(d) のようないくつかの条項はその存在感を示していますが、他の多くの条項が実際の効果に翻訳されたり実践されたりする様子はまだ見ていません。例えば、他のいくつかの薬物の強制実施についての議論があったが、これらの議論からは何も生まれていない。このうちどの程度が外部圧力、たとえばさまざまな FTA やもちろん USTR によるものであるかは不明です。そして、このうちのどれくらいが他の理由によるものである可能性がありますか。例えば、インドは新型コロナウイルス感染症パンデミックの最中に最前線で知的財産権の免除を求めていたものの、皮肉なことに、政府は国内レベルでの要求を行っていた。 取れる選択肢の数、あまりアクションは取られませんでした。たとえば、政府は次のようなものを提供できなかった。 IPRの所有権の明確性 (コヴァキシン)とそのハフカイン研究所への「承認を与える」行為は、議論されているように「健康への権利」に対する公共の利益を損なうべきものであった。 こちら & こちら。同様に、インド政府は、開示免除の根拠として知的財産権を規定する第 8 条(1)(d) および (e) を引用して、RTI を通じた臨床試験データの開示を拒否していました。国は、この保護を危機に瀕している公益と比較検討するというバランスをとることなく、データの公開を拒否する際に知的財産権の保護を発動した(これは TRIPS の S. 39(3) にも規定されている)。このように、国家は国際的な立場とは対照的に、自らの知的財産を公然と行使することができていない。
いずれにせよ、米国がこれまで国際的に強い立場をとってきた事柄について米国内で議論が行われているのは、興味深い展開だ。国内では、バイオテクノロジー省が最近、DBT 資金提供から生じる発明に関する独自の知的財産ガイドライン セットを発表しました。これはどうなるのでしょうか?また、失敗に終わった「公的資金による知財の保護と利用法案」を復活させる新たな試みの始まりとなるのでしょうか?同時に政府は次のような政策を打ち出しました。 製薬・医療技術分野における研究開発とイノベーションに関する国家政策 (ポリシー草案を参照) こちら)2023年XNUMX月にインドの製薬部門を「変革」し、研究インフラの強化と製薬部門における研究の促進という二重の方法でこれらの部門の研究開発を「促進」することを目的としています。注目すべきことに、このポリシーは知的財産に関する質問にはまったく対応していません。おそらく、これらはすべて熟考する価値のある質問であり、別の記事でまとめてみたいと思います。
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- PlatoData.Network 垂直生成 Ai。 自分自身に力を与えましょう。 こちらからアクセスしてください。
- プラトアイストリーム。 Web3 インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- プラトンESG。 カーボン、 クリーンテック、 エネルギー、 環境、 太陽、 廃棄物管理。 こちらからアクセスしてください。
- プラトンヘルス。 バイオテクノロジーと臨床試験のインテリジェンス。 こちらからアクセスしてください。
- 情報源: https://spicyip.com/2024/01/the-us-review-of-march-in-rights-and-some-questions-on-an-indian-counterpart.html



