Антибиотики спасли бесчисленное количество жизней и являются важнейшим инструментом современной медицины. Но мы теряем позиции в борьбе с бактериями. В середине прошлого века учёные открыл совершенно новые классы антибиотиков. С тех пор темпы открытий замедлились, а распространенность бактерий, устойчивых к антибиотикам, выросла.
Вероятно, антибиотики еще предстоит открыть, но химическая вселенная слишком велика, чтобы ее можно было исследовать. В последние годы ученые обратились к ИИ. Алгоритмы машинного обучения могут свести огромное количество потенциальных химических конфигураций к нескольким многообещающим кандидатам для тестирования.
На сегодняшний день ученые использовали ИИ для поиска отдельных соединений со свойствами антибиотиков. Но в новом исследовании опубликовано вчера в природаИсследователи Массачусетского технологического института говорят, что они создали и протестировали систему, которая может идентифицировать совершенно новые классы антибиотиков и прогнозировать, какие из них, вероятно, безопасны для людей.
ИИ проанализировал более 12 миллионов соединений и обнаружил неоткрытый класс антибиотиков, которые доказали свою эффективность на мышах против метициллин-резистентного Staphylococcus aureus (MRSA), смертельного штамма устойчивых к лекарствам насекомых.
Хотя эти антибиотики, открытые с помощью ИИ, еще должны доказать свою безопасность и эффективность на людях, пройдя стандартные испытания клинических испытаний, команда считает, что их работа может ускорить открытие на начальном этапе и, как мы надеемся, увеличить общий показатель успеха.
Исследование пространства наркотиков
Ученые все чаще используют помощников ИИ, чтобы ускорить процесс открытий. Пожалуй, самой известной является AlphaFold от DeepMind — программа машинного обучения, которая может моделировать форму белков — основных строительных блоков нашего тела. Идея состоит в том, что AlphaFold и его потомки могут ускорить трудный процесс исследования лекарств. Их убежденность настолько сильна, что в 2021 году DeepMind создала дочернюю компанию. Изоморфные лаборатории, посвященный именно этому.
Другие подходы к искусственному интеллекту также показали себя многообещающе. Группа Массачусетского технологического института, в частности, сосредоточилась на разработке совершенно новых антибиотиков для борьбы с супербактериями. Их первое исследование, опубликованное в 2020 году, показало, что этот подход может сработать, когда они обнаружили халицин, ранее не обнаруженный антибиотик, который может легко уничтожить устойчивую к лекарствам кишечную палочку.
По словам Джонатана Стоукса из Университета Макмастера, старшего автора исследования, в начале этого года команда нацелилась на Acinetobacter baumannii, «общественного врага № 1 в отношении бактериальных инфекций с множественной лекарственной устойчивостью».
«Ацинетобактер может выживать на больничных дверных ручках и оборудовании в течение длительного периода времени, а также может поглощать гены устойчивости к антибиотикам из окружающей среды. Сейчас очень часто можно найти изоляты A. baumannii, устойчивые почти ко всем антибиотикам». Стоукс сказал тогда.
Прочесав 6,680 соединений всего за два часа, ИИ выделил несколько сотен многообещающих кандидатов. Команда протестировала 240 из них, которые структурно отличались от существующих антибиотиков. Они выявили девять многообещающих кандидатов, в том числе один, абауцин, весьма эффективный против A. baumannii.
Оба исследования показали, что этот подход может работать, но выявили только одиночных кандидатов без информации о зачем они были эффективны. Алгоритмы машинного обучения, как известно, представляют собой черные ящики: то, что происходит, так сказать, «между ушами», часто является полной загадкой.
В последнем исследовании группа нацелилась на другого известного противника, MRSA, только на этот раз они объединили несколько алгоритмов, чтобы улучшить результаты и лучше прояснить рассуждения ИИ.
Переключатель
Последняя ищейка команды, работающая с антибиотиками, обучалась примерно 39,000 XNUMX соединениям, включая их химическую структуру и способность убивать MRSA. Они также обучили отдельные модели прогнозировать токсичность того или иного соединения для клеток человека.
«Вы можете представить практически любую молекулу как химическую структуру, а также указать модели, является ли эта химическая структура антибактериальной или нет», — Феликс Вонг, постдок в IMES и Институте Броуда Массачусетского технологического института и Гарварда, заявил Новости MIT. «Модель обучена на многих подобных примерах. Если затем вы дадите ему какую-нибудь новую молекулу, новое расположение атомов и связей, он может сказать вам, с какой вероятностью это соединение будет антибактериальным».
После завершения команда загрузила в систему более 12 миллионов соединений. ИИ сузил этот огромный список примерно до 3,600 соединений, разделенных на пять классов — в зависимости от их структуры — он предсказал, что они будут обладать некоторой активностью против MRSA и будут минимально токсичными для клеток человека. Команда составила окончательный список из 283 кандидатов для тестирования.
Из них они обнаружили два из одного и того же класса (то есть, у них были схожие структурные компоненты, которые, как полагают, способствуют антимикробной активности), которые оказались весьма эффективными. У мышей антибиотики боролись как с кожной, так и с системной инфекцией, уничтожая 90 процентов присутствующих бактерий MRSA.
Примечательно, что в то время как их предыдущая работа касалась грамотрицательных бактерий путем разрушения клеточных мембран, MRSA является грамположительным и имеет более толстые стенки.
«У нас есть довольно убедительные доказательства того, что этот новый структурный класс активен против грамположительных патогенов, избирательно рассеивая движущую силу протонов в бактериях», — сказал Вонг. «Молекулы избирательно атакуют мембраны бактериальных клеток, не нанося существенного ущерба клеточным мембранам человека».
Сделав свой ИИ объяснимым, команда надеется сосредоточиться на структурах, которые могут стать основой для будущих поисков или способствовать разработке более эффективных антибиотиков в лаборатории.
Выпускные экзамены
Здесь важно отметить, что, хотя новые антибиотики оказались эффективными на мышах в очень небольших масштабах, предстоит пройти долгий путь, прежде чем вам их пропишут.
Новые лекарства проходят строгие испытания и клинические испытания, и многие, даже многообещающие кандидаты, не доходят до другой стороны. Область открытия лекарств с помощью ИИ в более общем плане все еще на ранних стадиях в этом отношении, Первый Лекарства, созданные с помощью ИИ, сейчас проходят клинические испытания, но ни один из них еще не был одобрен.
Тем не менее, есть надежда на более быстрое пополнение конвейера лучшими кандидатами.
На открытие нового антибиотика, подходящего для клинических испытаний, может уйти от трех до шести лет. по данным Университет Пенсильвании Сезар де ла Фуэнте, чья лаборатория делает аналогичную работу. Тогда у вас есть сами испытания. Поскольку устойчивость к антибиотикам растет, у нас может не быть такого времени, не говоря уже о том, что антибиотики не приносят окупаемости инвестиций, которые есть у других лекарств. Любая помощь приветствуется.
«Теперь, благодаря машинам, мы смогли ускорить [временную шкалу]», де ла Фуэнте рассказал Scientific American. «Например, в моей работе и работе моих коллег мы можем за считанные часы обнаружить тысячи или сотни тысяч доклинических кандидатов вместо того, чтобы ждать от трех до шести лет. Я думаю, что искусственный интеллект в целом позволил это сделать».
Пока еще рано, но если антибиотики, открытые с помощью ИИ, окажутся достойными в ближайшие годы, возможно, мы сможем сохранить преимущество в нашей давней борьбе с бактериями.
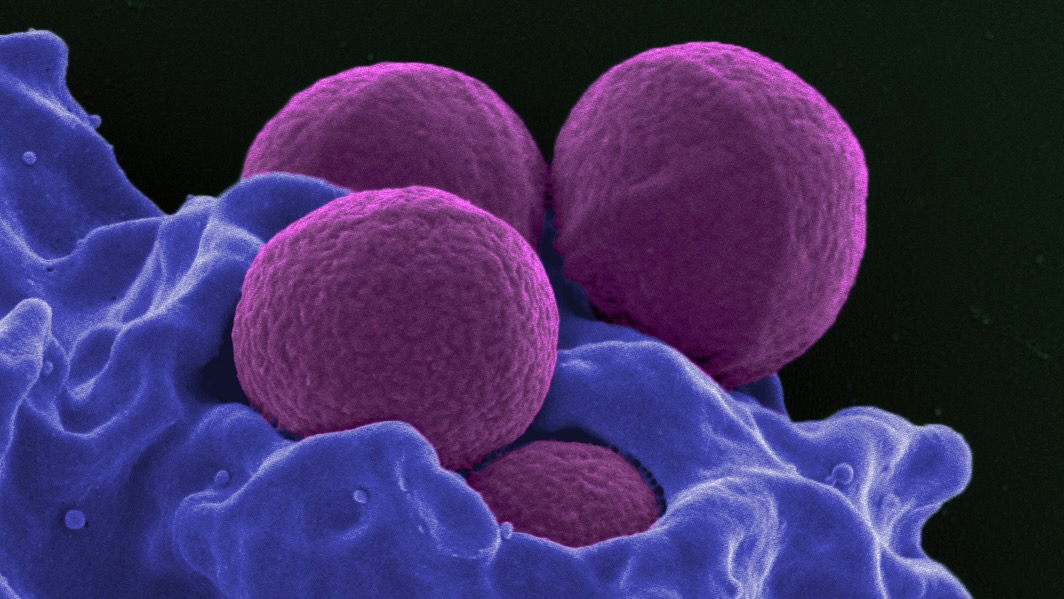
Изображение Фото: Лейкоциты человека, проглатывающие MRSA (фиолетовый) / Национальный институт аллергии и инфекционных заболеваний, Национальные институты здравоохранения
- SEO-контент и PR-распределение. Получите усиление сегодня.
- PlatoData.Network Вертикальный генеративный ИИ. Расширьте возможности себя. Доступ здесь.
- ПлатонАйСтрим. Интеллект Web3. Расширение знаний. Доступ здесь.
- ПлатонЭСГ. Углерод, чистые технологии, Энергия, Окружающая среда, Солнечная, Управление отходами. Доступ здесь.
- ПлатонЗдоровье. Биотехнологии и клинические исследования. Доступ здесь.
- Источник: https://singularityhub.com/2023/12/21/ai-discovers-a-new-class-of-antibiotics-after-scouring-12-million-compounds/



