We hebben allemaal te maken met de dreigende dreiging om tijdens ons leven kanker te ontwikkelen, hoe goed onze genetica ook is, of hoe gezond onze levensstijl ook is. Ondanks grote verbeteringen in de manier waarop we gevallen van kanker behandelen en zelfs genezen, is de realiteit vandaag de dag dat niet alle soorten kanker behandelbaar zijn. In veel gevallen bestaat de kans dat de kanker op een dag zal terugkeren, zelfs na volledige remissie, en chemotherapie in het bijzonder. gaat gepaard met potentiële levenslange gezondheidsproblemen. Van de meest veelbelovende nieuwe en opkomende behandelingen behoort immunotherapie beslist tot de meest veelbelovende.
Met deze aanpak wordt het lichaamseigen immuunsysteem geleerd om die kankercellen aan te vallen, waarbij weinig meer nodig is dan een paar aanpassingen aan de T-cellen die uit het lichaam van de patiënt zijn geoogst, waarna ze op hun vrolijke, kankerdodende manier worden gestuurd. . Maar hoe eenvoudig dit ook klinkt, het vinden van de juiste kenmerken die de kankercellen identificeren en het verkrijgen van een solide en langdurige immuunrespons is een zware uitdaging. Ondanks veelbelovende resultaten met immunotherapiebehandeling voor niet-vaste vormen van kanker zoals leukemie – die hebben geresulteerd in bijna wonderbaarlijke genezingen – is het vertalen van dit succes naar andere soorten kanker tot nu toe ongrijpbaar gebleven.
Nieuw onderzoek laat dat nu zien het veranderen van enkele kenmerken van deze gemodificeerde (chimere antigeenreceptoren of CAR) T-cellen kunnen de sleutel zijn om ze aanzienlijk langer te laten leven en effectiever te maken in het lichaam van een patiënt. Is dit de sleutel om immunotherapie voor nog veel meer kankersoorten mogelijk te maken?
Geen Twee Gelijk
Belangrijk om op te merken kanker is dat het niet de naam is voor een enkele ziekte, maar eerder de verzamelnaam voor een breed scala aan ziekten, die allemaal gepaard gaan met abnormale groei met het potentieel om binnen te dringen of zich te verspreiden (metastaseren) naar andere delen van het lichaam. Dit staat in contrast met dergelijke groei goedaardige tumoren, die nog steeds potentieel problematisch zijn als ze uiteindelijk druk uitoefenen op bloedvaten, zenuwen of organen, maar die voldoende gedifferentieerd zijn van het omringende weefsel om indien nodig operatief te kunnen worden verwijderd. Sommige van deze goedaardige tumoren kunnen later kwaadaardig worden. Daarom zijn zelfs zeer vaak voorkomende tumoren zoals a melanocytische naevus ('mol') moet op gelet worden bij eventuele wijzigingen.
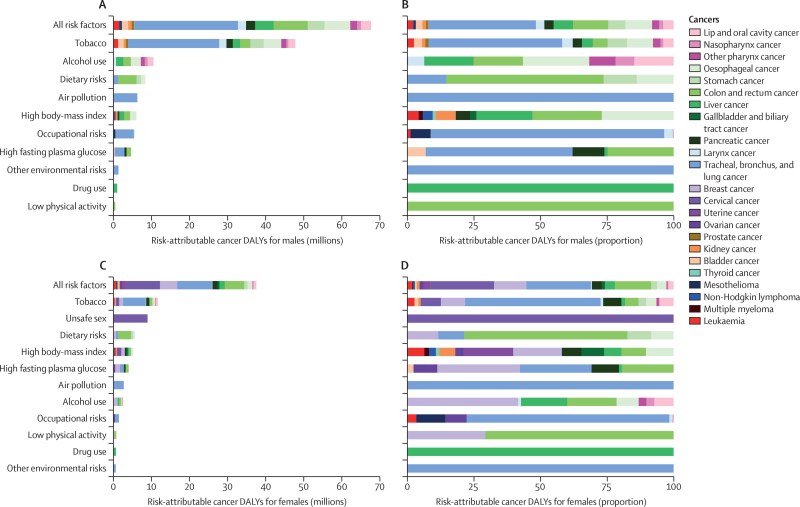
In het geval van een kwaadaardige tumor noemen we dit dus gezamenlijk 'kanker', die één of meer organen en/of weefseltypen in het lichaam kan aantasten. Er zijn veel redenen waarom een cel kanker kan krijgen, variërend van blootstelling aan kankerverwekkende stoffen, zoals aangetroffen in sigarettenrook, en andere vormen van vervuiling van de cel. bepaalde diëten, helemaal tot genetica (bijv. BRCA1- en BRCA2-mutaties voor borstkanker) en een virale infectie, evenals blootstelling aan hormonen en ioniserende straling. Sommige soorten kanker worden veroorzaakt door blootstelling aan minuscule inerte fysieke elementen, zoals asbest.
Met zoveel manieren waarop een kankergezwel kan ontstaan, is het misschien wel interessanter waarom we niet elke maand nieuwe kwaadaardige tumoren ontwikkelen. Hier zijn een aantal antwoorden op, waarbij zowel ingebouwde mechanismen in de lichaamscellen betrokken zijn die detecteren wanneer er iets niet in orde is, en op welk punt apoptose (geprogrammeerde celdood) zal worden geactiveerd. Apoptose kan ook extern worden geactiveerd met behulp van receptoren op het celmembraan waarmee een cytotoxische T-cel zich verbindt. Met behulp van deze intrinsieke en extrinsieke apoptoseroutes beëindigen cellen doorgaans zichzelf, of worden ze door het immuunsysteem van het lichaam als kwaadaardig geïdentificeerd en tot beëindiging aangezet.
Hoe komt het dan dat sommige kwaadaardige tumoren zich ongeacht deze mechanismen kunnen ontwikkelen?
T-cel-uitputting
Hoe effectief het adaptieve immuunsysteem van het lichaam ook is, het heeft een aantal zwakke punten. Eén daarvan is een fenomeen dat 'uitputting' wordt genoemd, waarbij chronische blootstelling aan antigeen zorgt ervoor dat T-cellen hun effectorfunctie verliezen en eerst overgaan in een ‘voorloper van uitgeput’ (TPEX) vorm vóór de terminale differentiatie in 'uitgeput' (TEX) formulier. De setPEX cellen kunnen dan niet meer vechten tegen de infectie of tumor (als T-effector, of TEFF), noch een T-effectorgeheugencel worden (TEM) later, noch produceren ze meer T-cellen. Omdat snelgroeiende kwaadaardige tumoren het lichaam waarschijnlijk zullen overspoelen met antigenen, is de kans groot dat een dergelijke uitputting zal optreden.
Hoewel TEFF cellen worden aangevuld door kerngeheugencellen (TCM) en nog minder gedifferentieerde stamgeheugencellen (TSCM), is dit niet voldoende om de kankercellen tegen te gaan. Dit verklaart zowel waarom een kwaadaardige tumor zich soms vrijwel ongehinderd kan ontwikkelen als waarom op T-cellen gebaseerde immuuntherapieën weinig succes hebben gehad bij de behandeling van solide kankers, omdat er simpelweg niet genoeg actieve T-cellen zijn.EFF cellen aanwezig.
Dit roept de vraag op waarom er sprake is van uitputting van T-cellen, en of het uitschakelen van dit mechanisme in geselecteerde T-cellen een oplossing zou kunnen bieden.
Epigenetische expressies
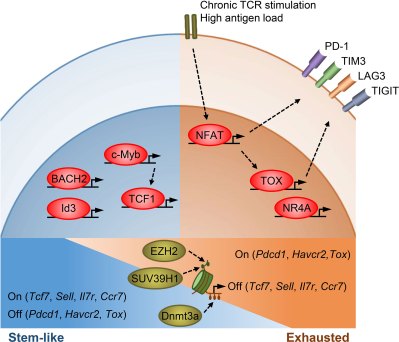
Het mechanisme dat TEFF cellen is die van epigenetica, specifiek door de methylering van het DNA van de cel, vergelijkbaar met de door methylering geïnduceerde veroudering van de lichaamscellen als geheel, een factor waarvan is aangetoond dat deze ook een belangrijke rol speelt bij het ontstaan van tumoren. Zoals voorgesteld door Enyong Dai en collega's in Moleculaire kankerzouden preventieve therapieën tegen kanker epigenetische geneesmiddelen kunnen omvatten die dergelijke onderliggende epigenetische veranderingen zouden aanpakken, naast de directe behandeling van bestaande kwaadaardige tumoren.
Epigenetica is een essentieel onderdeel van het cellulaire functioneren, waaronder DNA-methylatie en structurele elementen zoals chromatine en histonen, door genetische expressie te reguleren. Het maakt ook evolutionaire veranderingen op generatieniveau mogelijk, aangezien aspecten als methylatie erfelijk zijn. Hier is DNA-methylatie ook het meest relevant in de manier waarop het het individu rechtstreeks beïnvloedt, vooral omdat het betrekking heeft op TEFF cellen.
Zoals beschreven door Xuechen Yin en collega's in a 2023 overzichtsartikel in Immunologie, TEX cellen worden gekenmerkt door overexpressie van remmende receptoren (zoals geprogrammeerde dood-1, of PD-1), met TPEX cellen kunnen nieuw leven worden ingeblazen door deze receptoren te blokkeren. Bovendien werd CRISPR-Cas9 gebruikt om PD-1 knock-out CAR T-cellen te creëren, die significant betere prestaties vertoonden tegen solide tumoren. Hier heeft een potentieel doelwit al langer bekend, in de vorm van methylering van histon 3 lysine 9 (H3K9) en het effect ervan op het moduleren van immuunceldifferentiatie en immuunrespons. Dit epigenetische kenmerk heeft dus een grote invloed op de uitkomst van gebeurtenissen waarbij het immuunsysteem betrokken is.
De rol van histonmethylering bij immunotherapie gericht op tumoren werd in detail besproken door Yuanling Zhang en collega's in een overzichtsartikel uit januari 2023 in Grenzen in immunologie, dat een overzicht geeft van de verschillende routes binnen zowel T-cellen als kwaadaardige tumorcellen die immunotherapie beïnvloeden. Eén daarvan is het gen SUV39H1, dat de methylering van H3K9me3 beïnvloedt en de moord- en geheugenfuncties van TEFF cellen.
Misschien niet verrassend, het is exact dit SUV39H1-gen waarop Nayan Jain en collega's in dit nieuwste onderzoek, zoals eerder vermeld, zich richtten toen ze CRISPR-Cas9 gebruikten om SUV39H1 knock-out CAR T-cellen te creëren. In onderzoeken werden deze knock-out CAR T-cellen herhaaldelijk uitgedaagd met antigenen, maar vertoonden ze niet de gebruikelijke tekenen van verandering van T-cellen.EFF cellen in TPEX of TEX cellen. In feite lijkt dit op zijn minst de meest effectieve routes te hebben verwijderd waarlangs T-cellen uitgeput kunnen raken, en proeven met muizen hebben bemoedigende resultaten opgeleverd.
Een lange maar veelbelovende weg
Hoewel immunotherapie een goedgekeurde therapie voor een aantal vormen van kanker, zoals leukemie, is het probleem van de uitputting van T-cellen tot nu toe een van de belangrijkste obstakels geweest bij het bredere gebruik ervan. Nu klinische onderzoeken met SUV39H1 knock-out CAR T-cellen op dit moment een duidelijke mogelijkheid zijn, kan het slechts een kwestie van jaren zijn voordat we de effecten van deze specifieke aanpak met CAR T-immunotherapie beginnen te zien.
Misschien is het niet zo verrassend dat we, omdat sciencefictionliteratuur en films vaak verwijzen naar 'medische nanobots', op dit punt terechtkomen waar we ons best zouden doen om de nanomachines die al in ons eigen lichaam bestaan, te reverse-engineeren. Met dank aan een snelgroeiende hoeveelheid medische literatuur en geavanceerde hulpmiddelen voor het bewerken van genen, kunnen we vandaag de dag dromen van geneeswijzen en therapieën die nog maar een paar decennia geleden de puurste sciencefiction zouden hebben geleken.
Met hoe vreselijk kanker is en hoeveel levens het elke dag eist, lijkt het bijna verkeerd om je een wereld voor te stellen waarin elke vorm van kanker niet alleen behandelbaar is, maar ook te genezen door middel van routinematige immunotherapie. Toch zou dit de toekomst kunnen zijn waar we ons nu op bevinden.
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoData.Network Verticale generatieve AI. Versterk jezelf. Toegang hier.
- PlatoAiStream. Web3-intelligentie. Kennis versterkt. Toegang hier.
- PlatoESG. carbon, CleanTech, Energie, Milieu, Zonne, Afvalbeheer. Toegang hier.
- Plato Gezondheid. Intelligentie op het gebied van biotech en klinische proeven. Toegang hier.
- Bron: https://hackaday.com/2023/11/27/car-t-cell-immunotherapy-and-the-quiet-hope-for-a-universal-cancer-treatment/



