Antibiotica hebben talloze levens gered en zijn een cruciaal hulpmiddel in de moderne geneeskunde. Maar we verliezen terrein in onze strijd tegen bacteriën. Halverwege de vorige eeuw wetenschappers ontdekte geheel nieuwe klassen antibiotica. Sindsdien is het tempo van de ontdekkingen afgenomen tot een straaltje, en is de prevalentie van antibioticaresistente bacteriën toegenomen.
Er zijn waarschijnlijk nog antibiotica die ontdekt moeten worden, maar het chemische universum is te groot om door iemand te worden onderzocht. De afgelopen jaren hebben wetenschappers zich tot AI gewend. Machine learning-algoritmen kunnen enorme aantallen potentiële chemische configuraties terugbrengen tot een handvol veelbelovende kandidaten om te testen.
Tot nu toe hebben wetenschappers AI gebruikt om afzonderlijke verbindingen met antibiotische eigenschappen te vinden. Maar in een nieuwe studie gisteren gepubliceerd in NATUURMIT-onderzoekers zeggen dat ze een systeem hebben gebouwd en getest dat hele nieuwe klassen antibiotica kan identificeren en kan voorspellen welke waarschijnlijk veilig zijn voor mensen.
De AI doorzocht meer dan 12 miljoen verbindingen en vond een onontdekte klasse antibiotica die bij muizen effectief bleek te zijn tegen de methicilline-resistente Staphylococcus aureus (MRSA), een dodelijke stam van medicijnresistente insecten.
Hoewel deze door AI ontdekte antibiotica nog steeds moeten bewijzen dat ze veilig en effectief zijn bij mensen door de standaardhandschoen van klinische tests te doorstaan, gelooft het team dat hun werk de ontdekking aan de voorkant kan versnellen en hopelijk ons algehele trefferpercentage kan verhogen.
Het verkennen van de drugsruimte
Wetenschappers gebruiken steeds vaker AI-sidekicks om het ontdekkingsproces te versnellen. Het meest bekend is misschien wel AlphaFold van DeepMind, een machinaal leerprogramma dat de vormen van eiwitten, de fundamentele bouwstenen van ons lichaam, kan modelleren. Het idee is dat AlphaFold en zijn nakomelingen het moeizame proces van geneesmiddelenonderzoek kunnen versnellen. Hun overtuiging is zo sterk dat DeepMind in 2021 een dochteronderneming heeft opgericht, Isomorfe Labs, toegewijd om precies dat te doen.
Andere AI-benaderingen zijn ook veelbelovend gebleken. Vooral een MIT-groep heeft zich gefocust op de ontwikkeling van geheel nieuwe antibiotica om superbacteriën te bestrijden. Hun eerste onderzoek, gepubliceerd in 2020, toonde aan dat deze aanpak zou kunnen werken, toen ze halicine vonden, een voorheen onontdekt antibioticum dat zouden medicijnresistente E. coli gemakkelijk kunnen uitschakelen.
In een vervolgonderzoek eerder dit jaar richtte het team zich op Acinetobacter baumannii, “publieke vijand nr. 1 voor multiresistente bacteriële infecties”, aldus Jonathan Stokes van McMaster University, een senior auteur van het onderzoek.
“Acinetobacter kan lange tijd overleven op de deurknoppen en apparatuur van ziekenhuizen, en kan antibioticaresistentiegenen uit zijn omgeving opnemen. Het is nu heel gebruikelijk om isolaten van A. baumannii te vinden die resistent zijn tegen bijna elk antibioticum,” Stokes zei destijds.
Na in slechts twee uur 6,680 verbindingen te hebben doorzocht, bracht de AI een paar honderd veelbelovende kandidaten naar voren. Het team testte er 240 van, die structureel verschilden van de bestaande antibiotica. Ze vonden negen veelbelovende kandidaten, waaronder één, abaucin, die behoorlijk effectief was tegen A. baumannii.
Uit beide onderzoeken bleek dat de aanpak zou kunnen werken, maar slechts enkele kandidaten opleverde zonder informatie daarover Waarom ze waren effectief. Machine learning-algoritmen zijn notoir zwarte dozen; wat er ‘tussen de oren’ gebeurt, is vaak een compleet mysterie.
In het laatste onderzoek richtte de groep zich op een andere bekende tegenstander, MRSA, maar deze keer koppelden ze verschillende algoritmen aan elkaar om de resultaten te verbeteren en de redenering van de AI beter te verhelderen.
De schakelaar omzetten
De nieuwste antibiotische bloedhond van het team trainde op zo’n 39,000 verbindingen, inclusief hun chemische structuur en het vermogen om MRSA te doden. Ze trainden ook afzonderlijke modellen om de toxiciteit van een bepaalde stof voor menselijke cellen te voorspellen.
“Je kunt in principe elk molecuul als een chemische structuur weergeven, en je kunt het model ook vertellen of die chemische structuur antibacterieel is of niet”, zegt Felix Wong, een postdoc bij IMES en het Broad Institute of MIT en Harvard, vertelde MIT News. “Het model is getraind op veel van dit soort voorbeelden. Als je het vervolgens een nieuw molecuul geeft, een nieuwe rangschikking van atomen en bindingen, kan het je de waarschijnlijkheid vertellen dat die verbinding naar verwachting antibacterieel is.’
Eenmaal voltooid, heeft het team meer dan 12 miljoen verbindingen in het systeem ingevoerd. De AI heeft deze enorme lijst teruggebracht tot ongeveer 3,600 verbindingen, onderverdeeld in vijf klassen – op basis van hun structuren – waarvan zij voorspelde dat ze enige activiteit tegen MRSA zouden hebben en minimaal giftig zouden zijn voor menselijke cellen. Het team kwam tot een definitieve lijst van 283 kandidaten om te testen.
Hiervan vonden ze er twee uit dezelfde klasse – dat wil zeggen, ze hadden vergelijkbare structurele componenten waarvan werd aangenomen dat ze bijdroegen aan de antimicrobiële activiteit – die behoorlijk effectief waren. Bij muizen bestreden de antibiotica zowel een huidinfectie als een systemische infectie door 90 procent van de aanwezige MRSA-bacteriën uit te schakelen.
Terwijl hun eerdere werk Gram-negatieve bacteriën aanpakte door celmembranen te verstoren, is MRSA Gram-positief en heeft het dikkere wanden.
"We hebben behoorlijk sterk bewijs dat deze nieuwe structurele klasse actief is tegen Gram-positieve pathogenen door selectief de protonaandrijfkracht in bacteriën te dissiperen," zei Wong. “De moleculen vallen selectief bacteriële celmembranen aan, op een manier die geen substantiële schade aan menselijke celmembranen veroorzaakt.”
Door hun AI verklaarbaar te maken, hoopt het team zich te richten op structuren die toekomstige zoekopdrachten kunnen informeren of kunnen bijdragen aan het ontwerp van effectievere antibiotica in het laboratorium.
Eindexamens
Het belangrijkste om op te merken is dat, hoewel het erop lijkt dat de nieuwe antibiotica op zeer kleine schaal effectief waren bij muizen, er nog een lange weg te gaan is voordat je er een voorgeschreven krijgt.
Nieuwe medicijnen ondergaan strenge tests en klinische onderzoeken, en veel, zelfs veelbelovende kandidaten, halen de andere kant niet. Het gebied van AI-ondersteunde geneesmiddelenontdekking is dat in het algemeen wel op dit gebied nog in de beginfase. De eerste Door AI ontworpen medicijnen bevinden zich nu in klinische onderzoeken, maar er is nog geen goedgekeurd.
Toch is de hoop gevestigd op een snellere bevoorrading van de pijplijn met betere kandidaten.
Het kan drie tot zes jaar duren voordat een nieuw antibioticum wordt ontdekt dat geschikt is voor klinische onderzoeken. volgens de Universiteit van Pennsylvania Cesar de la Fuente, wiens laboratorium soortgelijk werk doet. Dan heb je de beproevingen zelf. Nu de resistentie tegen antibiotica toeneemt, hebben we dat soort tijd misschien niet meer, om nog maar te zwijgen van het feit dat antibiotica niet het rendement op de investering opleveren dat andere medicijnen wel hebben. Alle hulp is welkom.
“Nu hebben we met machines de tijdlijn kunnen versnellen,” de la Fuente vertelde Scientific American. “In het eigen werk van mij en mijn collega’s kunnen we bijvoorbeeld binnen enkele uren duizenden of honderdduizenden preklinische kandidaten ontdekken in plaats van drie tot zes jaar te moeten wachten. Ik denk dat AI dat in het algemeen mogelijk heeft gemaakt.”
Het is nog vroeg, maar als de door AI ontdekte antibiotica de komende jaren hun waarde bewijzen, kunnen we misschien de overhand behouden in onze al lang bestaande strijd tegen bacteriën.
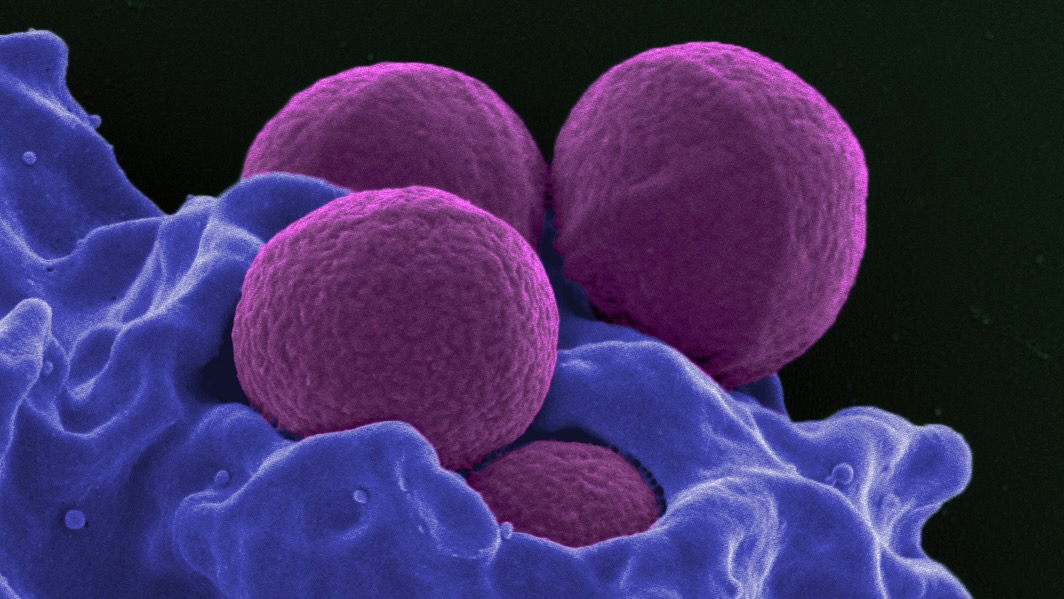
Krediet van het beeld: Een menselijke witte bloedcel die MRSA (paars) opneemt / National Institute of Allergy and Infectious Diseases, National Institutes of Health
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoData.Network Verticale generatieve AI. Versterk jezelf. Toegang hier.
- PlatoAiStream. Web3-intelligentie. Kennis versterkt. Toegang hier.
- PlatoESG. carbon, CleanTech, Energie, Milieu, Zonne, Afvalbeheer. Toegang hier.
- Plato Gezondheid. Intelligentie op het gebied van biotech en klinische proeven. Toegang hier.
- Bron: https://singularityhub.com/2023/12/21/ai-discovers-a-new-class-of-antibiotics-after-scouring-12-million-compounds/



