(나노 워크 뉴스) 연구자들은 DNA 및 기타 생물학적 나노입자를 정밀하게 조작하고 식별할 수 있는 다용도 도구를 개발하기 위해 오랫동안 노력해 왔습니다. 작은 입자를 포착하기 위해 레이저를 사용하는 광학 핀셋은 비접촉식 제어 기능을 제공하지만 특정 DNA 서열을 인식하는 기능이 부족했습니다.
동시에 CRISPR 유전자 편집은 매우 민감한 검출 방법으로 등장했지만 다음과 같은 개선과 통합이 필요합니다. 나노 기술. 이제 선전대학교와 홍콩중문대학교의 연구자들은 CRISPR를 광열 핀셋과 결합하여 이전의 한계를 극복하는 혁신을 이루었습니다.
에 발표된 새로운 연구에서 빛 : 과학 및 응용 ("CRISPR 기반 광열 나노핀셋: 다양한 바이오 나노입자 조작 및 단일 뉴클레오티드 식별"), 팀은 높은 정확도로 DNA를 동시에 포착하고 식별할 수 있는 플랫폼인 CRISPR 기반 광열 나노핀셋(CRONT)을 제시합니다. 이 획기적인 발전은 현장 검사, 바이오센싱 및 기초 생물물리학 연구의 발전을 위한 길을 열어줍니다.
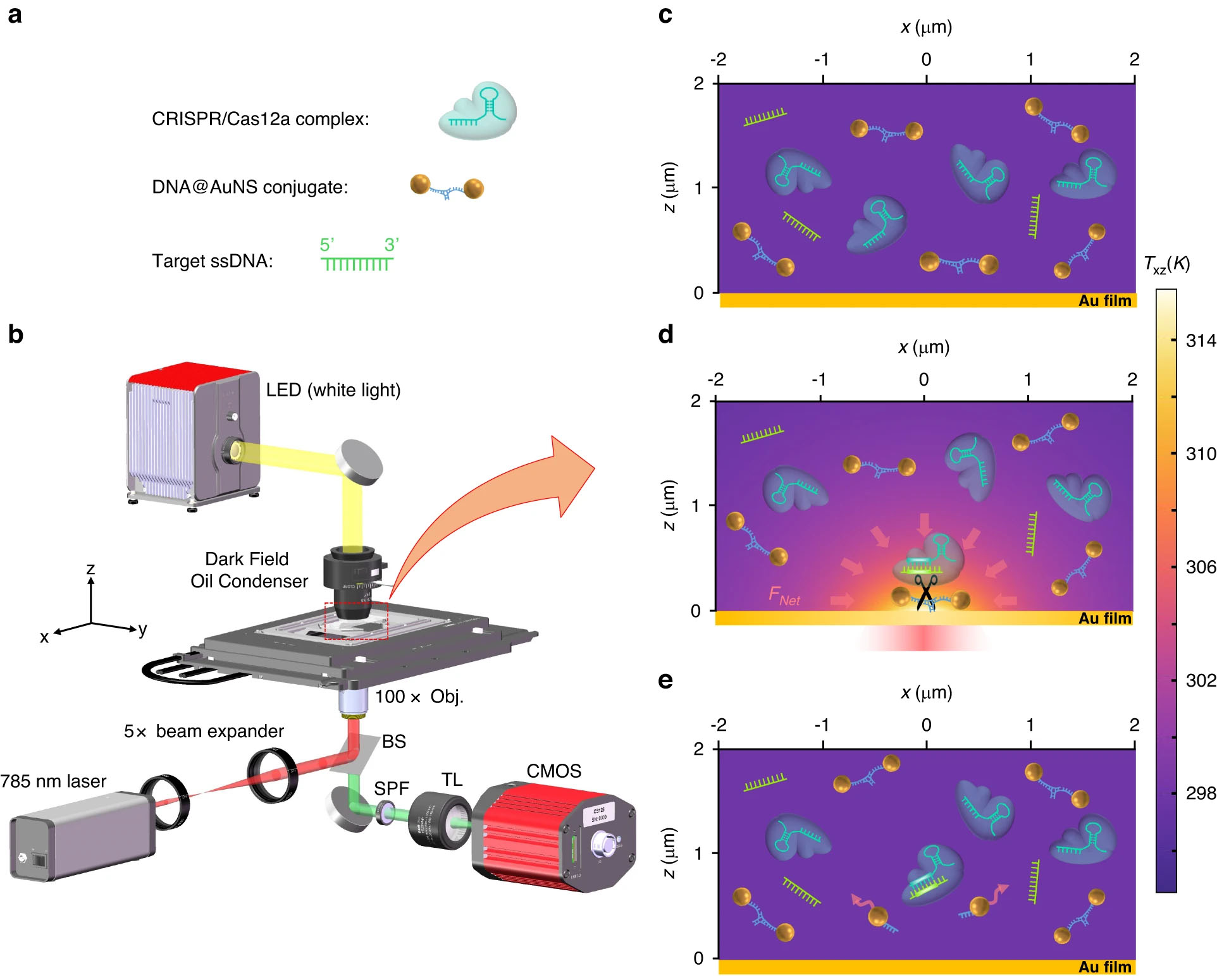 CRISPR 기반 광열 나노핀셋의 작동 원리. a 솔루션의 세 가지 구성 요소인 DNA@AuNS 접합체, CRISPR/Cas12a 복합체 및 대상 ssDNA의 도식적 스케치. b 광학 설정, BS, SPF 및 TL은 각각 빔 분할기, 단거리 통과 필터 및 튜브 렌즈(f=200mm)입니다. 설정에 대한 추가 세부 사항은 재료 및 방법 섹션에 제공됩니다. c 광학적 가열 없이 용액에 세 가지 성분을 분산시킵니다. d 광열 순 힘(F그물) 광학 가열 시 유도된 이동 및 DNA@AuNS 접합 절단, 가열 레이저 출력은 0.5mW입니다. e 광학 가열이 꺼진 후 분열 관찰. (© 빛: 과학 및 응용)
광학 핀셋 1986년 발명된 이래로 미세한 입자에 대한 비교할 수 없는 시공간 제어를 제공하는 매우 귀중한 기술이 되었습니다. 그러나 그들은 집중된 고출력 레이저의 운동량 전달에 의존하여 갇힐 수 있는 물질을 제한하고 국소 가열로 인한 광손상 위험을 초래합니다.
광열 핀셋은 훨씬 낮은 강도의 유망한 대안으로 15년 전에 소개되었습니다. 그들은 열확산과 대류력을 통해 입자를 조작하기 위해 빛을 흡수하는 표면 근처의 미세한 온도 구배와 유체 흐름을 활용합니다. 그러나 지금까지 전통적인 광학 핀셋과 광열 기술 모두 광학 신호를 사용하여 생물학적 입자를 직접 식별할 수 없었습니다. 이러한 기능은 번거로운 형광 태깅 방법을 통해서만 달성되었습니다.
이와 동시에 CRISPR 진단은 단일 염기쌍까지 극도의 특이성을 지닌 핵산 서열을 검출하는 획기적인 접근 방식이 되었습니다. 그러나 광범위한 샘플 준비와 필요한 표적 증폭으로 인해 벤치탑 분석을 현장 진료 장치로 전환하는 것은 여전히 어려운 일입니다. Shenzhen-CUHK 팀은 하나의 플랫폼에서 광열 핀셋의 정확한 조작과 CRISPR 감지를 융합하는 엄청난 잠재력을 깨달았습니다.
CRONT 시스템은 얇은 금 필름을 사용하여 표준 785 nm 레이저 포인터로 조명할 때 실온 바로 위의 가열 지점을 생성합니다. 이는 50개 이상의 서로 다른 DNA 서열을 선택적으로 포착할 수 있는 국부적인 대류 전류와 열확산을 생성합니다. 나노 입자 DNA로 기능화. 일단 갇히면, 표적 DNA 가닥을 절단하는 CRISPR 복합체를 도입하여 서열이 현장에서 식별되며, 단편화 시 개별 금 나노입자의 회절 패턴이 변경됨에 따라 실시간으로 관찰됩니다. 이 수동 광학 판독은 번거로운 형광 태깅 단계를 방지합니다.
놀랍게도, 이러한 자가 조립력을 활용하고 미세한 열 유도 흐름 내에 CRISPR 프로브를 통합함으로써 CRONT 핀셋은 농도와 상호 작용 속도를 높여 신속한 단일 DNA 검출을 가능하게 합니다. 연구팀은 표적 증폭 없이 원숭이폭스 바이러스의 염기서열에 대해 원자몰 민감도를 보여주었습니다. 이는 기존 CRISPR 분석에 비해 최대 10억 배 향상된 성능을 나타내며 PCR 수준 성능과 일치합니다. 저가형 레이저 핀셋 시스템의 이러한 초고감도 정량화는 현장 진료 테스트를 가능하게 할 수 있습니다.
마찬가지로 CRONT 핀셋은 이전에는 고가의 시퀀싱이나 PCR 플랫폼으로만 제한되었던 기능인 단일 염기 다형성(SNP) 인식을 용이하게 합니다. 이는 생물 다양성이나 질병 메커니즘을 연구하기 위해 유전적 다양성과 현장 돌연변이를 광학적으로 프로파일링할 수 있는 가능성을 열어줍니다. 실험적 검증에 따르면 CRONT는 SARS-CoV-2 변종 간의 단일 염기 차이를 구별할 수 있는 것으로 나타났습니다.
핵산 외에도 연구자들은 프로그래밍 가능한 단백질 조작을 시연하여 열 유발 단백질 상호 작용 연구에 대한 흥미로운 전망을 제시했습니다. 그리고 그들은 다양한 프로브를 사용한 기능화를 통해 플랫폼을 다양한 재료로 확장할 수 있다고 지적합니다.
CRISPR 분석과 광열 조작의 장점을 결합하여 여전히 개념 증명이기는 하지만 CRONT 핀셋은 두 기술을 독립적으로 가로막는 주요 장벽을 극복합니다. 팀은 이것이 현장 바이오센서, 질병 검사, 원격 세포 조작 및 통합을 향한 중요한 단계라고 믿습니다. 나노포토닉스 프로그래밍 가능한 생물학적 상호 작용을 통해. 그들은 유전체학, 후성유전학, 진단 전반에 걸쳐 연구 및 탐지를 가속화하기 위해 처리량을 더욱 향상시킬 계획입니다.
기술이 발전함에 따라 감도와 단순성이 유지될 수 있다면 CRISPR 기반 광열 핀셋은 실험실 및 임상 분석을 위한 유비쿼터스 도구가 되어 고급 나노기술을 실제 생물의학에 도입할 수 있습니다.
CRISPR 기반 광열 나노핀셋의 작동 원리. a 솔루션의 세 가지 구성 요소인 DNA@AuNS 접합체, CRISPR/Cas12a 복합체 및 대상 ssDNA의 도식적 스케치. b 광학 설정, BS, SPF 및 TL은 각각 빔 분할기, 단거리 통과 필터 및 튜브 렌즈(f=200mm)입니다. 설정에 대한 추가 세부 사항은 재료 및 방법 섹션에 제공됩니다. c 광학적 가열 없이 용액에 세 가지 성분을 분산시킵니다. d 광열 순 힘(F그물) 광학 가열 시 유도된 이동 및 DNA@AuNS 접합 절단, 가열 레이저 출력은 0.5mW입니다. e 광학 가열이 꺼진 후 분열 관찰. (© 빛: 과학 및 응용)
광학 핀셋 1986년 발명된 이래로 미세한 입자에 대한 비교할 수 없는 시공간 제어를 제공하는 매우 귀중한 기술이 되었습니다. 그러나 그들은 집중된 고출력 레이저의 운동량 전달에 의존하여 갇힐 수 있는 물질을 제한하고 국소 가열로 인한 광손상 위험을 초래합니다.
광열 핀셋은 훨씬 낮은 강도의 유망한 대안으로 15년 전에 소개되었습니다. 그들은 열확산과 대류력을 통해 입자를 조작하기 위해 빛을 흡수하는 표면 근처의 미세한 온도 구배와 유체 흐름을 활용합니다. 그러나 지금까지 전통적인 광학 핀셋과 광열 기술 모두 광학 신호를 사용하여 생물학적 입자를 직접 식별할 수 없었습니다. 이러한 기능은 번거로운 형광 태깅 방법을 통해서만 달성되었습니다.
이와 동시에 CRISPR 진단은 단일 염기쌍까지 극도의 특이성을 지닌 핵산 서열을 검출하는 획기적인 접근 방식이 되었습니다. 그러나 광범위한 샘플 준비와 필요한 표적 증폭으로 인해 벤치탑 분석을 현장 진료 장치로 전환하는 것은 여전히 어려운 일입니다. Shenzhen-CUHK 팀은 하나의 플랫폼에서 광열 핀셋의 정확한 조작과 CRISPR 감지를 융합하는 엄청난 잠재력을 깨달았습니다.
CRONT 시스템은 얇은 금 필름을 사용하여 표준 785 nm 레이저 포인터로 조명할 때 실온 바로 위의 가열 지점을 생성합니다. 이는 50개 이상의 서로 다른 DNA 서열을 선택적으로 포착할 수 있는 국부적인 대류 전류와 열확산을 생성합니다. 나노 입자 DNA로 기능화. 일단 갇히면, 표적 DNA 가닥을 절단하는 CRISPR 복합체를 도입하여 서열이 현장에서 식별되며, 단편화 시 개별 금 나노입자의 회절 패턴이 변경됨에 따라 실시간으로 관찰됩니다. 이 수동 광학 판독은 번거로운 형광 태깅 단계를 방지합니다.
놀랍게도, 이러한 자가 조립력을 활용하고 미세한 열 유도 흐름 내에 CRISPR 프로브를 통합함으로써 CRONT 핀셋은 농도와 상호 작용 속도를 높여 신속한 단일 DNA 검출을 가능하게 합니다. 연구팀은 표적 증폭 없이 원숭이폭스 바이러스의 염기서열에 대해 원자몰 민감도를 보여주었습니다. 이는 기존 CRISPR 분석에 비해 최대 10억 배 향상된 성능을 나타내며 PCR 수준 성능과 일치합니다. 저가형 레이저 핀셋 시스템의 이러한 초고감도 정량화는 현장 진료 테스트를 가능하게 할 수 있습니다.
마찬가지로 CRONT 핀셋은 이전에는 고가의 시퀀싱이나 PCR 플랫폼으로만 제한되었던 기능인 단일 염기 다형성(SNP) 인식을 용이하게 합니다. 이는 생물 다양성이나 질병 메커니즘을 연구하기 위해 유전적 다양성과 현장 돌연변이를 광학적으로 프로파일링할 수 있는 가능성을 열어줍니다. 실험적 검증에 따르면 CRONT는 SARS-CoV-2 변종 간의 단일 염기 차이를 구별할 수 있는 것으로 나타났습니다.
핵산 외에도 연구자들은 프로그래밍 가능한 단백질 조작을 시연하여 열 유발 단백질 상호 작용 연구에 대한 흥미로운 전망을 제시했습니다. 그리고 그들은 다양한 프로브를 사용한 기능화를 통해 플랫폼을 다양한 재료로 확장할 수 있다고 지적합니다.
CRISPR 분석과 광열 조작의 장점을 결합하여 여전히 개념 증명이기는 하지만 CRONT 핀셋은 두 기술을 독립적으로 가로막는 주요 장벽을 극복합니다. 팀은 이것이 현장 바이오센서, 질병 검사, 원격 세포 조작 및 통합을 향한 중요한 단계라고 믿습니다. 나노포토닉스 프로그래밍 가능한 생물학적 상호 작용을 통해. 그들은 유전체학, 후성유전학, 진단 전반에 걸쳐 연구 및 탐지를 가속화하기 위해 처리량을 더욱 향상시킬 계획입니다.
기술이 발전함에 따라 감도와 단순성이 유지될 수 있다면 CRISPR 기반 광열 핀셋은 실험실 및 임상 분석을 위한 유비쿼터스 도구가 되어 고급 나노기술을 실제 생물의학에 도입할 수 있습니다.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 출처: https://www.nanowerk.com/nanotechnology-news2/newsid=64221.php



