이에 대한 고무적인 데이터가 꾸준히 유입되어 왔습니다. MS용 줄기세포. 특히 특정 종류의 MS의 경우.
새로운 연구가 이러한 낙관적인 방향에 추가되었습니다.
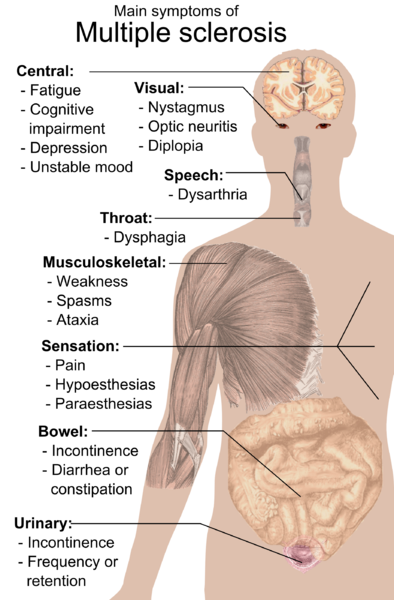
다발성 경화증(MS) 줄기세포에 대한 좋은 소식
스웨덴의 재발성 다발성 경화증 치료를 위한 조혈 줄기 세포 이식: 관찰 코호트 연구, 신경학, 신경외과, 정신의학 저널.
이 논문은 다른 그룹의 결과와 일치합니다. 조혈모세포이식 일부 MS 환자에게는 큰 이점이 있는 것으로 보입니다. 여기서 저자는 “RRMS에 대한 aHSCT 치료는 대부분의 환자에서 허용 가능한 부작용과 함께 질병 활동이 없는 것과 관련이 있습니다. 이 절차는 활성도가 높은 RRMS 환자를 위한 표준 치료로 간주되어야 합니다.”
다발성 경화증(MS)의 줄기 세포가 많은 사례에서 입증된 치료 표준이 된다면 상상해 보십시오. 정말 놀라울 거예요. 나는 특히 미국 이외의 일부 의사들이 이미 그것을 그렇게 보고 있다는 것을 알고 있습니다.
코로나XNUMX를 위한 Kimera Labs IND
엑소좀 제품을 제조하는 키메라랩스는 지난 XNUMX월 FDA로부터 좋은 소식을 받았습니다. 회사는 처음으로 승인된 IND를 받았습니다. 이 경우에는 조사를 위한 것입니다. 코로나XNUMX에 대한 엑소좀 치료법.
나는 이 IND 뉴스를 놓쳤습니다. 아마도 XNUMX월/XNUMX월 초에 XNUMX개의 NIH 보조금을 제출했고 XNUMX월 중순부터 심한 코로나 바이러스 사례를 겪었기 때문일 것입니다. 나는 팔로우해왔다 키메라 연구소 오랫동안. 이 IND와 후속 시험 데이터를 추적하는 것은 흥미로울 것입니다. 이번 IND는 특히 코로나XNUMX에 대한 제품 사용과 관련된 최악의 팬데믹 상황에서 FDA가 키메라에게 제목 없는 편지를 보냈다는 점에서 주목할 만합니다.
해당 기관은 또한 더글러스 스필(Douglas Spiel) 박사에게 코로나XNUMX 환자에 대한 엑소좀 사용에 대해 경고를 보냈습니다. Spiel은 Kimera의 임상 컨설턴트였지만 몇 년 동안 회사에서 직책을 맡지 않았습니다.
FDA – Cell Surgical Network 소송 항소
우리는 아마도 계류 중인 대규모 줄기 세포 소송 항소에 대해 훨씬 더 인내심을 가져야 할 것입니다.

FDA는 지방 세포 제품인 SVF가 약물인지 여부와 기타 문제에 대해 여기 캘리포니아에서 열린 연방 지방 법원 소송에서 패소했습니다. 플로리다에서도 비슷한 소송에서 승리했습니다.
이제 캘리포니아 SVF 사례는 세포외과네트워크 소송, The Ninth Circuit님이 있습니다. 이것은 아마도 결정되기 전에 2024년으로 밀릴 것입니다. 왜? 업데이트를 통해 현재 사건 목록에는 2024년 XNUMX월 구두 변론 가능성이 논의되어 있습니다. 당사자들이 독립적으로 사건을 해결할 수 없다면 이 사건은 매우 오랜 시간이 걸릴 것입니다.
왜 패서디나인가? 샌프란시스코에 있을 줄 알았는데.
기타 추천 도서
미만성 정중선 신경교종이 있는 성인의 H3K27M 표적 백신, Nat. Med. 이는 매우 예비적이라 할지라도 희망적이다. 특히 한 환자의 강한 반응이 흥미로웠습니다.
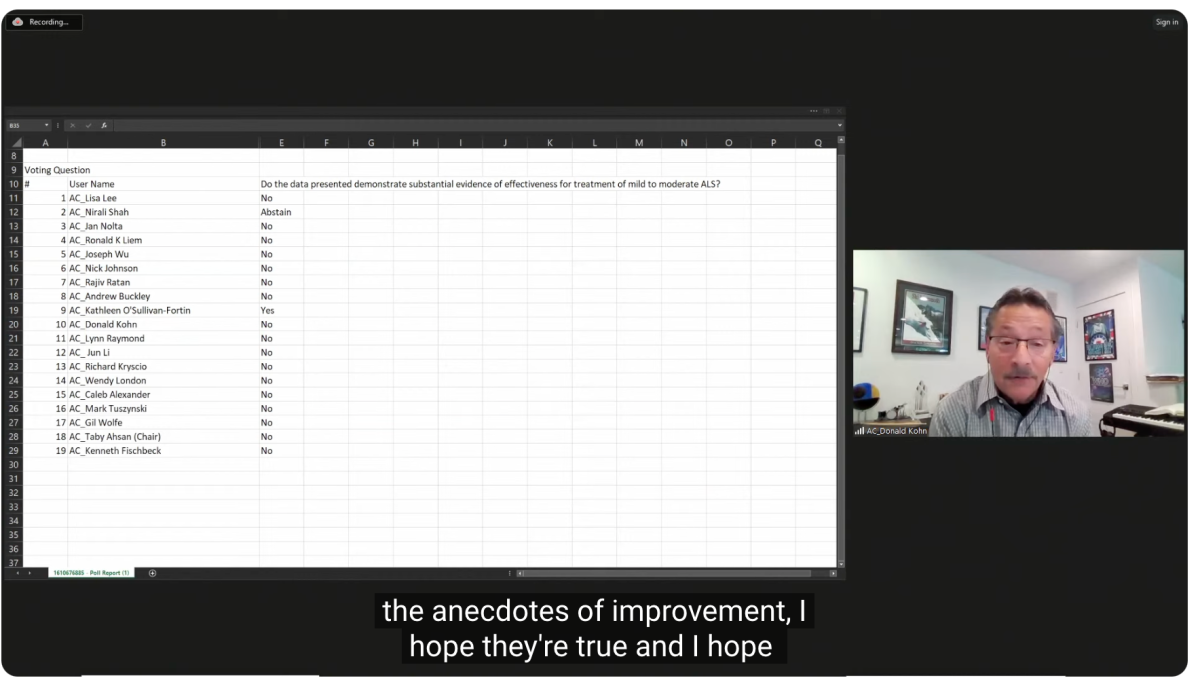
FDA 자문위원회는 다음과 같은 항소 유형의 노력을 거부했습니다. BrainStorm 세포 치료제 ALS를 위한 Nurown 제품.
패널회의를 조금 봤는데 상당히 부정적이었습니다. 그들은 데이터에 대한 큰 우려뿐 아니라 제품이 어떻게 작동해야 하는지에 대해서도 알지 못했습니다. 몇몇 위원회 위원들은 Nurown이 일부 환자에게 해를 끼칠 가능성도 있다고 말했습니다.
결국 단 한 명만이 '찬성'에 투표했고, XNUMX명은 '아니오'에 투표했고, 한 명은 기권했습니다. 위 영상에서 투표를 게시했습니다. 나는 최근에 회사의 이러한 노력을 어떻게 보았는지에 대해 썼습니다. 우박 메리. FDA는 이제 XNUMX월 초까지 최종 결정을 내려야 합니다. 현재로서는 Nurown이 앞으로 나아갈 가능성은 거의 없어 보입니다.
Neuron은 또한 MS에 대한 임상 시험을 진행했으며 MS 종류의 접근 방식에 대한 또 다른 가능한 줄기 세포를 나타내지만 지금까지의 데이터는 그다지 고무적이지 않았습니다.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoData.Network 수직 생성 Ai. 자신에게 권한을 부여하십시오. 여기에서 액세스하십시오.
- PlatoAiStream. 웹3 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 플라톤ESG. 탄소, 클린테크, 에너지, 환경, 태양광, 폐기물 관리. 여기에서 액세스하십시오.
- PlatoHealth. 생명 공학 및 임상 시험 인텔리전스. 여기에서 액세스하십시오.
- 출처: https://ipscell.com/2023/10/weekly-reads-stem-cells-for-ms-kimera-labs-ind-fda-lawsuit/



