تتطلب إصابات الدماغ المؤلمة (TBI)، الناجمة عن هزة مفاجئة أو تأثير على الرأس، التشخيص في أسرع وقت ممكن. ولمنع الضرر الذي لا يمكن إصلاحه، يجب اتخاذ قرارات العلاج الحرجة للحياة خلال "الساعة الذهبية" بعد الصدمة. من الصعب تشخيص إصابات الدماغ الرضية في نقطة الرعاية، ولكن الاعتماد على ملاحظات أطقم الإسعاف تليها التحقيقات الإشعاعية مثل التصوير بالرنين المغناطيسي أو الأشعة المقطعية عند الوصول إلى المستشفى.
لتمكين التدخل في الوقت المناسب، الباحثون من جامعة برمنغهام يقومون بتطوير جهاز تشخيصي محمول يكتشف إصابات الدماغ الرضية عن طريق تسليط ليزر آمن على العين. الجهاز موضح في علم السلف، مُستهدف للاستخدام بمجرد حدوث الإصابة - سواء على جانب الطريق أو في ساحة المعركة أو في الملعب الرياضي - لتقييم مرضى إصابات الدماغ الرضية، وتحديد مدى خطورة الصدمة والعلاج المباشر وفقًا لذلك.
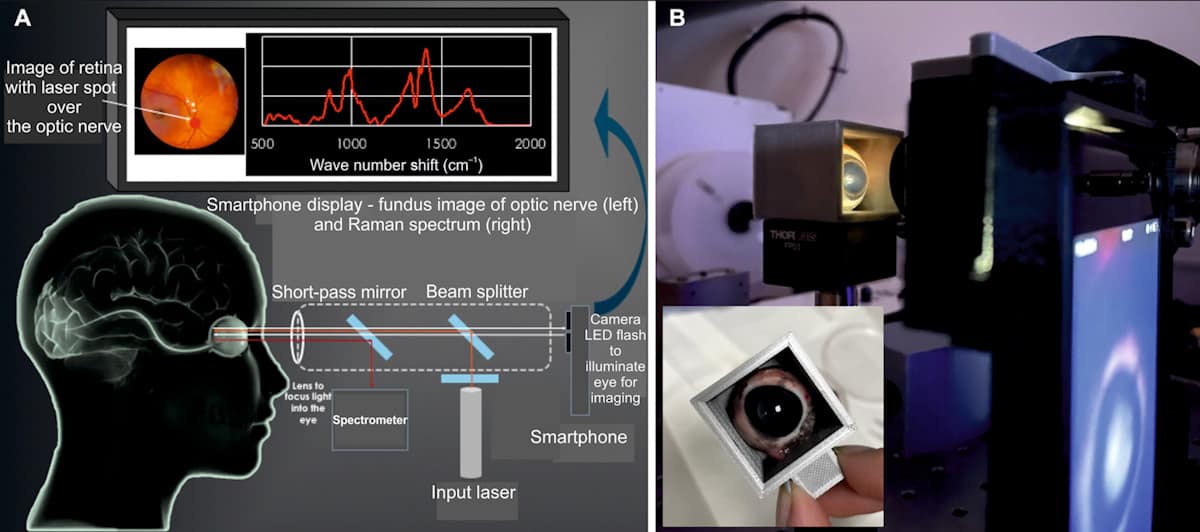
يعتمد جهاز حماية العين (EyeD) على تحليل رامان الطيفي، وهي تقنية بصرية تستخدم التشتت غير المرن لضوء الليزر لاستكشاف التركيب الجزيئي. يعمل عن طريق تسليط ليزر من الدرجة الأولى بطول 635 نانومتر على القرنية. يتم بعد ذلك تركيز الشعاع الموازي على شبكية العين بواسطة بصريات العين. ولتوجيه الليزر إلى المنطقة محل الاهتمام، يقوم نظام EyeD في الوقت نفسه بإجراء تصوير لقاع العين وتحليل طيفي باستخدام كاميرا الهاتف الذكي لتصور الجزء الخلفي من العين.
يتم تحليل أطياف رامان المجمعة من شبكية العين والعصب البصري بحثًا عن وجود تغيرات كيميائية حيوية خاصة بـ TBI، وذلك باستخدام خوارزمية الشبكة العصبية الاصطناعية SKiNET كأداة لدعم القرار. نظرًا لأن شبكية العين والعصب البصري مرتبطان ارتباطًا وثيقًا بالدماغ، فإن التغييرات في المؤشرات الحيوية بعد الإصابة ستعكس التغيرات البيوكيميائية في البيئة الدقيقة للدماغ.
"سيسمح جهازنا بالتشخيص المبكر لمرض TBI من خلال التقييم المباشر لتغيرات الضائقة الحادة في الوقت الفعلي في الأنسجة العصبية العصبية / البصرية الحية. يوضح قائد الفريق: "إنها تمكننا من فحص أنسجة الجهاز العصبي المركزي بشكل مباشر وغير جراحي". بولا غولدبرغ أوبنهايمر. "إن تحليل الشبكية العصبية باعتبارها إسقاطًا للجهاز العصبي المركزي يوفر نافذة على الكيمياء الحيوية للدماغ."
الدراسات الطيفية
ولاختبار أداء جهاز التصوير الخاص بهم، قام أوبنهايمر وزملاؤه ببناء شبح نسيجي يحاكي الأبعاد الفيزيائية والخصائص البصرية للعين، مع توفير توقيع رامان واقعي لشبكية العين. يشتمل الشبح على عدسة وثقب بقطر 4 مم يمثل الحدقة غير المتوسعة وحامل عينة لأنسجة الشبكية.
أثبت الفريق أن جهاز EyeD يمكنه تركيز شعاع الليزر بشكل فعال في الموضع المطلوب على شبكية العين. قامت الأطياف المقاسة من شبح الأنسجة بتحليل نطاقات رامان الرئيسية في المنطقة ذات العدد الموجي العالي، والتي يمكن استخدامها للتمييز بين عدد من أنواع الأنسجة.
استخدم الباحثون بعد ذلك الجهاز النموذجي لتحليل عينات الشبكية من عيون الخنازير، والتي تشبه عيون الإنسان في الحجم والبنية والتطور والتكوين. قاموا بجمع 510 قياسات من 39 عينة من شبكية TBI و12 عينة مراقبة، وسجلوا الأطياف من مكان قريب من القرص البصري. بشكل عام، أظهر أطياف رامان عدة نطاقات مميزة في 1200-1700 سم-1 منطقة بصمات الأصابع، بالإضافة إلى تعزيز نطاقات الموجات العالية في 2800-3200 سم-1 منطقة.

كشف استخدام SKiNET لإنشاء خرائط ذاتية التحسين (SOMs) توضح تجميع أطياف رامان الشبكية عن وجود فصل واضح بين شبكية العين مع TBI وعينات التحكم. ينشأ هذا لأن أطياف رامان تعكس التغيرات البيوكيميائية في العين بعد الإصابة الدماغية الرضية. على سبيل المثال، يزيد TBI من محتوى الدهون والبروتين في العين، مما يتسبب في أن تصبح القمم الناشئة عن هذه أكثر وضوحًا في أطياف رامان.
كانت أهم التغيرات الطيفية في الاستجابة لـ TBI بسبب مساهمات دهون الدماغ الكارديوليبين والسيتوكروم C، والتي تجلت في زيادة في نسبة 2930 إلى 2850 سم XNUMX.-1 الذروة في أطياف رامان. استخدم الباحثون ميزات مختارة لنسبة الذروة 2850/2930 وكثافة ست قمم مميزة من أطياف TBI لتشكيل تصنيف SKiNET، مما أدى إلى الحصول على باركود طيفي للكشف عن TBI.
لتقييم قدرة نظام EyeD على التمييز بين إصابات الدماغ المؤلمة عبر تغيرات الشبكية، قاموا بحساب المنطقة تحت المنحنى (AUC) لكل ذروة ونسبة الذروة 2930/2850، ورسموا معدلات إيجابية حقيقية مقابل معدلات سلبية كاذبة. أدى استخدام تحسين SKiNET مع التحقق من صحة بيانات التدريب بمقدار 10 أضعاف إلى دقة تصنيف تبلغ 90.7 ± 0.9٪. تشير هذه النتيجة إلى أن التغييرات في نسبة الذروة 2930/2850 بعد TBI يمكن أن توفر مؤشرا قيما لتمييز TBI عن الضوابط الصحية.
يقول أوبنهايمر: "إن استخدام التحليل الطيفي لرامان وتصوير قاع العين في وقت واحد، والذي يتم تعبئته كجهاز محمول منخفض التكلفة، يوفر أول مسار ملموس نحو تشخيص غير جراحي لنقطة الرعاية لإصابة الدماغ المؤلمة". عالم الفيزياء.

بالنسبة للارتجاجات، العيون هي نوافذ للدماغ
وستكون الخطوة التالية هي تحسين النموذج الأولي للتحقق من الصحة السريرية. لتسهيل الترجمة السريرية، يخطط الباحثون لاستبدال مقياس الطيف المستقل بمقياس طيفي مدمج على الجهاز وقراءة الهاتف الذكي، مما يتيح تصوير قاع العين وتحليل رامان الطيفي عبر شاشة هاتف ذكي واحدة.
يقول أوبنهايمر: "نحن نقوم حاليًا بتصميم جهاز قابل للنشر وسهل الاستخدام، ومتكامل مع خوارزمية الشبكة العصبية الاصطناعية الخاصة بنا للتفسير الآلي للمخرجات دون الحاجة إلى دعم متخصص، وتصنيف البيانات الطيفية بسرعة". "[نحن أيضًا] نقوم بتقييم قابلية استخدام الجهاز سريريًا لدى المتطوعين الأصحاء والمرضى لإثبات قدرته على التشخيص في الوقت الفعلي. وبعد التأكد من قابلية تحمل الجهاز وسهولة استخدامه، فإننا ننتقل إلى أول تقييم بشري وتجربة سريرية صغيرة النطاق.
- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- PlatoData.Network Vertical Generative Ai. تمكين نفسك. الوصول هنا.
- أفلاطونايستريم. ذكاء Web3. تضخيم المعرفة. الوصول هنا.
- أفلاطون كربون، كلينتك ، الطاقة، بيئة، شمسي، إدارة المخلفات. الوصول هنا.
- أفلاطون هيلث. التكنولوجيا الحيوية وذكاء التجارب السريرية. الوصول هنا.
- المصدر https://physicsworld.com/a/handheld-device-uses-eye-safe-retinal-spectroscopy-to-diagnose-brain-injury/



