02 أبريل 2024 (أضواء Nanowerk) الموائع الدقيقة، تقنية التحكم الدقيق في السوائل على مقياس أقل من المليمتر، كانت تبشر منذ فترة طويلة بإحداث ثورة في الأبحاث البيولوجية والتشخيص الطبي. ومن خلال تصغير الاختبارات إلى قطرات صغيرة من الماء في الزيت، يمكن لهذه المنصات تحليل الخلايا الفردية بسرعة وكفاءة غير مسبوقتين مع تقليل تكاليف الكاشف بشكل كبير. تعمل كل قطرة بمقياس بيكولتر كمفاعل دقيق معزول، مما يسمح بإجراء دراسات عالية الإنتاجية للسلوك الخلوي وتمكين تطبيقات متنوعة بدءًا من فحص الأدوية وحتى تحليل الخلايا النادرة. ومع ذلك، فإن إطلاق الإمكانات الكاملة لقطرات الموائع الدقيقة قد أعاقه التحدي المتمثل في التحليل السريع والشامل لمحتويات هذه الأجزاء الصغيرة. تعتمد الأساليب التقليدية على إعدادات الفحص المجهري المعقدة والمكلفة، وذلك باستخدام كاميرات عالية السرعة لتصوير كل قطرة أثناء تدفقها عبر الجهاز. وقد أدى التعقيد الفني والتكاليف الباهظة المرتبطة بهذه الأنظمة إلى الحد من الاعتماد الواسع النطاق للتقنيات القائمة على القطيرات في الأبحاث والإعدادات السريرية. الآن، قام فريق متعدد التخصصات من العلماء بتطوير OptiDrop، وهو جهاز مبتكر يتغلب ببراعة على هذه القيود من خلال دمج الألياف الضوئية مباشرة داخل شريحة ميكروفلويديك. يتيح هذا النهج الجديد اكتشاف معلمات بصرية متعددة من القطرات الفردية ومحتوياتها دون الاعتماد على المجهر أو الكاميرا. تم نشر النتيجة في مجلة Microsystems & Nanoengineering ("الفلورة المتعددة الإرسال والكشف عن التشتت باستخدام دقة الخلية المفردة باستخدام الألياف الضوئية الموجودة على الرقاقة لتطبيقات قطرات الموائع الدقيقة")، عبارة عن منصة مصغرة وبأسعار معقولة وسهلة الاستخدام توفر قوة تحليل الخلية المفردة متعددة المعلمات إلى تنسيق الفوق.
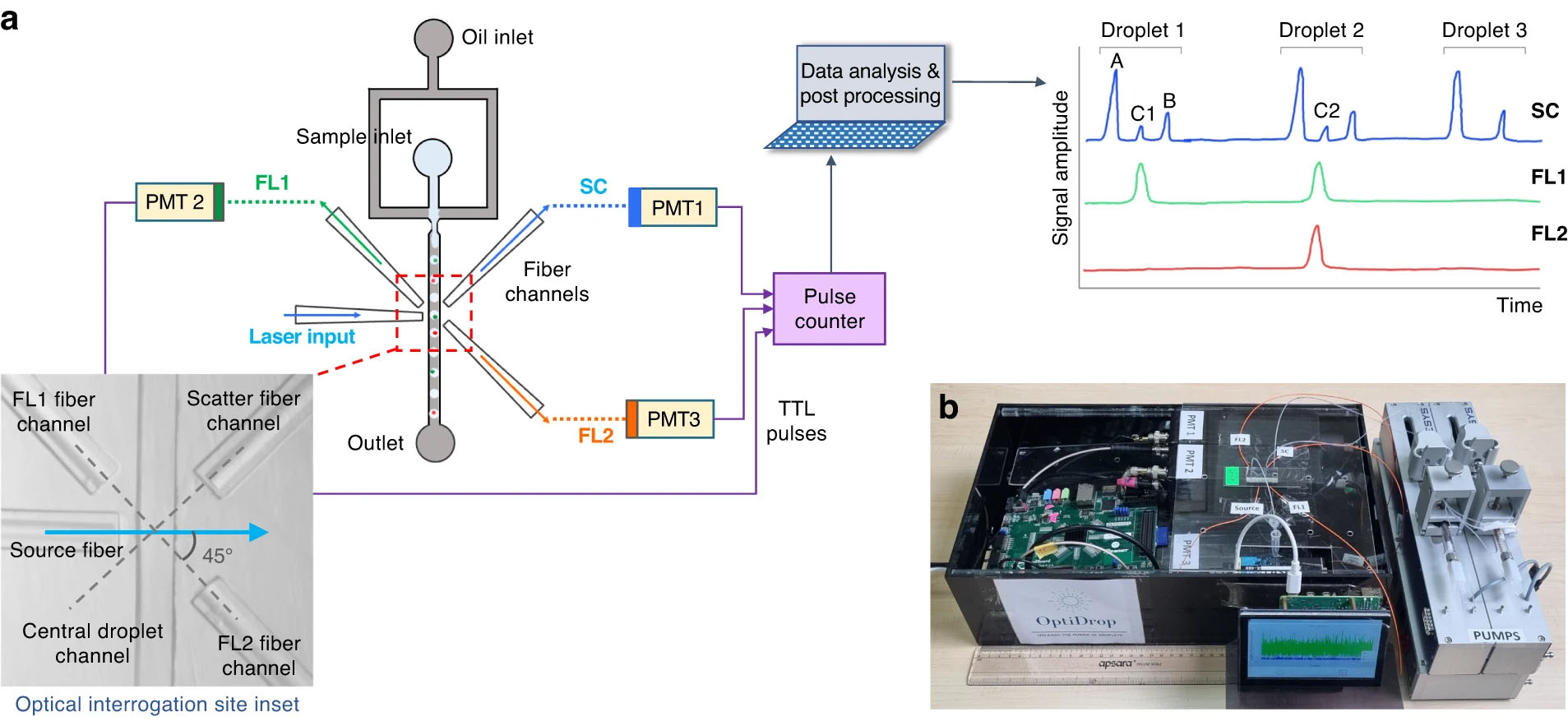 a تشتمل منصة OptiDrop على شريحة ميكروفلويديك مع مدخل للزيت والماء لتشكيل القطرات عند تقاطع تركيز التدفق. يتم تغليف الطور المائي داخل قطيرات ثم يتدفق بعد ذلك عبر موقع الاستجواب البصري (داخلي) ويحيط به مجموعة من أخاديد الألياف الضوئية مرتبة حول القناة المركزية. تُستخدم الأخاديد الموجودة على الرقاقة لإيواء الألياف الضوئية في مواضع زاوية محددة، مما يسمح بإضاءة قطرات فعالة باستخدام ضوء الليزر الساقط وجمع إشارات الضوء والتألق المتناثرة أثناء مرور القطرة عبر شعاع الضوء. يقترن إخراج الألياف الضوئية بـ PMT للكشف. يتم دمج أعداد نبضات TTL من كل PMT بواسطة شريحة FPGA مع عداد نبض ويتم رسمها كبيانات ذروة شدة الإشارة الخام. ويمكن تحليل البيانات الأولية بشكل أكبر لتحديد أو قياس شدة التألق من الخلايا محل الاهتمام. b وحدة مجمعة على سطح الطاولة مزودة بمسطرة قدم للقياس بالإضافة إلى شاشة عرض تدفق البيانات المباشرة ومضخات الحقن. (الصورة: Microsystems & Nanoengineering, CC BY 4.0) يكمن الابتكار الأساسي لـ OptiDrop في الوضع الاستراتيجي للألياف الضوئية حول قناة الموائع الدقيقة. عندما تمر كل قطرة عبر نقطة الاستجواب، يضيءها الليزر، مما يولد إشارات متناثرة وفلورية. يتم جمع هذه الإشارات الضوئية بكفاءة بواسطة ألياف موضوعة بزوايا 45 درجة ثم يتم توجيهها إلى أجهزة كشف منفصلة. تعمل الإلكترونيات المصممة خصيصًا على رقمنة الإشارات في الوقت الفعلي، مما يتيح التصور والتحليل الفوري للملف البصري لكل قطرة.
للتحقق من صحة أداء OptiDrop، قام الباحثون أولاً بتمييز حساسيته ونطاقه الديناميكي باستخدام أصباغ الفلورسنت القياسية. ومن المثير للإعجاب، أن الجهاز يمكنه اكتشاف تركيزات صبغية منخفضة تصل إلى 1 نانو مولار، مما ينافس حدود الكشف التي تحققها الأدوات التقليدية، بينما لا يتطلب سوى جزء صغير من حجم العينة. علاوة على ذلك، تم قياس شدة التألق بواسطة OptiDrop خطيًا عبر نطاق واسع من التركيزات، مما يضمن القياس الكمي الدقيق والموثوق.
بعد ذلك، أظهر الباحثون قدرات OptiDrop في تحليل الجسيمات باستخدام الخرزات الدقيقة ذات الأحجام المختلفة وكثافات الفلورسنت كمحاكاة للخلايا. تميزت المنصة بسهولة بين الخرزات بناءً على أبعادها الفيزيائية وخصائصها البصرية. والجدير بالذكر أنه حتى في الخليط غير المتجانس من حبات الفلورسنت الخافتة والمشرقة، تمكنت OptiDrop من تحديد وتعداد كل مجموعة سكانية فرعية بدقة. وهذا يسلط الضوء على قوة النظام في تحليل العينات البيولوجية المعقدة التي تحتوي على أنواع مختلفة من الخلايا.
ولعرض فائدة المنصة لتطبيق ذي صلة بيولوجيًا، أجرى الفريق اختبارًا للخلايا الحية للتحقيق في التعبير السطحي لبروتينات معقد التوافق النسيجي الرئيسي (MHC) على الخلايا المناعية. تعد جزيئات التوافق النسيجي الكبير (MHC) منظمات مهمة للاستجابات المناعية ضد مسببات الأمراض والخلايا غير الطبيعية، مما يجعل مستويات تعبيرها مؤشرات حيوية قيمة. من خلال الاستفادة من الأجسام المضادة ذات العلامات الفلورية، سمحت OptiDrop بالكشف المتزامن لكل من بروتينات MHC من الفئتين الأولى والثانية على الخلايا الفردية المغلفة داخل القطرات. أثار تحفيز الخلايا باستخدام إنترفيرون جاما، وهو السيتوكينات المحفزة للمناعة، التنظيم المتوقع لتعبير MHC، والذي تم قياسه بحساسية بواسطة منصة OptiDrop.
يمثل تطوير OptiDrop خطوة كبيرة نحو إضفاء الطابع الديمقراطي على قدرات التحليل المتطورة للخلية الواحدة. ومن خلال التغلب على حواجز التكلفة والتعقيد التي أعاقت اعتماد قطرات الموائع الدقيقة، توفر هذه المنصة المبتكرة أدوات استجواب خلوية قوية في متناول نطاق أوسع من الباحثين والأطباء. إن قدرته على تحمل التكاليف وسهولة الاستخدام والمتانة تجعله مناسبًا تمامًا للنشر الروتيني في مختبرات البحوث الطبية الحيوية وإعدادات تشخيص نقاط الرعاية.
التطبيقات المحتملة لـ OptiDrop واسعة وبعيدة المدى. وفي مجال مراقبة الأمراض، يمكن أن يتيح الكشف فائق الحساسية عن المؤشرات الحيوية النادرة، مما يسهل التشخيص المبكر غير الجراحي وتقييم الاستجابة للعلاج. قد يسمح التكامل مع سير عمل تسلسل الخلية الواحدة بالارتباط المباشر بين الأنماط الظاهرية البصرية وملفات تعريف التعبير الجيني، مما يوفر فهمًا أكثر شمولاً للحالات الخلوية. علاوة على ذلك، فإن التصميم المغلق للمنصة وقدرتها على معالجة العينات السريرية بسرعة يجعلها جذابة بشكل خاص لاختبار الأمراض المعدية وغيرها من التطبيقات التشخيصية الحساسة للوقت.
على الرغم من أن OptiDrop يمثل تقدمًا كبيرًا، إلا أنه لا يزال هناك مجال لمزيد من التحسين وتوسيع قدراته. إن زيادة الإنتاجية من خلال تمكين معدلات تدفق قطرات أسرع وتوليد قطرات أصغر يمكن أن تعزز كفاءتها وقابلية التوسع. إن دمج وظائف الفرز النشطة من شأنه أن يمكّن المستخدمين من عزل مجموعات سكانية فرعية محددة ذات أهمية بناءً على توقيعاتهم البصرية، مما يتيح إجراء التحليلات الجزيئية النهائية. علاوة على ذلك، سيكون تطوير تصميمات خرطوشة موحدة وواجهات برمجية بديهية أمرًا بالغ الأهمية لتبسيط تشغيلها وتفسير البيانات.
ومع تزايد الفروق الدقيقة في فهمنا للأنظمة البيولوجية، فإن أدوات مثل OptiDrop التي تدمج بسلاسة الموائع الدقيقة والبصريات والإلكترونيات ستكون لا غنى عنها لكشف تعقيداتها. من خلال توفير منصة يمكن الوصول إليها ومتعددة الاستخدامات لتحليل الخلية الواحدة عالي الإنتاجية، تزود OptiDrop الباحثين والأطباء بأداة قوية لطرح أسئلة جديدة، وتحدي النماذج الحالية، وترجمة الاكتشافات الرائدة إلى تأثيرات حقيقية ذات معنى.
a تشتمل منصة OptiDrop على شريحة ميكروفلويديك مع مدخل للزيت والماء لتشكيل القطرات عند تقاطع تركيز التدفق. يتم تغليف الطور المائي داخل قطيرات ثم يتدفق بعد ذلك عبر موقع الاستجواب البصري (داخلي) ويحيط به مجموعة من أخاديد الألياف الضوئية مرتبة حول القناة المركزية. تُستخدم الأخاديد الموجودة على الرقاقة لإيواء الألياف الضوئية في مواضع زاوية محددة، مما يسمح بإضاءة قطرات فعالة باستخدام ضوء الليزر الساقط وجمع إشارات الضوء والتألق المتناثرة أثناء مرور القطرة عبر شعاع الضوء. يقترن إخراج الألياف الضوئية بـ PMT للكشف. يتم دمج أعداد نبضات TTL من كل PMT بواسطة شريحة FPGA مع عداد نبض ويتم رسمها كبيانات ذروة شدة الإشارة الخام. ويمكن تحليل البيانات الأولية بشكل أكبر لتحديد أو قياس شدة التألق من الخلايا محل الاهتمام. b وحدة مجمعة على سطح الطاولة مزودة بمسطرة قدم للقياس بالإضافة إلى شاشة عرض تدفق البيانات المباشرة ومضخات الحقن. (الصورة: Microsystems & Nanoengineering, CC BY 4.0) يكمن الابتكار الأساسي لـ OptiDrop في الوضع الاستراتيجي للألياف الضوئية حول قناة الموائع الدقيقة. عندما تمر كل قطرة عبر نقطة الاستجواب، يضيءها الليزر، مما يولد إشارات متناثرة وفلورية. يتم جمع هذه الإشارات الضوئية بكفاءة بواسطة ألياف موضوعة بزوايا 45 درجة ثم يتم توجيهها إلى أجهزة كشف منفصلة. تعمل الإلكترونيات المصممة خصيصًا على رقمنة الإشارات في الوقت الفعلي، مما يتيح التصور والتحليل الفوري للملف البصري لكل قطرة.
للتحقق من صحة أداء OptiDrop، قام الباحثون أولاً بتمييز حساسيته ونطاقه الديناميكي باستخدام أصباغ الفلورسنت القياسية. ومن المثير للإعجاب، أن الجهاز يمكنه اكتشاف تركيزات صبغية منخفضة تصل إلى 1 نانو مولار، مما ينافس حدود الكشف التي تحققها الأدوات التقليدية، بينما لا يتطلب سوى جزء صغير من حجم العينة. علاوة على ذلك، تم قياس شدة التألق بواسطة OptiDrop خطيًا عبر نطاق واسع من التركيزات، مما يضمن القياس الكمي الدقيق والموثوق.
بعد ذلك، أظهر الباحثون قدرات OptiDrop في تحليل الجسيمات باستخدام الخرزات الدقيقة ذات الأحجام المختلفة وكثافات الفلورسنت كمحاكاة للخلايا. تميزت المنصة بسهولة بين الخرزات بناءً على أبعادها الفيزيائية وخصائصها البصرية. والجدير بالذكر أنه حتى في الخليط غير المتجانس من حبات الفلورسنت الخافتة والمشرقة، تمكنت OptiDrop من تحديد وتعداد كل مجموعة سكانية فرعية بدقة. وهذا يسلط الضوء على قوة النظام في تحليل العينات البيولوجية المعقدة التي تحتوي على أنواع مختلفة من الخلايا.
ولعرض فائدة المنصة لتطبيق ذي صلة بيولوجيًا، أجرى الفريق اختبارًا للخلايا الحية للتحقيق في التعبير السطحي لبروتينات معقد التوافق النسيجي الرئيسي (MHC) على الخلايا المناعية. تعد جزيئات التوافق النسيجي الكبير (MHC) منظمات مهمة للاستجابات المناعية ضد مسببات الأمراض والخلايا غير الطبيعية، مما يجعل مستويات تعبيرها مؤشرات حيوية قيمة. من خلال الاستفادة من الأجسام المضادة ذات العلامات الفلورية، سمحت OptiDrop بالكشف المتزامن لكل من بروتينات MHC من الفئتين الأولى والثانية على الخلايا الفردية المغلفة داخل القطرات. أثار تحفيز الخلايا باستخدام إنترفيرون جاما، وهو السيتوكينات المحفزة للمناعة، التنظيم المتوقع لتعبير MHC، والذي تم قياسه بحساسية بواسطة منصة OptiDrop.
يمثل تطوير OptiDrop خطوة كبيرة نحو إضفاء الطابع الديمقراطي على قدرات التحليل المتطورة للخلية الواحدة. ومن خلال التغلب على حواجز التكلفة والتعقيد التي أعاقت اعتماد قطرات الموائع الدقيقة، توفر هذه المنصة المبتكرة أدوات استجواب خلوية قوية في متناول نطاق أوسع من الباحثين والأطباء. إن قدرته على تحمل التكاليف وسهولة الاستخدام والمتانة تجعله مناسبًا تمامًا للنشر الروتيني في مختبرات البحوث الطبية الحيوية وإعدادات تشخيص نقاط الرعاية.
التطبيقات المحتملة لـ OptiDrop واسعة وبعيدة المدى. وفي مجال مراقبة الأمراض، يمكن أن يتيح الكشف فائق الحساسية عن المؤشرات الحيوية النادرة، مما يسهل التشخيص المبكر غير الجراحي وتقييم الاستجابة للعلاج. قد يسمح التكامل مع سير عمل تسلسل الخلية الواحدة بالارتباط المباشر بين الأنماط الظاهرية البصرية وملفات تعريف التعبير الجيني، مما يوفر فهمًا أكثر شمولاً للحالات الخلوية. علاوة على ذلك، فإن التصميم المغلق للمنصة وقدرتها على معالجة العينات السريرية بسرعة يجعلها جذابة بشكل خاص لاختبار الأمراض المعدية وغيرها من التطبيقات التشخيصية الحساسة للوقت.
على الرغم من أن OptiDrop يمثل تقدمًا كبيرًا، إلا أنه لا يزال هناك مجال لمزيد من التحسين وتوسيع قدراته. إن زيادة الإنتاجية من خلال تمكين معدلات تدفق قطرات أسرع وتوليد قطرات أصغر يمكن أن تعزز كفاءتها وقابلية التوسع. إن دمج وظائف الفرز النشطة من شأنه أن يمكّن المستخدمين من عزل مجموعات سكانية فرعية محددة ذات أهمية بناءً على توقيعاتهم البصرية، مما يتيح إجراء التحليلات الجزيئية النهائية. علاوة على ذلك، سيكون تطوير تصميمات خرطوشة موحدة وواجهات برمجية بديهية أمرًا بالغ الأهمية لتبسيط تشغيلها وتفسير البيانات.
ومع تزايد الفروق الدقيقة في فهمنا للأنظمة البيولوجية، فإن أدوات مثل OptiDrop التي تدمج بسلاسة الموائع الدقيقة والبصريات والإلكترونيات ستكون لا غنى عنها لكشف تعقيداتها. من خلال توفير منصة يمكن الوصول إليها ومتعددة الاستخدامات لتحليل الخلية الواحدة عالي الإنتاجية، تزود OptiDrop الباحثين والأطباء بأداة قوية لطرح أسئلة جديدة، وتحدي النماذج الحالية، وترجمة الاكتشافات الرائدة إلى تأثيرات حقيقية ذات معنى.
 a تشتمل منصة OptiDrop على شريحة ميكروفلويديك مع مدخل للزيت والماء لتشكيل القطرات عند تقاطع تركيز التدفق. يتم تغليف الطور المائي داخل قطيرات ثم يتدفق بعد ذلك عبر موقع الاستجواب البصري (داخلي) ويحيط به مجموعة من أخاديد الألياف الضوئية مرتبة حول القناة المركزية. تُستخدم الأخاديد الموجودة على الرقاقة لإيواء الألياف الضوئية في مواضع زاوية محددة، مما يسمح بإضاءة قطرات فعالة باستخدام ضوء الليزر الساقط وجمع إشارات الضوء والتألق المتناثرة أثناء مرور القطرة عبر شعاع الضوء. يقترن إخراج الألياف الضوئية بـ PMT للكشف. يتم دمج أعداد نبضات TTL من كل PMT بواسطة شريحة FPGA مع عداد نبض ويتم رسمها كبيانات ذروة شدة الإشارة الخام. ويمكن تحليل البيانات الأولية بشكل أكبر لتحديد أو قياس شدة التألق من الخلايا محل الاهتمام. b وحدة مجمعة على سطح الطاولة مزودة بمسطرة قدم للقياس بالإضافة إلى شاشة عرض تدفق البيانات المباشرة ومضخات الحقن. (الصورة: Microsystems & Nanoengineering, CC BY 4.0) يكمن الابتكار الأساسي لـ OptiDrop في الوضع الاستراتيجي للألياف الضوئية حول قناة الموائع الدقيقة. عندما تمر كل قطرة عبر نقطة الاستجواب، يضيءها الليزر، مما يولد إشارات متناثرة وفلورية. يتم جمع هذه الإشارات الضوئية بكفاءة بواسطة ألياف موضوعة بزوايا 45 درجة ثم يتم توجيهها إلى أجهزة كشف منفصلة. تعمل الإلكترونيات المصممة خصيصًا على رقمنة الإشارات في الوقت الفعلي، مما يتيح التصور والتحليل الفوري للملف البصري لكل قطرة.
للتحقق من صحة أداء OptiDrop، قام الباحثون أولاً بتمييز حساسيته ونطاقه الديناميكي باستخدام أصباغ الفلورسنت القياسية. ومن المثير للإعجاب، أن الجهاز يمكنه اكتشاف تركيزات صبغية منخفضة تصل إلى 1 نانو مولار، مما ينافس حدود الكشف التي تحققها الأدوات التقليدية، بينما لا يتطلب سوى جزء صغير من حجم العينة. علاوة على ذلك، تم قياس شدة التألق بواسطة OptiDrop خطيًا عبر نطاق واسع من التركيزات، مما يضمن القياس الكمي الدقيق والموثوق.
بعد ذلك، أظهر الباحثون قدرات OptiDrop في تحليل الجسيمات باستخدام الخرزات الدقيقة ذات الأحجام المختلفة وكثافات الفلورسنت كمحاكاة للخلايا. تميزت المنصة بسهولة بين الخرزات بناءً على أبعادها الفيزيائية وخصائصها البصرية. والجدير بالذكر أنه حتى في الخليط غير المتجانس من حبات الفلورسنت الخافتة والمشرقة، تمكنت OptiDrop من تحديد وتعداد كل مجموعة سكانية فرعية بدقة. وهذا يسلط الضوء على قوة النظام في تحليل العينات البيولوجية المعقدة التي تحتوي على أنواع مختلفة من الخلايا.
ولعرض فائدة المنصة لتطبيق ذي صلة بيولوجيًا، أجرى الفريق اختبارًا للخلايا الحية للتحقيق في التعبير السطحي لبروتينات معقد التوافق النسيجي الرئيسي (MHC) على الخلايا المناعية. تعد جزيئات التوافق النسيجي الكبير (MHC) منظمات مهمة للاستجابات المناعية ضد مسببات الأمراض والخلايا غير الطبيعية، مما يجعل مستويات تعبيرها مؤشرات حيوية قيمة. من خلال الاستفادة من الأجسام المضادة ذات العلامات الفلورية، سمحت OptiDrop بالكشف المتزامن لكل من بروتينات MHC من الفئتين الأولى والثانية على الخلايا الفردية المغلفة داخل القطرات. أثار تحفيز الخلايا باستخدام إنترفيرون جاما، وهو السيتوكينات المحفزة للمناعة، التنظيم المتوقع لتعبير MHC، والذي تم قياسه بحساسية بواسطة منصة OptiDrop.
يمثل تطوير OptiDrop خطوة كبيرة نحو إضفاء الطابع الديمقراطي على قدرات التحليل المتطورة للخلية الواحدة. ومن خلال التغلب على حواجز التكلفة والتعقيد التي أعاقت اعتماد قطرات الموائع الدقيقة، توفر هذه المنصة المبتكرة أدوات استجواب خلوية قوية في متناول نطاق أوسع من الباحثين والأطباء. إن قدرته على تحمل التكاليف وسهولة الاستخدام والمتانة تجعله مناسبًا تمامًا للنشر الروتيني في مختبرات البحوث الطبية الحيوية وإعدادات تشخيص نقاط الرعاية.
التطبيقات المحتملة لـ OptiDrop واسعة وبعيدة المدى. وفي مجال مراقبة الأمراض، يمكن أن يتيح الكشف فائق الحساسية عن المؤشرات الحيوية النادرة، مما يسهل التشخيص المبكر غير الجراحي وتقييم الاستجابة للعلاج. قد يسمح التكامل مع سير عمل تسلسل الخلية الواحدة بالارتباط المباشر بين الأنماط الظاهرية البصرية وملفات تعريف التعبير الجيني، مما يوفر فهمًا أكثر شمولاً للحالات الخلوية. علاوة على ذلك، فإن التصميم المغلق للمنصة وقدرتها على معالجة العينات السريرية بسرعة يجعلها جذابة بشكل خاص لاختبار الأمراض المعدية وغيرها من التطبيقات التشخيصية الحساسة للوقت.
على الرغم من أن OptiDrop يمثل تقدمًا كبيرًا، إلا أنه لا يزال هناك مجال لمزيد من التحسين وتوسيع قدراته. إن زيادة الإنتاجية من خلال تمكين معدلات تدفق قطرات أسرع وتوليد قطرات أصغر يمكن أن تعزز كفاءتها وقابلية التوسع. إن دمج وظائف الفرز النشطة من شأنه أن يمكّن المستخدمين من عزل مجموعات سكانية فرعية محددة ذات أهمية بناءً على توقيعاتهم البصرية، مما يتيح إجراء التحليلات الجزيئية النهائية. علاوة على ذلك، سيكون تطوير تصميمات خرطوشة موحدة وواجهات برمجية بديهية أمرًا بالغ الأهمية لتبسيط تشغيلها وتفسير البيانات.
ومع تزايد الفروق الدقيقة في فهمنا للأنظمة البيولوجية، فإن أدوات مثل OptiDrop التي تدمج بسلاسة الموائع الدقيقة والبصريات والإلكترونيات ستكون لا غنى عنها لكشف تعقيداتها. من خلال توفير منصة يمكن الوصول إليها ومتعددة الاستخدامات لتحليل الخلية الواحدة عالي الإنتاجية، تزود OptiDrop الباحثين والأطباء بأداة قوية لطرح أسئلة جديدة، وتحدي النماذج الحالية، وترجمة الاكتشافات الرائدة إلى تأثيرات حقيقية ذات معنى.
a تشتمل منصة OptiDrop على شريحة ميكروفلويديك مع مدخل للزيت والماء لتشكيل القطرات عند تقاطع تركيز التدفق. يتم تغليف الطور المائي داخل قطيرات ثم يتدفق بعد ذلك عبر موقع الاستجواب البصري (داخلي) ويحيط به مجموعة من أخاديد الألياف الضوئية مرتبة حول القناة المركزية. تُستخدم الأخاديد الموجودة على الرقاقة لإيواء الألياف الضوئية في مواضع زاوية محددة، مما يسمح بإضاءة قطرات فعالة باستخدام ضوء الليزر الساقط وجمع إشارات الضوء والتألق المتناثرة أثناء مرور القطرة عبر شعاع الضوء. يقترن إخراج الألياف الضوئية بـ PMT للكشف. يتم دمج أعداد نبضات TTL من كل PMT بواسطة شريحة FPGA مع عداد نبض ويتم رسمها كبيانات ذروة شدة الإشارة الخام. ويمكن تحليل البيانات الأولية بشكل أكبر لتحديد أو قياس شدة التألق من الخلايا محل الاهتمام. b وحدة مجمعة على سطح الطاولة مزودة بمسطرة قدم للقياس بالإضافة إلى شاشة عرض تدفق البيانات المباشرة ومضخات الحقن. (الصورة: Microsystems & Nanoengineering, CC BY 4.0) يكمن الابتكار الأساسي لـ OptiDrop في الوضع الاستراتيجي للألياف الضوئية حول قناة الموائع الدقيقة. عندما تمر كل قطرة عبر نقطة الاستجواب، يضيءها الليزر، مما يولد إشارات متناثرة وفلورية. يتم جمع هذه الإشارات الضوئية بكفاءة بواسطة ألياف موضوعة بزوايا 45 درجة ثم يتم توجيهها إلى أجهزة كشف منفصلة. تعمل الإلكترونيات المصممة خصيصًا على رقمنة الإشارات في الوقت الفعلي، مما يتيح التصور والتحليل الفوري للملف البصري لكل قطرة.
للتحقق من صحة أداء OptiDrop، قام الباحثون أولاً بتمييز حساسيته ونطاقه الديناميكي باستخدام أصباغ الفلورسنت القياسية. ومن المثير للإعجاب، أن الجهاز يمكنه اكتشاف تركيزات صبغية منخفضة تصل إلى 1 نانو مولار، مما ينافس حدود الكشف التي تحققها الأدوات التقليدية، بينما لا يتطلب سوى جزء صغير من حجم العينة. علاوة على ذلك، تم قياس شدة التألق بواسطة OptiDrop خطيًا عبر نطاق واسع من التركيزات، مما يضمن القياس الكمي الدقيق والموثوق.
بعد ذلك، أظهر الباحثون قدرات OptiDrop في تحليل الجسيمات باستخدام الخرزات الدقيقة ذات الأحجام المختلفة وكثافات الفلورسنت كمحاكاة للخلايا. تميزت المنصة بسهولة بين الخرزات بناءً على أبعادها الفيزيائية وخصائصها البصرية. والجدير بالذكر أنه حتى في الخليط غير المتجانس من حبات الفلورسنت الخافتة والمشرقة، تمكنت OptiDrop من تحديد وتعداد كل مجموعة سكانية فرعية بدقة. وهذا يسلط الضوء على قوة النظام في تحليل العينات البيولوجية المعقدة التي تحتوي على أنواع مختلفة من الخلايا.
ولعرض فائدة المنصة لتطبيق ذي صلة بيولوجيًا، أجرى الفريق اختبارًا للخلايا الحية للتحقيق في التعبير السطحي لبروتينات معقد التوافق النسيجي الرئيسي (MHC) على الخلايا المناعية. تعد جزيئات التوافق النسيجي الكبير (MHC) منظمات مهمة للاستجابات المناعية ضد مسببات الأمراض والخلايا غير الطبيعية، مما يجعل مستويات تعبيرها مؤشرات حيوية قيمة. من خلال الاستفادة من الأجسام المضادة ذات العلامات الفلورية، سمحت OptiDrop بالكشف المتزامن لكل من بروتينات MHC من الفئتين الأولى والثانية على الخلايا الفردية المغلفة داخل القطرات. أثار تحفيز الخلايا باستخدام إنترفيرون جاما، وهو السيتوكينات المحفزة للمناعة، التنظيم المتوقع لتعبير MHC، والذي تم قياسه بحساسية بواسطة منصة OptiDrop.
يمثل تطوير OptiDrop خطوة كبيرة نحو إضفاء الطابع الديمقراطي على قدرات التحليل المتطورة للخلية الواحدة. ومن خلال التغلب على حواجز التكلفة والتعقيد التي أعاقت اعتماد قطرات الموائع الدقيقة، توفر هذه المنصة المبتكرة أدوات استجواب خلوية قوية في متناول نطاق أوسع من الباحثين والأطباء. إن قدرته على تحمل التكاليف وسهولة الاستخدام والمتانة تجعله مناسبًا تمامًا للنشر الروتيني في مختبرات البحوث الطبية الحيوية وإعدادات تشخيص نقاط الرعاية.
التطبيقات المحتملة لـ OptiDrop واسعة وبعيدة المدى. وفي مجال مراقبة الأمراض، يمكن أن يتيح الكشف فائق الحساسية عن المؤشرات الحيوية النادرة، مما يسهل التشخيص المبكر غير الجراحي وتقييم الاستجابة للعلاج. قد يسمح التكامل مع سير عمل تسلسل الخلية الواحدة بالارتباط المباشر بين الأنماط الظاهرية البصرية وملفات تعريف التعبير الجيني، مما يوفر فهمًا أكثر شمولاً للحالات الخلوية. علاوة على ذلك، فإن التصميم المغلق للمنصة وقدرتها على معالجة العينات السريرية بسرعة يجعلها جذابة بشكل خاص لاختبار الأمراض المعدية وغيرها من التطبيقات التشخيصية الحساسة للوقت.
على الرغم من أن OptiDrop يمثل تقدمًا كبيرًا، إلا أنه لا يزال هناك مجال لمزيد من التحسين وتوسيع قدراته. إن زيادة الإنتاجية من خلال تمكين معدلات تدفق قطرات أسرع وتوليد قطرات أصغر يمكن أن تعزز كفاءتها وقابلية التوسع. إن دمج وظائف الفرز النشطة من شأنه أن يمكّن المستخدمين من عزل مجموعات سكانية فرعية محددة ذات أهمية بناءً على توقيعاتهم البصرية، مما يتيح إجراء التحليلات الجزيئية النهائية. علاوة على ذلك، سيكون تطوير تصميمات خرطوشة موحدة وواجهات برمجية بديهية أمرًا بالغ الأهمية لتبسيط تشغيلها وتفسير البيانات.
ومع تزايد الفروق الدقيقة في فهمنا للأنظمة البيولوجية، فإن أدوات مثل OptiDrop التي تدمج بسلاسة الموائع الدقيقة والبصريات والإلكترونيات ستكون لا غنى عنها لكشف تعقيداتها. من خلال توفير منصة يمكن الوصول إليها ومتعددة الاستخدامات لتحليل الخلية الواحدة عالي الإنتاجية، تزود OptiDrop الباحثين والأطباء بأداة قوية لطرح أسئلة جديدة، وتحدي النماذج الحالية، وترجمة الاكتشافات الرائدة إلى تأثيرات حقيقية ذات معنى.

By
مايكل
بيرجر
- مايكل مؤلف لثلاثة كتب للجمعية الملكية للكيمياء:
جمعية النانو: دفع حدود التكنولوجيا,
تقنية النانو: المستقبل صغيرو
هندسة النانو: المهارات والأدوات التي تجعل التكنولوجيا غير مرئية
حقوق الطبع والنشر ©
نانويرك ذ
كن مؤلفًا ضيفًا في Spotlight! انضم إلى مجموعتنا الكبيرة والمتنامية من المساهمين الضيوف. هل نشرت للتو ورقة علمية أو لديك تطورات أخرى مثيرة لمشاركتها مع مجتمع تكنولوجيا النانو؟ إليك كيفية النشر على nanowerk.com.
- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- PlatoData.Network Vertical Generative Ai. تمكين نفسك. الوصول هنا.
- أفلاطونايستريم. ذكاء Web3. تضخيم المعرفة. الوصول هنا.
- أفلاطون كربون، كلينتك ، الطاقة، بيئة، شمسي، إدارة المخلفات. الوصول هنا.
- أفلاطون هيلث. التكنولوجيا الحيوية وذكاء التجارب السريرية. الوصول هنا.
- المصدر https://www.nanowerk.com/spotlight/spotid=64952.php



