تتيح منصة اكتشاف الأدوية RADR® التي تعتمد على الذكاء الاصطناعي من Lantern Pharma إنشاء قيمة عبر أبعاد متعددة لعملية تطوير أدوية الأورام: بدءًا من توسيع المؤشرات العلاجية وتحديد تركيبات الأدوية لاستخدامها في علم الأورام الدقيق ، بالإضافة إلى إنشاء توقيعات استجابة المريض أو ملفات تعريف العلامات الحيوية التي يمكن استخدامها لزيادة نجاح تجربة سريرية.
إن عملية إنشاء علاجات جديدة للسرطان محفوفة بالعديد من العوائق ، مما يؤثر بشكل كبير على فعاليته ويبطئ انتشار العلاجات الناجحة. الواقع المثير للقلق هو أن 97٪ من عقاقير الأورام المحتملة لا يتم تقديمها إلى السوق أبدًا ، وفقًا لتقديرات من قبل Wong، Siah and Lo، 2019. يرجع معدل الفشل هذا إلى حد كبير إلى التفاعل المعقد للأهداف الجينية ، والزيادات المفاجئة غير المتوقعة في مقاومة المريض للأدوية ، والقيود التنبؤية لنماذجنا قبل السريرية الحالية. ومما يزيد الأمور تعقيدًا أن الأدوية الناجحة غالبًا ما تسفر فقط عن فوائد هامشية للبقاء على قيد الحياة للمرضى.
يعد تصميم التجارب السريرية مشكلة أيضًا ، وغالبًا ما يتم اختبار الأدوية بشكل عشوائي عبر أنواع مختلفة من السرطان ، دون النظر إلى الآثار الجينية المحددة للعقار. وفقًا لدراسة عام 2021 هل استخدام العلامات الحيوية في علم الأورام يحسن من مخاطر فشل التجارب السريرية؟ تحليل واسع النطاق'، فإن التجارب السريرية المصممة بدون دمج المؤشرات الحيوية ذات الصلة والمفيدة أكثر عرضة للفشل 12 مرة.
الحاجة الماسة لإحراز تقدم في اكتشاف أدوية الأورام
يمكن أن يُعزى معدل فشل برامج اكتشاف عقاقير الأورام الحالية في التجارب السريرية إلى عوامل معقدة متعددة. يتمثل أحد التحديات البارزة في سوء فهم فعالية الدواء ، غالبًا بسبب التأثيرات غير المتوقعة خارج الهدف ، والتي تحجب آلية العمل الحقيقية للدواء (MOA). على سبيل المثال ، يمكن أن يؤدي هذا الالتباس إلى التوصيف الخاطئ لمثبطات محددة الهدف ، وهو أحد المضاعفات مثال عن طريق مثبط لوسين سحاب كيناز الأمومي (MELK) OST167. على الرغم من تحديد MELK باعتباره حاسمًا في أنواع السرطان المتعددة ، فقد وجد أنه غير ضروري لصلاحية الخلايا السرطانية ، مما ساهم على الأرجح في سوء الفهم. ينشأ المزيد من الالتباس من سوء تحديد المؤشرات الحيوية ، مما يعيق تحديد الهدف الحقيقي للدواء. دراسات مثل لين وآخرون. (2019) أظهرت أيضًا أن بعض البروتينات ، بما في ذلك MELK و HDAC6 و MAPK14 و PAK4 و PBK و PIM1 ، التي كان يُعتقد في البداية أنها ضرورية للسرطان ، هي في الواقع غير ضرورية لبقاء الخلايا السرطانية ، وبالتالي إضافة طبقة أخرى من التعقيد لاكتشاف الدواء والموافقة عليه عملية.
قد يؤدي النهج العشوائي للتجارب السريرية للأورام إلى إضعاف فعالية التجارب وتفويت الفرص المحتملة. يقدم عقار sorafenib مثالاً حياً على مفاجآت في تطوير عقاقير السرطان. كان من المتوقع في البداية أن يعمل عن طريق تثبيط جين BRAF ، لكن الاختبارات في الورم الميلانيني ، حيث تكون طفرات BRAF شائعة ، لم تسفر عن فائدة للبقاء على قيد الحياة. وبدلاً من ذلك ، أظهر العقار فاعلية في منع VEGF ، وهو جزيء ينظم نمو الأوعية الدموية. أدى ذلك إلى موافقة إدارة الغذاء والدواء الأمريكية على علاج سرطان الكلى والكبد والغدة الدرقية.
إن تعقيد وتنوع المشهد الجيني للسرطان ، إلى جانب التحدي المتمثل في مقاومة الأدوية ، لهما تأثير كبير على تقدم علاجات السرطان الناجحة. خذ ، حتى الآن مثال آخر، عقار Avastin الذي كان واعدًا في يوم من الأيام. تمت الموافقة مبدئيًا على سرطان الثدي النقيلي في عام 2008 ، وتم إلغاؤه لاحقًا من قِبل إدارة الغذاء والدواء في عام 2011 بسبب نقص الأدلة في تمديد بقاء المريض وتخفيف نمو الورم.
تسلط هذه التحديات الضوء على الحاجة الملحة لاستراتيجية أكثر تعقيدًا في تطوير عقاقير السرطان وتصميم التجارب السريرية - استراتيجية قادرة على معالجة التنوع الجيني بذكاء وتوقع مقاومة الأدوية وتحسين التخصيص العلاجي. هذه الإستراتيجية المتطورة هي في صميم مهمة Lantern Pharma ، التي تعزز قوة الذكاء الاصطناعي (AI) من خلال منصة RADR® الخاصة بهم لتلبية هذه الاحتياجات وجهاً لوجه.
تمكين علاج الأورام الدقيق باستخدام منصة RADR® AI
منذ إنشائها في عام 2014 ، مقرها دالاس التكنولوجيا الحيوية المرحلة السريرية لانترن فارما لقد التزم بتحسين معايير الرعاية لمرضى السرطان من خلال توسيع مساحة المؤشرات العلاجية ، وتحديد فرص العلاج المركب ، وتصميم تجارب سريرية أفضل مع استراتيجيات اختيار المريض بدقة.
دعم اكتشاف الأدوية السرطانية وتطويرها باستخدام الذكاء الاصطناعي ومنصة التعلم الآلي RADR®
في مواجهة التحديات متعددة الأوجه لتطوير علاج السرطان ، تحتل Lantern Pharma موقع الصدارة بأداة رائدة: RADR® ، وهي عبارة عن منصة تعتمد على الذكاء الاصطناعي تستغل التعلم الآلي لتحديد آليات العمل (MoA) ، والتي تقود التطوير قبل السريري لـ أصول علم الأورام ، وتحديد المؤشرات العلاجية الجديدة ، والتمييز والتنبؤ باستجابات المريض لأدوية معينة. تم تصميم RADR® لتحليل البيانات الجينومية والنسخية المستمدة من الدراسات السريرية وما قبل السريرية بعمق ، وهو حل يضيء على تعقيدات عدم التجانس الجيني في السرطانات والمرضى.
غالبًا ما يعقد التنوع الجيني للسرطان تحديد مجموعات المرضى التي من المحتمل أن تستجيب بشكل إيجابي لعقار معين في التجارب السريرية ، مما يؤدي إلى نقاط نهاية قد تفتقر إلى الأهمية الإحصائية وتعيق إثبات الفائدة السريرية للموافقة التنظيمية. تم تصميم RADR® لمواجهة هذا التحدي بشكل مباشر ، بهدف الكشف عن مجموعات المرضى الأكثر ملاءمة لعلاجات محددة.
باستخدام البيانات النصية والجينومية والحساسية للأدوية من مصادر متعددة ، يحلل RADR® أكثر من 25 مليار نقطة بيانات سريرية ، وأكثر من 154 تفاعلًا مع الورم الدوائي ، وأكثر من 130,000 سجل مريض عبر 17 قاعدة بيانات. تحتضن المنصة مجموعات بيانات من الموارد العامة ، والدراسات السريرية التجارية ، ونماذج الورم خارج الجسم الحي ثلاثي الأبعاد من Lantern لرسم العلاقات بين المؤشرات الحيوية الجينية ونشاط الدواء. تعمل هذه العملية الشاملة على تحويل بيانات omics المتعددة إلى نموذج مثالي يتنبأ باستجابات الأدوية ، ويولد المؤشرات الحيوية المرشحة ويساعد في التقسيم الطبقي للمريض لتصميم التجارب السريرية.

رصيد الصورة: Lantern Pharma. منصة اكتشاف الأدوية RADR® التي تعتمد على الذكاء الاصطناعي في الشركة.
والجدير بالذكر أن منصة RADR® لا تتعلق فقط بتحسين اختيار المريض ؛ إنه يتعلق أيضًا بتخفيف المخاطر وتحسين النجاح في تطوير الأدوية. من خلال فصل المرضى إلى مستجيبين محتملين وغير مستجيبين لعلاجات الأورام المختلفة ، يعزز RADR® القدرة على التخلص من المخاطر السريرية وزيادة احتمالية موافقة إدارة الغذاء والدواء. إن هذا الإثراء الاستراتيجي للمرضى لا يؤدي فقط إلى تبسيط التجارب السريرية ، مما يقلل من تكاليف الأبحاث ويسرع في تقديم علاجات جديدة مهمة فحسب ، بل يمهد أيضًا الطريق لتخصيص علاجات السرطان وتحسين نتائج المرضى.
علاوة على ذلك ، يتم تكييف سير العمل التشغيلي لـ RADR® بمرونة لمجموعة من الأدوية المرشحة: تلك الموجودة في المراحل المبكرة للمساعدة في تحديد المؤشرات أو التركيبات أو الجرعات الفعالة المستهدفة ؛ المرحلة المتأخرة من الأدوية المرشحة أو التي تم وضعها على الرف للمساعدة في تحديد الأكثر احتمالية للاستجابة بشكل إيجابي ؛ وأدوية مسوقة أو عامة لمؤشر سرطان جديد أو مختلف على مجموعة محددة من المرضى.
منصة ذكاء اصطناعي تم اختبارها في المعارك لعلم الأورام الدقيق
يتحدث من حيث النتائج الفعلية ، Lantern Pharmain أعلنت للتو تخليص إدارة الغذاء والدواء (FDA) من تطبيق العقار الجديد التجريبي (IND) لـ LP-184 ، وهو جزيء صغير جديد وقاتل صناعيًا تم تطويره داخليًا بالكامل - باستخدام رؤى من منصة Lantern's AI ، RADR®. من المتوقع أن تبدأ التجربة السريرية الأولى من نوعها في الإنسان لـ LP-1 هذا الصيف لأورام صلبة متعددة وسرطانات الدماغ والجهاز العصبي المركزي (CNS).
في وقت سابق من مارس 2023 ، نجحت Lantern Pharma في تحقيق ذلك جرعات أول مريض في المرحلة 2 تجربة سريرية متعددة المراكز Harmonic ™ ، مما يشير إلى علامة بارزة في تطوير دواء الأورام. من خلال الاستفادة من منصة التعلم الآلي RADR® AI ومنصة التعلم الآلي ، تقوم الشركة بتحويل الاستراتيجيات العلاجية للمرضى المحرومين من الخدمات ، مثل الذين لم يدخنوا مطلقًا مع سرطان الرئة ذو الخلايا غير الصغيرة المتقدمة. والجدير بالذكر أنه في تجربة سابقة من المرحلة 3 ، أظهر المرضى الذين تلقوا LP-300 الخاص بالشركة مع العلاج الكيميائي زيادة في معدلات البقاء على قيد الحياة ، مما يدل على الفعالية المحتملة لنهج Lantern. مع وجود ما يقدر بـ 24,000 إلى 30,000 شخص لم يدخنوا أبدًا مع NSCLC في الولايات المتحدة في عام 2021 وحده ، فإن الضرورة والتأثير المحتمل لمثل هذه العلاجات كبيرتان.
في وقت سابق من هذا العام ، فانوس أيضا حصل بنجاح على تسمية الأدوية اليتيمة (ODD) من إدارة الغذاء والدواء (FDA) لـ LP-284، العقار الجديد المرشح لعلاج سرطان الغدد الليمفاوية لخلية الوشاح (MCL). تم تحقيق هذا التقدم المدعوم بالذكاء الاصطناعي في اكتشاف وتطوير عقاقير الأورام في أقل من عامين ، مما يدل على قدرة المنصة على تغيير وتيرة وفعالية تقديم علاجات جديدة إلى السوق. LP-284 هو رابع ODD في خط أنابيب Lantern Pharma ، المرشحون الأوائل الذين وصلوا إلى هذا الإنجاز هم في سرطان البنكرياس ، والورم الأرومي الدبقي ، والأورام الخبيثة غير النمطية (ATRT) لاستخدام الأطفال (انظر الرسم التوضيحي لخط الأنابيب أدناه). تعمل حالة ODD ، التي توفر مزايا كبيرة مثل سبع سنوات من التفرد في السوق وبرامج التطوير المعجلة ، على ترسيخ مسار التطوير الإكلينيكي والآفاق التجارية لمرشحي الأدوية المرشحة لشركة Lantern Pharma LP-284 و LP-184 و STAR-001.
في مارس ، أنشأت Lantern Pharma شركة فرعية ، Starlight Therapeutics ، مكرسة لتطوير علاجات للجهاز العصبي المركزي (CNS) وسرطانات الدماغ ، بمساعدة منصة RADR® AI التحولية. سهلت المنصة المدعومة بالذكاء الاصطناعي التطور السريع لـ STAR-001 ، المرشح الرائد في Starlight ، والذي أثبت فعاليته في مختلف نماذج سرطان الدماغ والجهاز العصبي المركزي. من المقرر إجراء التجارب السريرية لمؤشرات سرطان الجهاز العصبي المركزي الجديدة للبالغين والأطفال ، والتي تم تحديدها وتحديد أولوياتها مع رؤى من منصة RADR® AI ، في أواخر عام 2023 وأوائل عام 2024.
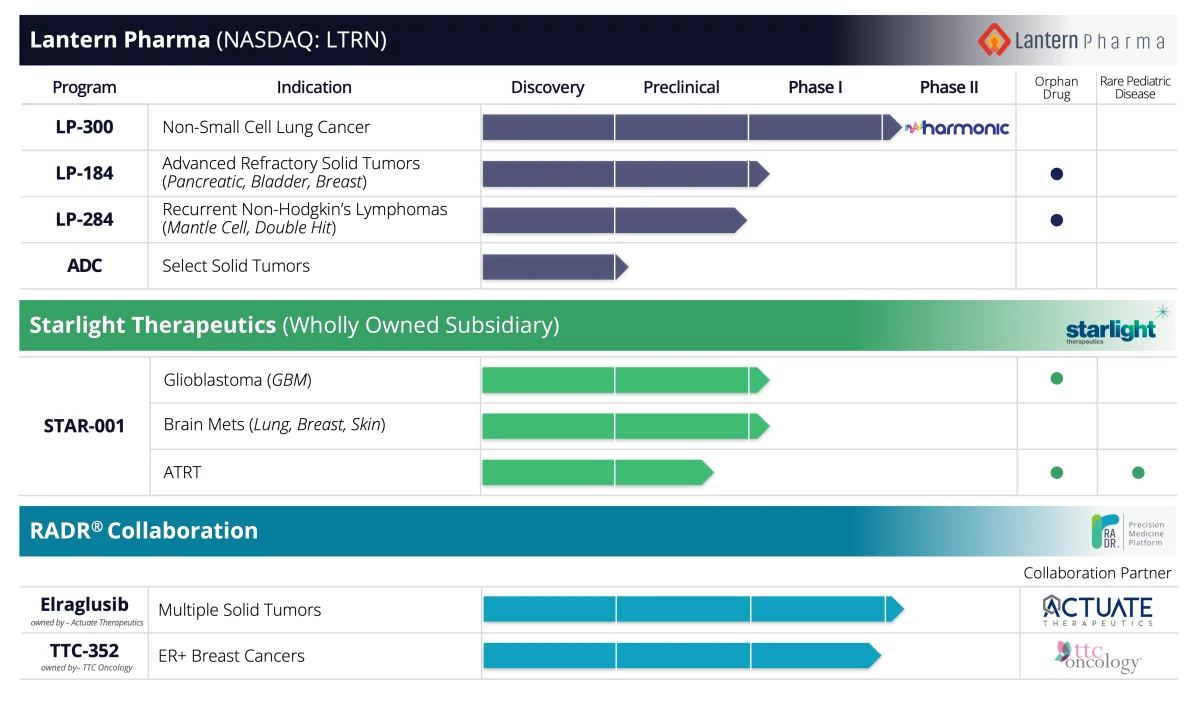
رصيد الصورة: Lantern Pharma. خط أنابيب الشركة للأورام ، الذي تم تمكينه بواسطة منصة اكتشاف الأدوية RADR® التي يقودها الذكاء الاصطناعي.
تشتمل محفظة Lantern Pharma على أربعة أدوية مرشحة ، بما في ذلك برنامجين من برامج المرحلة الثانية ، وبرنامج اقتران الأجسام المضادة والأدوية (ADC) عبر 2 مؤشرًا للسرطان ، وعددًا متزايدًا من البرامج الشريكة. من خلال الاستفادة الفعالة من منصة RADR® المدعومة بالذكاء الاصطناعي ، تقدم الشركة فرصة واعدة لأصحاب المصلحة في الصناعة الذين يسعون إلى تعزيز خطوط الأنابيب العلاجية الخاصة بهم.
تطوير اكتشاف أدوية الأورام من خلال الشراكات
توفر Lantern Pharma حلاً جديدًا للمشهد الذي غالبًا ما يمثل تحديًا لتطوير عقاقير علاج الأورام. تستخدم منصة RADR® الخاصة بهم مزيجًا متطورًا من علم الجينوم والذكاء الاصطناعي (AI) لإعادة توظيف وتنشيط عقاقير المرحلة السريرية التي تم إيقافها سابقًا. من خلال تحديد المؤشرات الحيوية والتحقق من صحتها لاستجابة المريض ، تعمل Lantern Pharma على تعزيز القيمة المحتملة لهذه العلاجات بشكل فعال ، مما يوفر فرصة مربحة للشركاء الذين يتطلعون إلى تحسين خطوط أنابيب الأورام الخاصة بهم وربما إحياء الأدوية المرشحة الفاشلة.
بدلاً من إنشاء الأدوية من الألف إلى الياء ، تتخذ Lantern Pharma نهجًا استراتيجيًا من خلال التركيز على الأدوية السريرية في المراحل المتأخرة التي أظهرت فعاليتها في مجموعات معينة من المرضى ولكن تم إيقافها بخلاف ذلك. باستخدام علم الجينوم المتقدم وتحليلات البيانات والذكاء الاصطناعي ، فإنهم `` ينقذون '' هذه الأدوية القيمة ويعيدون توجيهها نحو مجموعات المرضى المحددة التي تم تحديدها من خلال التنميط الجزيئي. تسمح هذه العملية بمعالجة طبقية وفعالة للمرضى ضمن التجارب السريرية المركزة ، بما في ذلك برامج التعاون المستمر لشركة Lantern Pharma مع Actuate Therapeutics (Elraglusib ، في المرحلة 2) ، و TTC Oncology (TTC-352 ، في المرحلة 1).
على سبيل المثال ، تمكنت منصة RADR® AI من Lantern Pharma من التنبؤ باستجابة Elraglusib للورم الميلانيني النقيلي ، المقاوم لمثبطات نقاط التفتيش ، بدقة 88٪ - لمجموعة من 26 مريضًا.
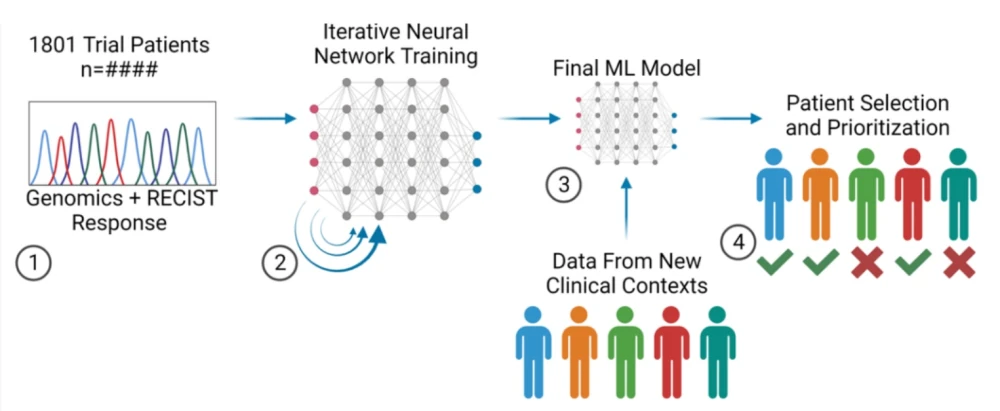
تطوير نموذج التعلم الآلي للتنبؤ باستجابة المريض Elraglusib بإدخال الجينوم.
رصيد الصورة: من ASCO 2023 ملصق رقم 3079.
عند إعادة استخدام الدواء بنجاح وتحديد العلامات الحيوية التشخيصية للاستجابة للأدوية ، تفتح Lantern Pharma فرصًا للترخيص أو الشراكات. تعزز استراتيجيتهم الفريدة تطوير علاجات دقيقة مع معالجة الاحتياجات الكبيرة التي لم تتم تلبيتها في سوق الأورام في الوقت نفسه ، مما يجعل Lantern Pharma شريكًا مثاليًا للمؤسسات التي تتطلع إلى تحسين إستراتيجية تطوير علم الأورام لديها.
في قطاع تطوير أدوية الأورام ، تبرز Lantern Pharma من خلال منصتها التي تعتمد على الذكاء الاصطناعي ، RADR® ، مما يساعد في الكشف عن آليات عمل جديدة (MoAs) لأصول علم الأورام ، وتمكين تطوير المرشح قبل السريري المستند إلى البيانات ، وتحديد المؤشرات العلاجية الجديدة ، واشتقاق مؤشرات حيوية جديدة من أجل علم الأورام الدقيق ، والتنبؤ باستجابات المرضى لعلاجات السرطان ، يقوم RADR® بتكرير التجارب السريرية ويمكن أن يزيد من الفرص في الرحلة نحو موافقة إدارة الغذاء والدواء. لكن ابتكاراتهم لا تتوقف عند هذا الحد. كما قاموا بإنقاذ الأدوية المرشحة على الرف ، ومنحهم فرصة ثانية للحياة.
لا يمكن التغاضي عن الوعد الذي يحمله نموذج Lantern Pharma الفريد للمجتمع العلمي الأوسع. تمتلك الشركة تاريخًا من الشراكات الناجحة مع المنظمات الرائدة ، بما في ذلك Actuate Therapeutics ، و TTC Oncology ، و John Hopkins ، و Fox Chase ، و UT Health San Antonio ، ومركز أبحاث جمعية السرطان الدنماركية ، و Mayo Clinic ، وغيرها. على سبيل المثال ، في تعاون حديث مع المعهد الوطني للسرطان (الولايات المتحدة) ، استخدمت Lantern Pharma منصتها للذكاء الاصطناعي ، RADR® ، للمساعدة في اكتشاف عامل ضار للحمض النووي للسرطان النادر جدًا المعروف باسم أورام ربودية مسخية غير نمطية ( ATRT) ، تقدم تمت مناقشته في ورقة منشورة حديثًا.
تشير رحلة الشركة إلى مستقبل يصبح فيه علاج السرطان شخصيًا وتقوده الدقة. بالنسبة لأولئك المعنيين بمكافحة السرطان ، فإن التفكير في التعاون مع الذكاء الاصطناعي في رواد اكتشاف الأدوية مثل Lantern Pharma يمكن أن ينير الطريق إلى الحلول التحويلية في علم الأورام.
المواضيع: شركات التكنولوجيا الحيوية
- محتوى مدعوم من تحسين محركات البحث وتوزيع العلاقات العامة. تضخيم اليوم.
- تمويل EVM. واجهة موحدة للتمويل اللامركزي. الوصول هنا.
- مجموعة كوانتوم ميديا. تضخيم IR / PR. الوصول هنا.
- أفلاطونايستريم. ذكاء بيانات Web3. تضخيم المعرفة. الوصول هنا.
- المصدر https://www.biopharmatrend.com/post/690-unveiling-lantern-pharmas-success-story-in-ai-powered-precision-oncology/



