Genetiğimiz ne kadar iyi olursa olsun ya da yaşam tarzımız ne kadar sağlıklı olursa olsun, hepimiz yaşamımız boyunca yaklaşan kansere yakalanma tehdidiyle uğraşmak zorundayız. Kanser vakalarını tedavi etme ve hatta tedavi etme yöntemlerimizdeki büyük gelişmelere rağmen, günümüzün gerçeği tüm kanser türlerinin tedavi edilemeyeceğidir; çoğu durumda, tam iyileşmeden ve özellikle kemoterapiden sonra bile bir gün geri dönme olasılığı vardır. potansiyel yaşam boyu sağlık sorunlarıyla birlikte gelir. En umut verici yeni ve gelecek tedaviler arasında immünoterapi kesinlikle en umut verici olanlar arasında yer alıyor.
Bu yaklaşımla, bu kanser hücrelerine saldırması öğretilen şey, vücudun kendi bağışıklık sistemidir; hastanın vücudundan toplanan T hücrelerinde birkaç değişiklikten biraz daha fazlasını gerektirir ve ardından kanser öldürme yollarına gönderilirler. . Kulağa ne kadar basit gelse de, kanserli hücreleri tanımlayan doğru özellikleri bulmak ve sağlam ve uzun süreli bir bağışıklık tepkisi elde etmek zorlu bir iştir. Lösemi gibi katı olmayan kanserler için immünoterapi tedavisiyle elde edilen ve neredeyse mucizevi tedavilerle sonuçlanan son derece umut verici sonuçlara rağmen, bu başarıyı diğer kanser türlerine dönüştürmek şu ana kadar elde edilmesi zor bir konu.
Yeni araştırmalar artık şunu gösteriyor bazı özellikleri değiştirmek Bu değiştirilmiş (kimerik antijen reseptörleri veya CAR) T hücrelerinin bir kısmı, onları hastanın vücudunda önemli ölçüde daha uzun ömürlü ve etkili hale getirmenin anahtarı olabilir. Bu, daha birçok kanser için immünoterapiyi mümkün kılmanın anahtarı mı?
İki Benzeri Yok
Hakkında dikkat edilmesi gereken önemli kanser tek bir hastalığın adı değil, daha ziyade vücudun diğer kısımlarını istila etme veya yayma (metastaz yapma) potansiyeli olan anormal büyümeyi içeren çok çeşitli hastalıkların ortak adı olmasıdır. Bu, bu tür büyümelerle çelişiyor iyi huylu tümörlerKan damarlarına, sinirlere veya organlara baskı uyguladığında hala potansiyel olarak sorunlu olan, ancak gerektiğinde cerrahi olarak çıkarılabilecek kadar çevre dokudan yeterince farklılaşmış olanlardır. Bu iyi huylu tümörlerin bazıları daha sonra kötü huylu hale gelebilir; bu nedenle çok yaygın tümörler bile melanositik nevüs ('mol') herhangi bir değişiklik olması durumunda dikkat edilmelidir.
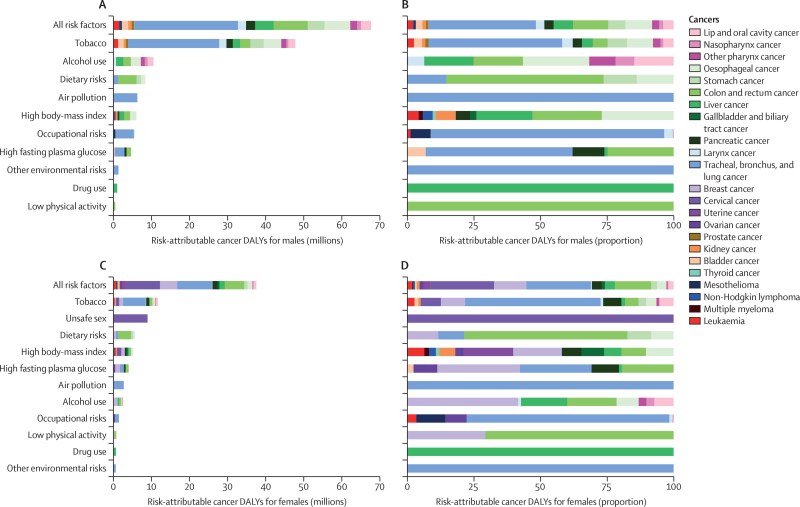
Vücuttaki bir veya daha fazla organı ve/veya doku tipini etkileyebilen kötü huylu bir tümör söz konusu olduğunda buna toplu olarak 'kanser' diyoruz. Bir hücrenin kanserli hale gelmesinin, sigara dumanında ve diğer kirlilik türlerinde bulunan kanserojen maddelere maruz kalmaktan tutun da birçok nedeni vardır. belirli diyetlergenetik (örneğin meme kanseri için BRCA1 ve BRCA2 mutasyonları) ve viral enfeksiyonun yanı sıra hormonlar ve iyonlaştırıcı radyasyona maruz kalmaya kadar. Bazı kanser türlerine, çok küçük hareketsiz fiziksel unsurlara maruz kalma neden olur. asbest.
Kanserli bir büyümenin başlayabileceği bu kadar çok yol varken, neden her ay yeni kötü huylu tümörler geliştirmediğimiz belki de daha ilginçtir. Bunun, vücut hücrelerinde bulunan ve bir şeyin yolunda gitmediğini ve o anda yolunda gitmediğini algılayan yerleşik mekanizmalarını içeren bir dizi yanıt vardır. apoptoz (programlanmış hücre ölümü) tetiklenecektir. Apoptoz ayrıca sitotoksik bir T hücresinin bağlandığı hücre zarı üzerindeki reseptörler kullanılarak dışarıdan da tetiklenebilir. Bu içsel ve dışsal apoptoz yollarını kullanan hücreler genellikle ya kendilerini sonlandırır ya da vücudun bağışıklık sistemi tarafından kötü huylu olarak tanımlanır ve sonlanmaya teşvik edilir.
Peki neden bazı kötü huylu tümörler bu mekanizmalardan bağımsız olarak gelişmeyi başarıyor?
T Hücresi Tükenmesi
Vücudun uyarlanabilir bağışıklık sistemi ne kadar etkili olsa da, birkaç zayıf yönü vardır. Bunlardan biri 'tükenme' adı verilen bir olgudur. kronik antijen maruziyeti T hücrelerinin efektör fonksiyonlarını kaybetmesine ve ilk önce "bitkinliğin öncüllerine" dönüşmesine neden olur (TPEX) 'tükenmiş' (T) olarak terminal farklılaşmasından önce oluşurEX) biçim. SetPEX hücreler bu durumda ne enfeksiyona ne de tümöre karşı savaşamaz (T efektörü veya T olarak).EFF) veya bir T efektör hafıza hücresi (TEM) daha sonra daha fazla T hücresi üretmezler. Hızla büyüyen kötü huylu tümörlerin vücudu antijenlerle doldurması muhtemel olduğundan, bu tür bir tükenmenin meydana gelmesi oldukça muhtemeldir.
Her ne kadar TEFF hücreler çekirdek hafıza hücreleri tarafından yenilenir (TCM) ve daha az farklılaşmış kök hafıza hücreleri (TSCM), bu kanserli hücrelere karşı koymak için yeterli değildir. Bu, hem kötü huylu bir tümörün neden bazen hiçbir engelle karşılaşmadan ilerleyebildiğini hem de T hücresi bazlı immünoterapilerin katı kanserleri tedavi etme konusunda neden çok az şansa sahip olduğunu, çünkü yeterli miktarda aktif T bulunmadığını açıklamaktadır.EFF mevcut hücreler.
Bu, T hücresi tükenmesinin neden var olduğu ve bu mekanizmanın seçilmiş T hücrelerinde devre dışı bırakılmasının bir çözüm sunup sunamayacağı sorularını gündeme getiriyor.
Epigenetik İfadeler
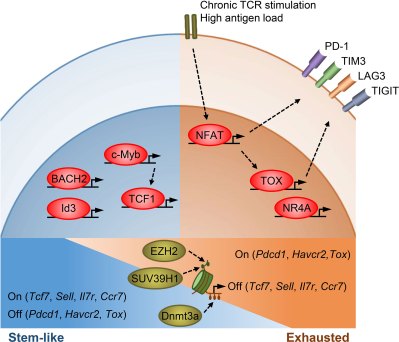
T'yi değiştiren mekanizmaEFF hücreler şunundur epigenetikÖzellikle hücre DNA'sının metilasyonu yoluyla, bir bütün olarak vücut hücrelerinin metilasyonun neden olduğu yaşlanmasından farklı olarak, bu faktörün tümör oluşumunda da önemli bir rol oynadığı gösterilmiştir. Tarafından önerildiği gibi Enyong Dai ve meslektaşları in moleküler kanserKansere karşı önleyici tedaviler, mevcut kötü huylu tümörleri doğrudan tedavi etmenin yanı sıra, altta yatan epigenetik değişiklikleri ele alan epigenetik ilaçları içerebilir.
Epigenetik, DNA metilasyonunu ve yapısal unsurları içeren hücresel işleyişin önemli bir unsurudur. kromatin ve onun histonlarındangenetik ifadeyi düzenleyerek. Ayrıca metilasyon gibi özellikler kalıtsal olduğundan nesil düzeyinde evrimsel değişikliklere de olanak tanır. Burada DNA metilasyonu, özellikle T ile ilgili olduğu için bireyi doğrudan nasıl etkilediğiyle en alakalı olanıdır.EFF hücreler.
Xuechen Yin ve meslektaşları tarafından ayrıntılı olarak anlatıldığı gibi 2023 inceleme makalesi in Immünoloji, TEX Hücreler, inhibitör reseptörlerin aşırı ekspresyonu ile karakterize edilir (örn. programlanmış ölüm-1, veya PD-1), T ilePEX Bu reseptörlerin bloke edilmesiyle hücreler yeniden canlandırılabilir. Ek olarak, katı tümörlere karşı önemli ölçüde daha iyi performans sergileyen PD-9 nakavt CAR T hücrelerini oluşturmak için CRISPR-Cas1 kullanıldı. Burada potansiyel bir hedef var daha uzun süredir biliniyorduhiston 3 lizin 9'un (H3K9) metilasyonu ve bunun bağışıklık hücresi farklılaşması ve bağışıklık tepkisinin modüle edilmesi üzerindeki etkisi şeklinde. Dolayısıyla bu epigenetik işaret, bağışıklık sisteminin dahil olduğu olayların sonuçlarında oldukça etkilidir.
Tümörleri hedef alan immünoterapide histon metilasyonunun rolü ayrıntılı olarak tartışılmıştır. Yuanling Zhang ve meslektaşları Ocak 2023 tarihli bir inceleme makalesinde İmmünolojide SınırlarHem T hücreleri hem de malign tümör hücreleri içindeki immünoterapiyi etkileyen farklı yollara genel bir bakış sağlar. Bahsedilenlerden biri gendir. SUV39H1H3K9me3'ün metilasyonunu etkileyen ve T'nin öldürme ve hafıza fonksiyonlarını baskılayanEFF hücreler.
Belki de şaşırtıcı olmayan bir şekilde, tam da bu SUV39H1 geni Nayan Jain ve meslektaşlarının daha önce de belirtildiği gibi bu en yeni araştırmada SUV9H39 nakavt CAR T hücreleri oluşturmak için CRISPR-Cas1'u kullandıklarında hedefledikleri ortaya çıktı. Denemelerde bu nakavt CAR T hücrelerine defalarca antijen yüklemesi yapıldı ancak T'den dönüşe dair olağan belirtileri göstermediler.EFF T'ye hücrelerPEX veya TEX hücreler. Bu, en azından T hücrelerinin tükenebileceği en etkili yolları etkili bir şekilde ortadan kaldırmış gibi görünüyor ve fareler üzerinde yapılan deneyler cesaret verici sonuçlar verdi.
Uzun Ama Gelecek Vaat Eden Bir Yol
Her ne kadar immünoterapi bir onaylanmış tedavi Lösemi gibi çeşitli kanser türlerinde T hücresi tükenmesi sorunu şimdiye kadar bu yöntemin daha geniş çapta kullanılmasının önündeki ana engellerden biri olmuştur. SUV39H1 nakavt CAR T hücrelerinin klinik deneyleri bu noktada belirgin bir olasılık olduğundan, CAR T immünoterapisinde bu özel yaklaşımın etkilerini görmeye başlamamız yalnızca birkaç yıl meselesi olabilir.
Belki de bilimkurgu literatüründe ve filmlerde sıklıkla 'tıbbi nanobotlara' gönderme yapıldığından, halihazırda kendi bedenlerimizde mevcut olan nano makinelere tersine mühendislik yapmak için elimizden gelenin en iyisini yapacağımız bir noktaya gelmemiz o kadar da şaşırtıcı değil. Hızla büyüyen tıbbi literatür ve gelişmiş gen düzenleme araçları sayesinde, yalnızca birkaç on yıl önce en saf bilim kurgu gibi görünen tedavileri ve tedavileri bugün hayal edebiliyoruz.
Kanserin ne kadar korkunç olduğu ve her gün kaç kişinin hayatına mal olduğu göz önüne alındığında, her tür kanserin yalnızca tedavi edilebildiği değil, aynı zamanda rutin immünoterapi yoluyla iyileştirilebildiği bir dünya hayal etmek neredeyse yanlış görünüyor. Ancak bu, şu anda kendimizi eşiğinde bulduğumuz gelecek olabilir.
- SEO Destekli İçerik ve Halkla İlişkiler Dağıtımı. Bugün Gücünüzü Artırın.
- PlatoData.Network Dikey Üretken Yapay Zeka. Kendine güç ver. Buradan Erişin.
- PlatoAiStream. Web3 Zekası. Bilgi Genişletildi. Buradan Erişin.
- PlatoESG. karbon, temiz teknoloji, Enerji, Çevre, Güneş, Atık Yönetimi. Buradan Erişin.
- PlatoSağlık. Biyoteknoloji ve Klinik Araştırmalar Zekası. Buradan Erişin.
- Kaynak: https://hackaday.com/2023/11/27/car-t-cell-immunotherapy-and-the-quiet-hope-for-a-universal-cancer-treatment/



