Adaptif bağışıklık sistemi, patojenleri ve tümör hücrelerini hedef almak ve yok etmek için tasarlanmış özel hücrelerden ve biyokimyasal yollardan oluşur. Bu genellikle istilacı organizmalar veya tümör transformasyonu tarafından indüklenen değişikliklerden kaynaklanan anormal protein belirteçlerini eksprese eden hücrelerin tanınmasıyla elde edilir.
Enfekte veya tümör hücrelerinin yok edilmesinde rol oynayan birincil hücre tipi sitotoksik T hücreleri.[1] Özel sitotoksik T hücrelerinin genişletilmesini ve tasarlanmasını içeren immünoterapiler neredeyse on yıldır kullanılmaktadır.
Tümör hücresi hedefleme durumunda immünologlar arasında hakim olan görüş, bireysel T hücrelerinin yalnızca belirli bir tümör antijenini tanır.[2] Bununla birlikte, tümöre infiltre eden lenfositler (TIL'ler) üzerine yapılan yeni bir çalışma, bazı T hücrelerinin aslında birden fazla tümör antijenini hedefleyebileceğini öne sürüyor.
Çalışma Geçmişi
Danimarka'daki Herlev Hastanesi ve İngiltere'deki Cardiff Üniversitesi'nden ortak bir grup tarafından yürütülen araştırma, şaşırtıcı varlığı ortaya çıkardı. Farklı tümör antijenlerini tanıyabilen tek T hücreleri.[3]
Araştırmacılar, başarılı immünoterapi sonuçlarına sahip hastalar ile kanserden kurtulmayan hastalar arasındaki biyolojik farklılıkları anlamak istedi. Çalışma, evre IV melanomu olan ve tümör infiltre edici lenfosit tedavisi (TIL tedavisi) yoluyla tedavi edilen birkaç hastayı içeriyordu.
TIL'ler, tümör hücrelerini anormal olarak tanıyan, tümöre nüfuz eden T hücreleridir. TIL tedavisi için, TIL'ler cerrahi olarak rezeke edilmiş veya biyopsi yapılmış bir tümörden toplanır ve laboratuvarda genişletilir. Daha sonra çok sayıda TIL hastaya geri verilir.
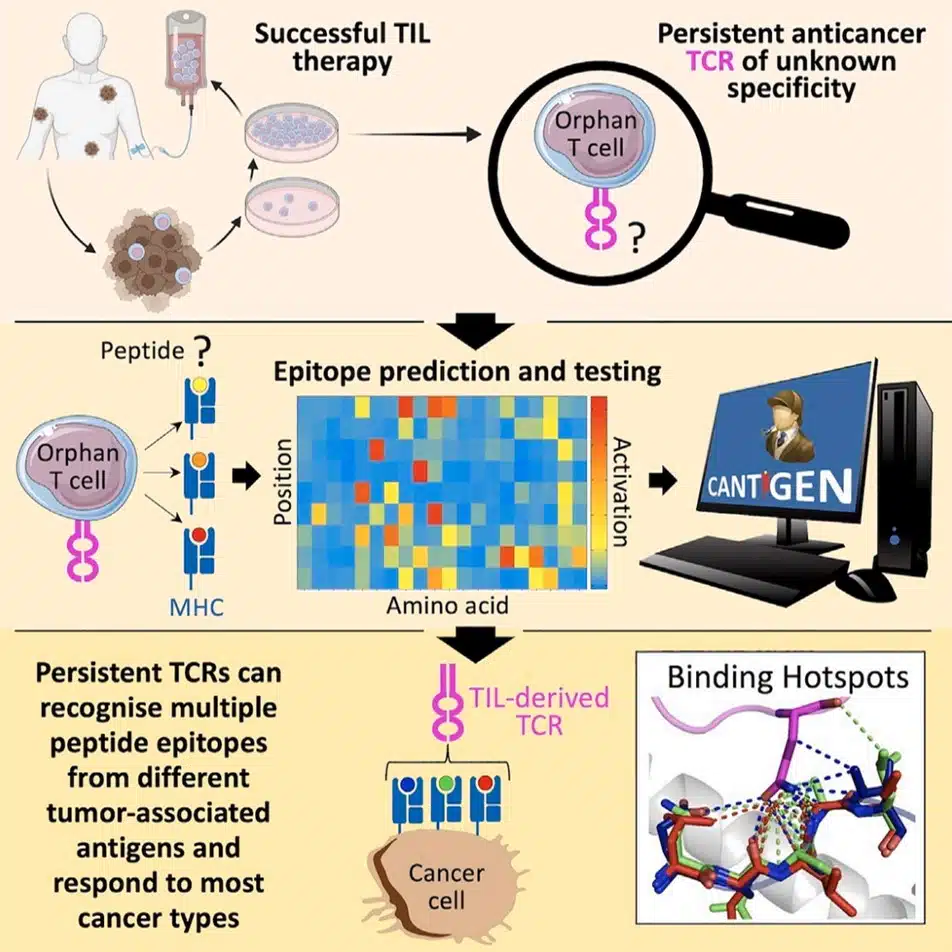
“Çok Uçlu” T Hücrelerinin Keşfi
Çalışma, T hücreleri tarafından hedeflenen antijenleri belirlemek için uzun süreli melanom remisyonu elde eden hastaların TIL infüzyon kaynağının analiz edilmesini gerektirdi. Proteomik teknolojiler T hücreleri tarafından tanınan kanserle ilişkili epitopları tanımlamak için kullanıldı.[4]
TIL infüzyon ürünü içindeki T hücresi klonlarının aynı anda üç farklı antijen epitopuna yanıt verdiği bulundu. Keşfedilen tanınmış epitoplardan ikisi yeni tanımlanmıştır. Kansere özgü T hücresi reseptörlerinin, TIL tedavisinden yıllar sonra da devam ettiği bulundu.
Ayrıca çarpıcı olan, tümörle ilişkili antijen tanımanın aditif olması ve bunun, yalnızca bir antijeni tanıyan geleneksel T hücrelerine kıyasla daha üstün tümör hücresi tanımayla sonuçlanmasıdır. Bu "çok uçlu" T hücrelerinin tedaviye rağmen kanseri ilerleyen hastalarda bulunmadığının gözlemlenmesi, bu T hücrelerinin kanserin temizlenmesi veya gerilemesinde anahtar rol oynadığını düşündürmektedir.
Gelecekteki İmmünoterapilere Yönelik Çıkarımlar
Kanser hücreleri yapabilir geleneksel T hücreleri tarafından tanınan bir antijenin ekspresyonunun durdurulması,ve bu kaçınma mekanizması, kanserin bir hastada genişlemeye devam etmesine izin verir.[5]
Kanser hücrelerinin bu biyolojik avantajı, birden fazla kanser hücresi antijenini tanıyabilen T hücreleri tarafından aşılabilir. Aynı anda birden fazla tümör antijenini tanıyabilen bireysel T hücrelerinin keşfi, onkologlar için üstün kanserle mücadele araçlarının geliştirilmesine yol açabilir.
Keşfedilen çok uçlu T hücreleri, bir kanser hücresinin yüzeyindeki birden fazla epitopu tanıyabilir; bu nedenle çok uçlu T hücrelerine dayanan immünoterapiler, kanser temizleme tedavilerinin etkinliğini artırabilir. Bu hücreler aynı zamanda farklı kanser türlerini hedef alabilecek tedaviler tasarlama yeteneğini de geliştirebilir.
Bildirilen çalışmadaki az sayıda hasta göz önüne alındığında, daha fazla sayıda TIL ile tedavi edilen hayatta kalan katılımcıya sahip bir çalışma, çok yönlü T hücresi popülasyonunun daha iyi tanımlanması ve bulguların doğrulanması açısından değerli olacaktır.
Bu konu hakkında daha fazla bilgi edinmek istiyorsanız, ilgili içeriğimizden bazılarına göz atın. ortaya çıkan hücre tedavileri ve T hücrelerinin biyolojisi.
Referanslar
[1] Barry, M., Bleackley, R. Sitotoksik T lenfositleri: tüm yollar ölüme çıkar. Nat Rev Immunol 2, 401–409 (2002). https://doi.org/10.1038/nri819. [2] Zamora AE, Crawford JC, Thomas PG. Hedefi Vurmak: T Hücreleri Tümörleri Nasıl Tespit Ediyor ve Ortadan Kaldırıyor? J İmmünol. 2018 15 Ocak;200(2):392-399. doi: 10.4049/jimmunol.1701413. PMID: 29311380; PMCID: PMC6116355. [3] Dolton ve diğerleri, 2023, Hücre 186, 3333–3349 3 Ağustos 2023 ª 2023 Yazarlar. Elsevier Inc. tarafından yayınlanmıştır. https://doi.org/10.1016/j.cell.2023.06.020. [4] Bilal Aslam ve diğerleri, Proteomik: Teknolojiler ve Uygulamaları, Kromatografik Bilim Dergisi, Cilt 55, Sayı 2, 1 Şubat 2017, Sayfa 182–196, https://doi.org/10.1093/chromsci/bmw167. [5] Kim SK, Cho SW. Tümör Mikro Ortamında Kanser Bağışıklığının Kaçınma Mekanizmaları ve İlaç Müdahalesi. Ön Farmakol. 2022 Mayıs 24;13:868695. doi: 10.3389/fphar.2022.868695.
- SEO Destekli İçerik ve Halkla İlişkiler Dağıtımı. Bugün Gücünüzü Artırın.
- PlatoData.Network Dikey Üretken Yapay Zeka. Kendine güç ver. Buradan Erişin.
- PlatoAiStream. Web3 Zekası. Bilgi Genişletildi. Buradan Erişin.
- PlatoESG. karbon, temiz teknoloji, Enerji, Çevre, Güneş, Atık Yönetimi. Buradan Erişin.
- PlatoSağlık. Biyoteknoloji ve Klinik Araştırmalar Zekası. Buradan Erişin.
- Kaynak: https://cytologicsbio.com/study-reveals-tcells-capable-of-targeting-multiple-tumor-antigens-simultaneously/



