<!–
->
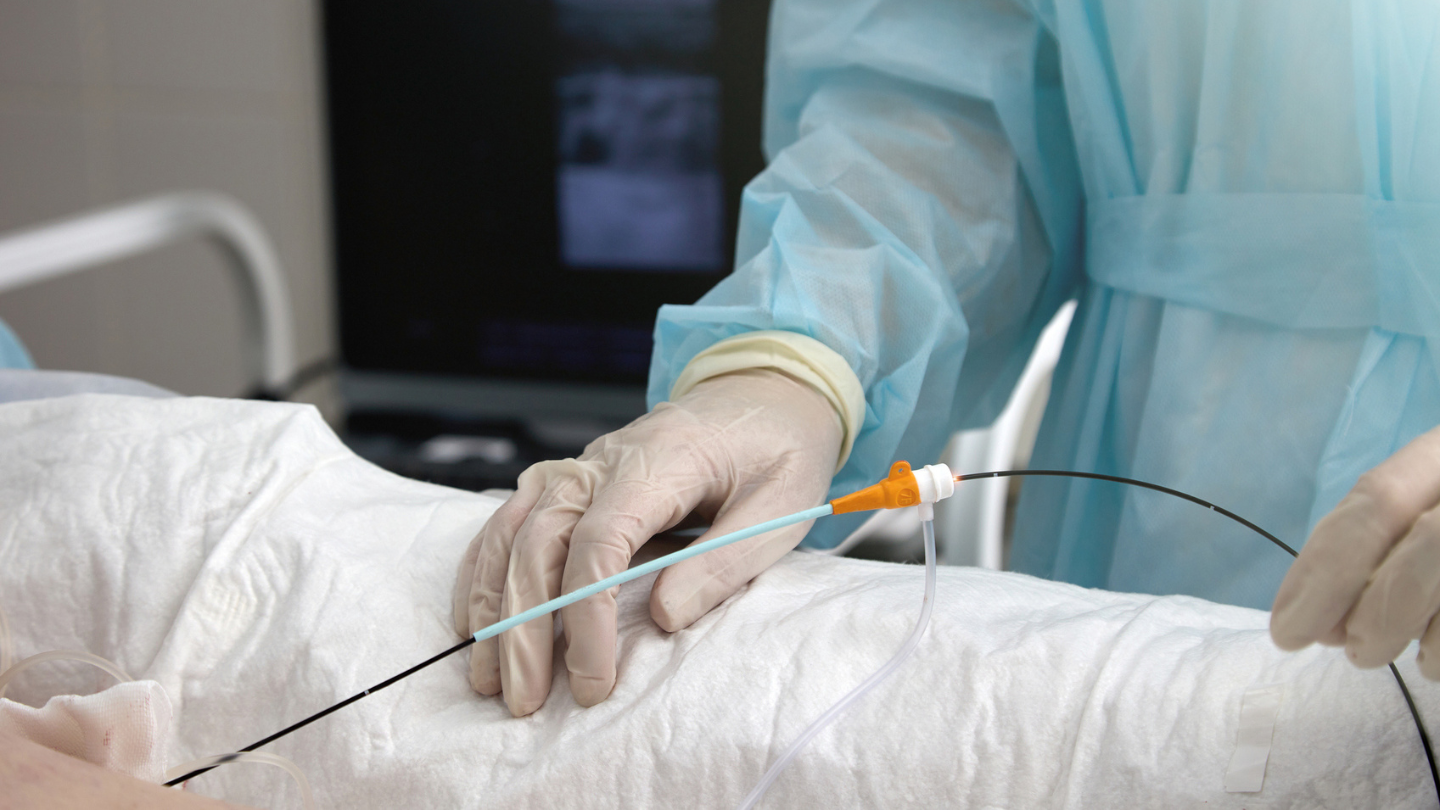
Firma Citius Pharmaceuticals osiągnęła ważny kamień milowy w badaniu klinicznym terapii Mino-Lok (MLT), antybiotykowego roztworu zabezpieczającego do ratowania cewników u pacjentów z zakażeniami krwi związanymi z cewnikami.
Citius uważa, że wszystkie 92 zdarzenia wymagane do ukończenia próby zostały osiągnięte, jednak oczekuje na potwierdzenie przez niezależnych recenzentów. Część pacjentów pozostaje w aktywnym leczeniu.
MLT to nowatorska terapia blokująca antybiotyk, która łączy minocyklinę z wersenianem disodowym w leczeniu pacjentów z infekcjami krwi związanymi z cewnikiem. Obecne leczenie polega na klinicznym usunięciu i wymianie centralnego cewnika żylnego (CVC), dla którego terapia stanowi alternatywę.
Jeśli zostanie zatwierdzony, MLT, który Licencja Citiusa z The University of Texas MD Anderson Cancer Center, byłby pierwszym i jedynym lekiem zatwierdzonym przez FDA, który ratuje centralne cewniki żylne powodujące infekcje krwi związane z linią centralną. MLT uzyskał kwalifikację produktu do zwalczania chorób zakaźnych oraz oznaczenie szybkiej ścieżki od Amerykańskiej Agencji ds. Żywności i Leków (FDA). To posiada ochronę patentową do 2024 r. i ochrona patentowa preparatu do 2036 r.
Prezes i dyrektor generalny Leonard Mazur powiedział: „To ważny kamień milowy dla Citius, ponieważ zbliżamy się do zakończenia III fazy badań Mino-Lok. Gdy zakończymy terapię pacjentów w trakcie aktywnego leczenia, będziemy nadal rejestrować pacjentów w kolejce i inicjować działania zamykające.”
Projekt próbny Mino-Lok Faza III
Badanie III fazy MLT (NCT02901717), które jest prowadzone w Stanach Zjednoczonych i Indiach, jest wieloośrodkowym, randomizowanym, otwartym, zaślepionym badaniem mającym na celu określenie skuteczności i bezpieczeństwa MLT. Pierwszorzędowym punktem końcowym jest czas do uszkodzenia cewnika. Dodatkowe drugorzędowe miary wyniku obejmują ogólny sukces, eradykację mikrobiologiczną i wyleczenie kliniczne.
Pacjenci, którzy spełniają wszystkie kryteria niezbędne do badania, są losowo przydzielani w stosunku 1:1 do grupy otrzymującej MLT lub standardową terapię antybiotykową. Pacjenci w ramieniu MLT otrzymują dzienną dawkę przez siedem dni. W przypadku pacjentów w ramieniu kontrolnym badacz określa antybiotyk zastosowany w blokadzie, dawkę, czas przebywania i liczbę dni podawania w oparciu o standardy instytucjonalne lub wytyczne Amerykańskiego Towarzystwa Chorób Zakaźnych (IDSA).
<!– GPT AdSlot 3 dla jednostki reklamowej „Verdict/Verdict_In_Article” ### Rozmiar: [[670,220]] —
!– Koniec boksu reklamowego 3 –>
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- PlatoData.Network Pionowe generatywne AI. Wzmocnij się. Dostęp tutaj.
- PlatoAiStream. Inteligencja Web3. Wiedza wzmocniona. Dostęp tutaj.
- PlatonESG. Motoryzacja / pojazdy elektryczne, Węgiel Czysta technologia, Energia, Środowisko, Słoneczny, Gospodarowanie odpadami. Dostęp tutaj.
- Platon Zdrowie. Inteligencja w zakresie biotechnologii i badań klinicznych. Dostęp tutaj.
- ChartPrime. Podnieś poziom swojej gry handlowej dzięki ChartPrime. Dostęp tutaj.
- Przesunięcia bloków. Modernizacja własności offsetu środowiskowego. Dostęp tutaj.
- Źródło: https://www.clinicaltrialsarena.com/news/citius-reaches-milestone-mino-lok/



