개요
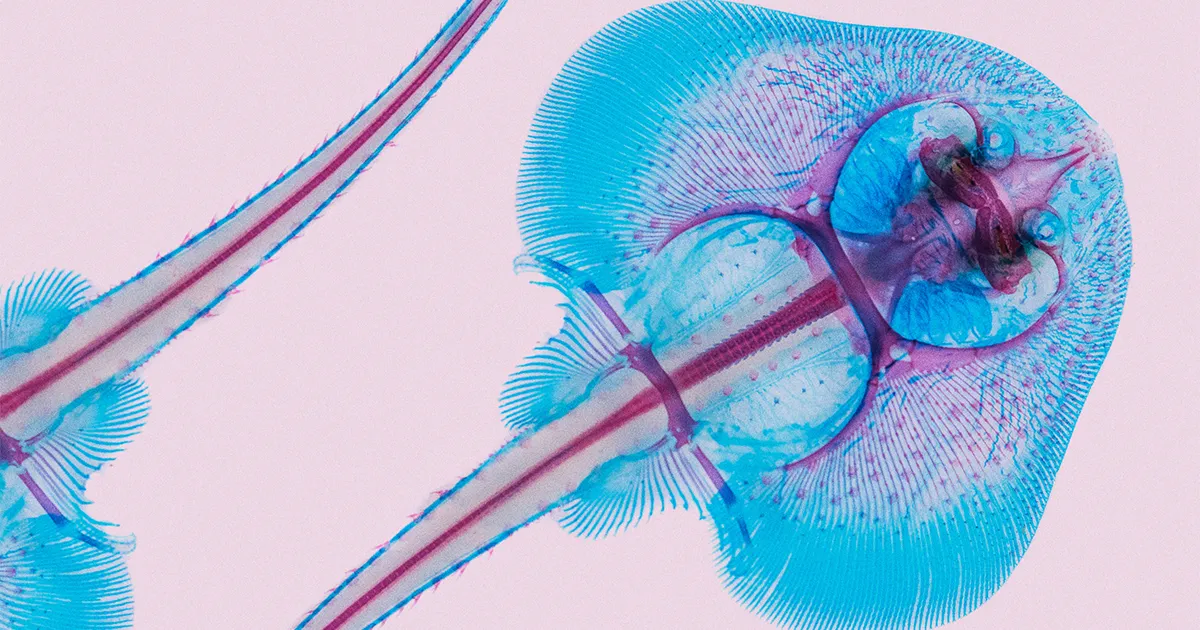
홍어라고 불리는 해양 생물은 바다 밑바닥을 훑어보며 날개 같은 가슴지느러미를 물결치며 나아가고 모래 속에 숨어 있는 작은 생물을 휘젓습니다. 그들의 특이한 납작한 몸 구조는 그들을 바다에서 가장 이상한 어류과 중 하나로 만들고 약 285억 XNUMX만 년 전에 헤엄쳤던 유선형의 상어 같은 육식 동물에서 진화했다는 것이 더 이상해 보입니다.
이제 연구자들은 홍어가 독특한 프로필을 어떻게 진화시켰는지 발견했습니다. 홍어 DNA 서열의 재배열은 게놈의 3D 구조를 변경하고 핵심 발달 유전자와 이를 지배하는 조절 서열 사이의 고대 연결을 파괴했습니다. 이러한 변화는 차례로 동물의 신체 계획을 다시 작성했습니다. 과학자들 그들의 발견을보고했다 in 자연 4월 인치
이 발견은 발달을 지시하는 유전적 메커니즘에 고정함으로써 홍어의 진화적 변형의 수수께끼를 풀었습니다. "화석 기록은 이러한 변화가 일어났다고 말하지만 실제로 어떻게 일어났습니까?" 말했다 크리스 아메미야, 새로운 연구에 참여하지 않은 머세드 캘리포니아 대학의 분자유전학자. "이것은 고전적인 evo-devo 질문입니다."
홍어의 새로운 체형의 기원을 밝히기 위해 몇 년 전 진화유전체학자는 호세 루이스 고메즈-스카메타 유전체학 연구자와 진화 발달 생물 학자로 구성된 다양한 국제 팀을 구성했습니다. 첫 번째 단계는 홍어의 게놈을 배열하고 조립하는 것이고 홍어와 상어 같은 연골 어류의 게놈을 편집하는 것은 엄청나게 어렵기 때문에 부분적으로 팀이 필요했습니다.
"인간 게놈보다 더 큰 경우가 많기 때문에 조합하기가 정말 어렵습니다."라고 말했습니다. 멜라니 드비아스-티보, 작업에 참여하지 않은 프랑스 몽펠리에 대학의 진화 발달 유전학자.
작업을 위해 팀은 작은 스케이트(류코라자 에리나세아), 북미 대서양 연안을 따라 쉽게 채집됩니다. 또한 실험실에서 사육할 수 있어 프로젝트의 일환으로 동물에 대한 발달 및 기능 실험을 실행할 수 있습니다.
작은 홍어의 게놈을 다른 척추동물의 게놈과 비교함으로써 연구자들은 홍어 게놈이 일반적으로 서열 수준에서 척추동물 조상의 게놈과 매우 유사하게 남아 있음을 확인했습니다. 그러나 게놈의 3D 구조에 영향을 미쳤을 몇 가지 주목할 만한 재배열이 있었습니다. 개인의 DNA에서 이러한 재배열은 유전자 조절을 방해하여 질병을 유발할 수 있습니다. 이 발견으로 연구원들은 홍어의 재배열이 신체 계획에 대한 원래의 유전적 지침을 유사하게 방해했을 수 있는지 궁금해했습니다.
경계 허물기
염색체의 DNA 서열을 보면 그 안에 있는 유전자는 유전자의 활동을 조절하는 짧은 "인핸서(enhancer)" 서열에서 놀라울 정도로 멀리 떨어져 있는 것처럼 보일 수 있습니다. 하지만 실제로는 세포핵의 DNA가 감겨 있고, 접히고, 다시 고리 모양으로 돌아가기 때문에 서로 멀리 떨어져 있지 않은 경우가 많습니다.
척추 동물에서 기능적으로 관련된 유전자 세트와 그 인핸서는 물리적으로 위상 결합 도메인(TAD)이라는 단위로 XNUMX차원으로 함께 그룹화됩니다. 경계 영역은 인핸서가 동일한 TAD의 유전자에만 작용하도록 합니다.
개요
그러나 팀이 홍어의 DNA에서 본 것과 같은 주요 게놈 재배열이 발생하면 경계가 사라지고 염색체에서 유전자의 상대적 위치가 바뀔 수 있습니다. 그 결과 "일부 인핸서는 잘못된 유전자에 지침을 제공할 수 있다"고 설명했다. 다리오 루피아네즈, 베를린 Max Delbrück Center의 진화 생물학자이자 연구의 수석 저자 중 한 명.
홍어 게놈의 3D 구조 변화가 상어 같은 조상으로부터 물려받은 고대 유전자 블록을 파괴하여 유전자의 기능에 영향을 미쳤을 가능성이 있어 보였습니다. "우리는 작은 홍어의 일부 게놈 재배열이 실제로 이러한 블록을 깨뜨리는지 여부를 확인하려고 했습니다."라고 말했습니다. 페르디난드 말레타즈, 유니버시티 칼리지 런던(University College London)의 유전체학자이자 이 연구의 공동 제XNUMX저자.
연구원들은 다른 척추동물에는 없는 작은 홍어의 게놈 재배열을 확인했습니다. 그런 다음 그들은 게놈 서열을 기반으로 TAD의 무결성에 가장 영향을 미칠 것으로 보이는 변화로 초점을 좁혔습니다.
그 노력으로 그들은 평면 세포 극성(PCP) 경로라고 하는 발달 시스템을 조절하는 TAD의 경계를 제거할 것이라고 예측한 재배열로 이끌었습니다. 그들은 다음을 예상하지 못했습니다. PCP 경로의 알려진 기능에 대해 즉시 지느러미 발달을 조절할 것이라고 제안한 것은 없습니다. 대부분 배아에서 세포의 모양과 방향을 설정합니다.
새로운 유전적 이웃
핀 개발에 대한 TAD 변경의 잠재적 영향을 테스트하기 위해, 나카무라 테츠야Rutgers University의 진화 발달 생물학자인 Rutgers는 작은 홍어 배아를 PCP 경로의 억제제에 노출시켰습니다. 지느러미의 앞쪽(전방) 가장자리는 크게 변형되어 정상적으로 자라는 것처럼 머리와 연결되지 않았습니다. 그것은 조상 TAD의 붕괴가 신체의 새로운 부분에서 PCP 유전자를 활성화함으로써 홍어의 독특한 지느러미를 만들어냈다고 제안했습니다.
Lupiáñez는 “TAD의 이러한 재배열은 기본적으로 유전자의 전체 환경을 변화시키고 새로운 인핸서를 유전자 주변으로 가져옵니다.
개요
그러나 그것이 연구원들이 발견한 유일한 관련 게놈 변화는 아니었습니다. 그들은 또한 발달적으로 중요한 일부 유전자의 발현을 조절하는 인핸서의 돌연변이를 확인했습니다. 혹스 그룹입니다. 혹스 유전자는 모든 좌우 대칭 동물의 일반적인 신체 계획을 지정합니다. 그 중 한 부분집합인 호사 유전자 클러스터는 일반적으로 발달 중인 지느러미의 뒤쪽(뒤쪽) 가장자리와 손가락의 형성을 지정하는 사지에서만 표현됩니다.
작은 스케이트에는 호사 유전자는 지느러미의 앞부분과 뒷부분 모두에서 활성화되었습니다. 마치 지느러미 뒤쪽의 성장 영역이 앞쪽을 따라 복제되어 동물이 지느러미 앞쪽에 뒤쪽 구조와 대칭인 새로운 구조 세트를 만들었다고 Debiais-Tibaud는 말했습니다.
Nakamura는 스케이트의 돌연변이된 인핸서가 호사 표현 패턴. 그는 홍어의 인핸서를 형광 단백질 유전자와 결합한 다음 그 유전자 조합을 제브라피쉬 배아에 삽입했습니다. 물고기의 가슴지느러미가 비정상적으로 자라났고 앞쪽 가장자리와 뒤쪽 가장자리를 따라 형광이 나타나 홍어의 인핸서가 추진하고 있음을 보여주었다. 호사 지느러미의 양쪽 부분에서 표현. Nakamura가 상어의 인핸서로 실험을 반복했을 때 지느러미 성장은 영향을 받지 않았고 형광은 후방으로 제한되었습니다.
“그래서 이제 우리는 유전적 돌연변이가 특히 홍어 인핸서에서 발생했다고 생각하고 있습니다. 혹스 스케이트 지느러미의 유전자 발현”이라고 Nakamura는 말했습니다.
새로운 삶의 방식을 위한 형태
연구자들이 재구성한 홍어 진화 그림에서, 홍어 혈통이 상어에서 갈라진 후 어느 시점에서 그들은 인핸서에서 돌연변이를 획득하여 호사 가슴지느러미의 앞과 뒤 모두에서 활동하는 유전자. 그리고 지느러미의 앞쪽을 따라 자라는 새로운 조직 내에서 게놈 재배열로 인해 PCP 경로가 다른 TAD의 인핸서에 의해 활성화되어 지느러미가 앞으로 확장되어 동물의 머리와 융합되는 추가 효과가 있었습니다.
"날개 같은 구조를 형성함으로써 [홍어는] 이제 완전히 다른 생태학적 틈새인 바다 밑바닥에 서식할 수 있습니다."라고 Amemiya는 설명했습니다.
가오리, 쥐가오리 및 기타 가오리는 홍어와 밀접한 관련이 있으며(모두 "바토이드" 물고기로 분류됨) 유사한 팬케익 모양은 아마도 동일한 게놈 재배열 때문일 것입니다. 그러나 가오리는 기본적으로 물 속을 날아갈 수 있도록 날개 모양의 지느러미도 수정했습니다. "홍어는 지느러미의 굴곡이 있고 바닥에 머물러 있지만 만타 가오리는 표면으로 올라와 완전히 다른 이동 방식을 가질 수 있습니다."라고 Amemiya는 말했습니다.
진화 발달 생물학자들은 이전에 게놈의 3D 구조에서 이러한 변화가 가능할 수 있다고 추측했지만, 이것은 아마도 신체 형태의 상당히 큰 변화와 명확하게 연결하는 첫 번째 논문 중 하나일 것이라고 Marletaz는 말했습니다.
Lupiáñez는 또한 이번 발견이 스케이트에 대한 이해를 훨씬 넘어서는 의미가 있다고 믿습니다. "이것은 진화에 대해 생각하는 완전히 새로운 방식입니다."라고 그는 말했습니다. 구조적 재배열은 "유전자가 있어서는 안 되는 곳에서 활성화되도록 할 수 있습니다." 그는 "이것은 질병의 메커니즘일 수 있지만 진화의 원동력이 될 수도 있다"고 덧붙였다.
- SEO 기반 콘텐츠 및 PR 배포. 오늘 증폭하십시오.
- PlatoAiStream. Web3 데이터 인텔리전스. 지식 증폭. 여기에서 액세스하십시오.
- 미래 만들기 w Adryenn Ashley. 여기에서 액세스하십시오.
- PREIPO®로 PRE-IPO 회사의 주식을 사고 팔 수 있습니다. 여기에서 액세스하십시오.
- 출처: https://www.quantamagazine.org/how-3d-changes-in-the-genome-turned-sharks-into-skates-20230530/



