L'IA dans la découverte de médicaments en un coup d'œil
L'essor continu de l'intelligence artificielle (IA) a un impact significatif sur diverses industries, les secteurs pharmaceutique et biotechnologique ne faisant pas exception. Il n'est pas surprenant que les grandes et les petites organisations pharmaceutiques adoptent de plus en plus des plateformes de découverte de médicaments par IA pour rationaliser les processus de recherche et de développement, réduire les délais et les coûts de découverte et améliorer l'efficacité globale.
Des sociétés pharmaceutiques de premier plan telles que J&J, GSK, AstraZeneca, Novartis, Pfizer, Sanofi et Eli Lilly, entre autres, ont réalisé des investissements substantiels dans l'IA pour la découverte de médicaments. Ces investissements comprennent des prises de participation, des acquisitions ou des partenariats avec des entreprises axées sur l'IA, le développement de capacités internes ou une combinaison de ces stratégies.
Parallèlement, il y a une vague de nouvelles sociétés de découverte de médicaments et de biotechnologie qui se sont établies en tant qu'organisations centrées sur l'IA, souvent dès leur création. Fondées principalement au cours de la dernière décennie, ces sociétés ont déjà construit et testé des plateformes spécialisées de découverte de médicaments axées sur l'IA. Ces plates-formes intègrent souvent de nombreux modèles d'apprentissage automatique et commencent maintenant à offrir des avantages significatifs en termes de capacités de découverte de cibles et de conception de médicaments rapides et rentables. En conséquence, ils produisent des candidats-médicaments précliniques et cliniques à un rythme accéléré. Dans les sections suivantes, nous explorerons une sélection de candidats-médicaments développés par l'IA, y compris de petites molécules, des produits biologiques et d'autres modalités, qui ont déjà entamé des essais cliniques ou sont sur le point de le faire.
De plus, certaines sociétés d'IA ont fait des progrès dans la modélisation de la biologie en utilisant des données multimodales complexes à des échelles inimaginables il y a à peine deux décennies. Un autre groupe d'entreprises a développé des plateformes basées sur l'IA pour améliorer l'efficacité opérationnelle et la conception d'expériences dans les essais cliniques ou l'analyse de données réelles, comme la pharmacovigilance.
De grandes entreprises technologiques, comme Alphabet, Microsoft, Amazon, IBM et Tencent, possèdent une expertise dans les technologies de l'IA et du Big Data, et s'aventurent également dans le domaine de la découverte de médicaments. Leur implication comprend l'investissement, la création de startups, le partenariat avec des entreprises des sciences de la vie, l'expérimentation et l'innovation.
Enfin, des progrès significatifs ont été réalisés dans d'autres technologies de pointe, telles que l'informatique quantique, Cryo-EM et les bibliothèques codées par ADN. Ces technologies convergent avec la tendance de l'IA, ce qui entraîne non seulement de nouveaux types d'outils, de produits et de services, mais également une vague de startups innovantes et même de nouveaux modèles commerciaux.
Qu'est-ce que l'IA et comment est-elle appliquée à la découverte de médicaments ?
L'intelligence artificielle est un concept relativement ancien, formalisé lors d'une célèbre conférence du Dartmouth College en 1956. Les technologies d'IA dans la découverte de médicaments ont évolué à partir des concepts et approches antérieurs d'apprentissage automatique (ML), de chimie informatique et de bioinformatique. Par exemple, l'application de l'apprentissage automatique au développement de modèles de relation quantitative structure-activité (QSAR) et de systèmes experts pour la prédiction de la toxicité a une longue histoire.
Cependant, l'avènement rapide (dans certains cas - "exponentiel") des mégadonnées, de l'analyse avancée, de la minimisation des coûts de calcul, de l'accélération GPU, de l'informatique en nuage, du développement d'algorithmes (par exemple, des réseaux de neurones profonds et de grands modèles de langage) et la "démocratisation" de la technologie de l'IA — tous ont conduit à un « boom » synergique dans la commercialisation et l'industrialisation de l'intelligence artificielle, en particulier dans les industries pharmaceutiques et biotechnologiques.
Dans ce livre blanc, nous utilisons le terme collectif « intelligence artificielle » pour désigner tout système de calcul et de modélisation sophistiqué qui peut automatiquement apprendre des informations et tirer des suggestions pratiques à partir de « mégadonnées », de données structurées et non structurées, ainsi que de données multimodales.
Bien qu'il n'y ait pas de limite à une famille particulière d'algorithmes que nous appelons "l'intelligence artificielle", nous impliquons, dans la plupart des cas, diverses saveurs de systèmes basés sur l'apprentissage automatique (principalement des réseaux de neurones profonds) et un grand traitement du langage naturel (NLP) des modèles. Les systèmes d'IA modernes peuvent apprendre sans recevoir d'instructions explicites (contrairement aux logiciels de chimie informatique traditionnels dans la logique "si-alors"), ils peuvent améliorer la précision après de nouveaux cycles d'apprentissage et lorsque davantage de données sont transmises au système, et - plus particulièrement - ils peuvent traiter des données multimodales de haute dimensionnalité de taille énorme. Tous ces attributs sont ce qui différencie considérablement les systèmes d'intelligence artificielle modernes des anciens progiciels de chimie informatique et de bioinformatique. De telles capacités sont au centre de ce qui motive l'engouement continu pour l'IA (et le battage médiatique).
Alors que certains composants de ce que nous appelons "l'intelligence artificielle" - par exemple, les outils d'apprentissage automatique et les modèles de langage - sont utilisés par à peu près toutes les organisations pharmaceutiques et laboratoires universitaires, certaines entreprises ont réussi à construire des pipelines de calcul et de modélisation sophistiqués, des "plates-formes d'IA" de recherche. qui incluent des flux de travail automatisés sur des dizaines, voire des centaines de modèles et systèmes variés (apprentissage en profondeur, modèles de langage) et des centaines de sources de données publiques et propriétaires diverses.
La haute sophistication et l'automatisation de certaines plates-formes d'IA ont conduit à leur « banalisation » au point qu'elles ont déposé des noms commerciaux. Dans le même temps, certains d'entre eux sont proposés en tant que logiciel en tant que service à d'autres sociétés. Les exemples incluent mRNA DESIGN STUDIO™ de Moderna, Centaur Chemist® d'Exscientia, Guardian Angel™ d'AI Therapeutics, ConVERGE™ de Verge Genomics, Taxonomy3® de C4X Discovery et bien d'autres.
Vous trouverez ci-dessous un exemple de Pharma.AI d'Insilico Medicine, un système modulaire pour la découverte de médicaments de bout en bout qui comprend des centaines de sous-systèmes différents et de modèles d'apprentissage automatique - entièrement contrôlés par d'autres algorithmes d'abstraction de modélisation supérieure (via un principe de « l'apprentissage d'ensemble »).
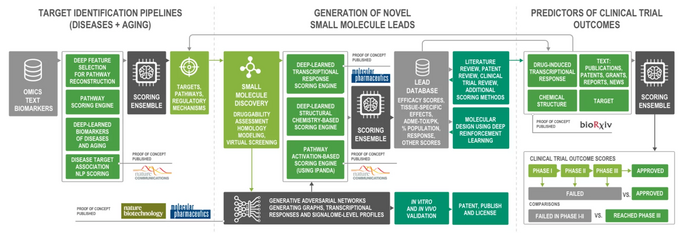
Un schéma de plate-forme de bout en bout Pharma.AI. Crédit image : https://insilico.com
L'intelligence artificielle est largement utilisée dans presque tous les aspects de la recherche pharmaceutique, de l'exploration de données, de la modélisation biologique et de la découverte de cibles à l'identification des pistes et à la recherche préclinique et clinique. Il est également utilisé pour la planification de la synthèse, la recherche intelligente de réactifs et de consommables de recherche, et les tâches auxiliaires telles que les cahiers de laboratoire intelligents et les assistants virtuels.

La source: https://www.biopharmatrend.com/m/companies/ai/
L'écosystème des adopteurs d'IA des sciences de la vie comprend les principales catégories d'acteurs suivantes :
|
Plus de 400 entreprises axées sur l'IA (startups/scaleups), offrant un large éventail de plates-formes et de services basés sur l'IA - du modèle classique de logiciel en tant que service aux services personnalisés de science des données, à la découverte de médicaments ("Candidat médicamenteux en tant que service") et au support/gestion des essais cliniques ressources. |
|
Les fournisseurs de logiciels spécifiques à un domaine (par exemple, KNIME, ChemAxon, Dotmatics, MolSoft et autres) se concentrent principalement sur les logiciels de chimie informatique/bioinformatique, mais fournissent également des outils d'apprentissage automatique. |
|
Des entreprises pharmaceutiques et biotechnologiques de premier plan développant une expertise interne en IA dans le cadre de leur stratégie de R&D. Ces acteurs collaborent souvent avec des fournisseurs d'IA externes et des startups biotechnologiques axées sur l'IA pour explorer des programmes pilotes dans la découverte de médicaments/la biologie fondamentale/l'analyse des essais cliniques. |
|
Des entreprises technologiques de premier plan comme Google, Amazon et Tencent entrent dans l'espace pharmaceutique, en tirant parti des technologies d'IA de pointe et des infrastructures de mégadonnées. |
|
Organisations de recherche sous contrat (CRO) développant une expertise en IA pour augmenter leur offre de valeur aux clients pharmaceutiques/biotechnologiques |
|
Laboratoires universitaires dans l'espace pharmaceutique / biotechnologique, menant des recherches sur l'IA et développant des cadres et des outils spécialisés pertinents pour l'industrie (généralement un berceau pour les futures startups / spin-outs de l'IA) |
|
Fournisseurs de logiciels non spécifiques à un domaine développant des packages et des modèles d'IA en tant que service adaptés à une application dans la recherche pharmaceutique (par exemple, "IA prête à l'emploi") |
|
Outils et cadres d'apprentissage automatique open source, largement exploités par les professionnels des sciences de la vie dans leurs projets de recherche |
Paysage d'investissement dans la découverte de médicaments par IA
Après 2021, l'année anormalement réussie pour l'industrie de la biotechnologie en termes de montant des transactions de capital-risque, du nombre record d'introductions en bourse, d'une abondance de sorties réussies et d'un climat généralement très positif sur le marché boursier, l'année 2022 a démontré ralentissement important de l'activité financière et carrément mauvaise performance du marché boursier.
Cependant, l'intelligence artificielle dans le secteur de la découverte de médicaments a fait preuve d'une certaine résilience, du moins dans le paysage des transactions de capital-investissement, plusieurs entreprises ayant levé des centaines de millions de capital-risque. Quelques exemples incluent MegaRobo Technologies, basée à Pékin (300 millions de dollars de série C), ConcertAI basée au Massachusetts (150 millions de dollars de série C) et Celsius Therapeutics (83 millions de dollars de série A), Insilico Medicine basée à Hong Kong (95 millions de dollars de série D), Californie- basée sur BigHat Biosciences (75 millions de dollars de série B) et DeepCell (73 millions de dollars de série B), et plusieurs autres – lisez «Principales rondes de capital-risque pour les entreprises d'IA dans la découverte de médicaments et la biotechnologie en 2022 ».
Le paysage des fusions et acquisitions (M&A) a été marqué par un récent accord notable impliquant un géant de la biotechnologie Ginkgo Bioworks acquiert Zymergen dans une transaction valorisant Zymergen à 300 millions de dollars. L'acquisition associe les capacités d'apprentissage automatique et de science des données de Zymergen à la plateforme de biologie synthétique de Ginkgo.
Principales observations et tendances de l'industrie
L'avènement de l'IA et des technologies de données, ainsi que de nouveaux outils informatiques et solutions d'infrastructure (bases de données, services cloud, etc.), redéfinissent tous le mode de fonctionnement de l'industrie pharmaceutique - au niveau de la recherche, clinique et commercial. Ci-dessous, passons en revue certaines des tendances et observations de l'IA pour l'espace de découverte de médicaments et les développements illustratifs de l'industrie en 2022.
Modélisation biologique et découverte de cibles basées sur l'IA
Dans la recherche sur la découverte de médicaments, l'identification de nouvelles cibles médicamenteuses est essentielle pour développer de nouveaux médicaments thérapeutiques de première classe - des « blockbusters » potentiels. Les efforts de découverte de médicaments au cours des dernières décennies se sont concentrés, traditionnellement, sur le ciblage de protéines spécifiques avec des « poches » appropriées pour être influencées par une molécule de ligand (souvent, une petite molécule). Mais sur l'ensemble de toutes les protéines humaines (alias « protéome »), un petit nombre de protéines ont été explorées comme cibles. Il y a actuellement 20,360 XNUMX protéines humaines dans Swiss-Prot, dont environ 4,600 22 sont connues pour être impliquées dans les mécanismes de la maladie selon la base de données OMIM, représentant environ XNUMX % des protéines humaines ayant un rôle dans la maladie. Ces protéines sont la région évidente du protéome humain susceptible de contenir des cibles médicamenteuses viables. Cependant, à partir de 2017, seules environ 890 biomolécules humaines et dérivées d'agents pathogènes (principalement des protéines) étaient réellement utilisées par les médicaments approuvés par la FDA. Ces biomolécules comprenaient 667 protéines dérivées du génome humain ciblées par des médicaments pour les maladies humaines. Les choses ne sont pas très différentes aujourd'hui, il y a donc encore beaucoup de place pour identifier de nouvelles cibles dans ce pool. De nouvelles approches informatiques basées sur des technologies d'intelligence artificielle permettent d'identifier de nouvelles poches de protéines médicamenteuses à grande échelle, permettant parfois des écrans virtuels à l'échelle du protéome.
Mais ce qui est encore plus excitant, les outils de modélisation avancés aident à identifier et à moduler de nouveaux types de cibles, telles que les interactions protéine-protéine, les cibles avec de grandes zones de contact, les interactions protéine-acide nucléique et les cibles de nouvelle génération, telles que l'exploitation de la protéine cellulaire. machinerie de dégradation.
De nombreuses entreprises axées sur l'IA se concentrent sur la modélisation de la biologie, la découverte et la validation de nouvelles cibles et offrent un "modèle de maladie en tant que service" ou une "découverte de cible en tant que service" à d'autres organisations. La demande pour ce type de services de recherche sous contrat augmente, ce qui se reflète dans le nombre croissant de partenariats de découverte de cibles.
Par exemple, en septembre 2022, une société de modélisation biologique basée en Israël, CytoReason, a annoncé une collaboration élargie de 110 millions de dollars avec Pfizer. Les deux sociétés ont commencé à travailler ensemble en 2019 lorsque Pfizer a commencé à utiliser les modèles biologiques de CytoReason dans la recherche visant à développer de nouveaux médicaments pour les maladies à médiation immunitaire et les immunothérapies contre le cancer.
En mai 2022, AstraZeneca a annoncé avoir collecté une deuxième cible de fibrose pulmonaire grâce à sa collaboration avec BenevolentAI, un leader basé au Royaume-Uni dans la découverte de médicaments basés sur l'IA. Cette étape a marqué une troisième nouvelle cible découverte par BenevolentAI pour AstraZeneca depuis le début de la collaboration en 2019. Quelques mois plus tard, en octobre 2022, BenevolentAI a réussi à fournir deux cibles supplémentaires générées par l'IA pour le portefeuille de R&D d'AstraZeneca, visant les maladies rénales chroniques et idiopathiques. fibrose pulmonaire.
En novembre 2022, Insilico Medicine, basée à Hong Kong, a signé un accord d'une valeur potentielle de 1.2 milliard de dollars avec Sanofi pour découvrir jusqu'à six nouvelles cibles en exploitant la plateforme "Pharma.AI" d'Insilico Medicine.
Alors que des algorithmes de pointe tels que les réseaux de neurones profonds nécessitent de gros volumes de données pour modéliser correctement la biologie, il existe des cibles avec une petite quantité de données disponibles. Cyclica, une société basée au Canada, a développé une plateforme basée sur l'IA pour la polypharmacologie et le dépistage à l'échelle du protéome, capable de travailler avec des cibles à « faible niveau de données ». En novembre 2022, Cyclica a reçu une subvention de 1.8 million de dollars de la Fondation Bill & Melinda Gates pour appliquer sa plateforme de découverte de médicaments basée sur l'IA afin de découvrir de nouveaux contrats non hormonaux, en exploitant plusieurs cibles biologiques à faible niveau de données.
Selon le Rapport BiopharmaTrend, il existe au moins 182 autres sociétés d'IA dans l'espace de découverte cible, y compris des sociétés de premier plan bien financées dotées de plateformes de R&D de pointe, telles qu'Insitro, Relay Therapeutics, Valo Health et d'autres.
De nouvelles startups « natives de l'IA » émergent constamment dans le domaine de la modélisation biologique. Par exemple, CardiaTec Biosciences, WhiteLab Genomics, Degron Therapeutics pour n'en nommer que quelques-uns.
EN RELATION: 11 startups de découverte de médicaments alimentées par l'IA fondées en 2021
Dans l'ensemble, les méthodes de modélisation avancées basées sur l'intelligence artificielle aident à redéfinir la définition même des cibles biologiques, car nous essayons de lier la réponse aux médicaments à la variation génétique, de comprendre l'efficacité et la sécurité cliniques stratifiées, de rationaliser les différences entre les médicaments d'une même classe thérapeutique et de prédire utilité du médicament dans des sous-groupes de patients.
Craquer la biologie structurale avec l'IA
L'un des sujets liés à l'IA les plus discutés dans la communauté des sciences de la vie cette année a été le récent succès de la filiale britannique d'Alphabet DeepMind, qui a reçu une large couverture pour son succès dans la résolution du problème de repliement des protéines, un problème biologique vieux d'un demi-siècle.
En juillet 2022, le logiciel d'apprentissage en profondeur AlphaFold de DeepMind prévu et partagé publiquement structures protéiques de plus de 200 millions de protéines, ayant démontré la capacité étonnante de son système d'IA à prédire avec précision les structures 3D uniquement à partir de sa séquence d'acides aminés 1D. Alors que certains soutiennent que cette découverte n'a peut-être pas (pour l'instant) un rôle aussi transformateur dans la découverte de médicaments qu'on pourrait le supposer, et qu'AlphaFold n'a pas beaucoup mieux fonctionné que le hasard pour prédire les interactions entre les protéines bactériennes et les composés antibactériens, la découverte change certainement de paradigme pour la biologie structurale et illustre le potentiel de l'IA dans la recherche fondamentale en biologie.
En novembre 2022, le succès révolutionnaire de DeepMind dans la modélisation du protéome a été concurrencé par les chercheurs de Meta (anciennement Facebook, dont le siège est à Menlo Park, en Californie). Il a utilisé l'IA pour prédire les structures de quelque 600 millions de protéines de bactéries, de virus et d'autres micro-organismes qui n'ont pas été caractérisés.
Les scientifiques de Meta ont utilisé une méthode entièrement approche différente de l'IA — en utilisant un "grand modèle de langage", un type d'IA capable de prédire le texte à partir de quelques lettres ou mots seulement. Les modèles de langage naturel (NLP) sont généralement formés sur de gros volumes de texte. Cependant, les séquences de protéines 1D sont essentiellement des chaînes de lettres, de sorte que les NLP peuvent être appliqués à de tels problèmes de la même manière que pour travailler avec des langues humaines.
Fait intéressant, de tels sauts technologiques majeurs dans le repliement des protéines pourraient s'avérer plus utiles pour conception de protéines de novo, que de simplement modéliser les structures de protéines existantes pour la découverte de médicaments. Le temps nous dira où l'impact sera le plus important, mais les succès ci-dessus de DeepMind et Meta ne sont pas le seul développement passionnant pour les biologistes structurels en 2022.
Récemment, les progrès rapides de la cryo-EM, associés aux technologies d'IA, ont donné naissance à un nouvelle vague de startups biotechnologiques tels que Gandeeva Therapeutics, Septerna et MOMA Therapeutics. Le domaine de la cryo-EM se réchauffe avec des start-ups biotechnologiques attirant l'attention d'un large éventail d'investisseurs, des petites entreprises de capital-risque au propriétaire de TikTok et au géant de la technologie Internet ByteDance, investissant dans Shuimu BioSciences. L'intérêt est motivé non seulement par la technologie révolutionnaire primée par le prix Nobel, mais aussi par le recrutement actif de l'IA dans le processus. La publication récente "Un pipeline cryo-EM assisté par l'IA pour les études structurelles d'extraits cellulaires" a mis en évidence le rôle non remplaçable de l'IA dans les pipelines cryo-EM complexes, y compris la prédiction de modèles atomiques basée sur l'IA pour étudier rapidement et simultanément la structure de plusieurs membres de la communauté protéique de novo. L'apprentissage automatique permet non seulement d'accélérer et d'optimiser le pipeline cryo-EM, mais également d'éviter les pièges de biais de l'utilisateur.
Gandeeva Therapeutics, fondée en 2021, a levé 40 millions de dollars au début de cette année pour développer de nouvelles thérapies basées sur l'imagerie de précision des interactions protéines-médicaments. Leur moteur de sélection de cible, associé au moteur Cryo-EM, peut aider à "éviter les impasses de découverte", comme l'a déclaré la société. Dans le même temps, lancée en 2020, la biotech cryo-EM MOMA Therapeutics a levé la somme colossale de 236 millions de dollars en seulement deux ans, avec pour objectif ambitieux de mettre à la disposition des cliniques de nouveaux médicaments de précision contre le cancer. Le MOMA se concentre sur une classe unique de cibles biologiques - les «machines moléculaires».
Développer de petites molécules grâce à l'IA
Après la modélisation de maladies et la découverte de cibles, la conception de molécules chimiques ou biologiques est le deuxième cas d'utilisation le plus abondant pour appliquer l'intelligence artificielle à la découverte de médicaments. Plus de 130 entreprises axées sur l'intelligence artificielle sur les 384 entreprises du rapport BiopharmaTrend AI appliquent l'intelligence artificielle pour concevoir des candidats-médicaments, entre autres cas d'utilisation.
La conception de médicaments basée sur l'IA se divise principalement en trois grandes catégories : la conception de médicaments de novo (par exemple, générative), le criblage virtuel des bases de données existantes et la réorientation des médicaments.
La conception de médicaments de novo est principalement rendue possible par des modèles d'apprentissage en profondeur, tels que les réseaux neuronaux antagonistes génératifs (GAN). Parmi les exemples de plates-formes d'IA génératives, citons le logiciel Chemistry42 d'Insilico Medicine, Makya d'Iktos et De Novo Platform de Ro5. Les autres acteurs de cette catégorie incluent Recursion Pharmaceuticals, Deep Cure, Standigm et autres.
L'application du criblage virtuel à très grande échelle activé par l'intelligence artificielle, passant au crible des milliards de molécules pour trouver des succès. En août 2022, Sanofi s'est associé à Atomwise dans le cadre d'un accord de conception de médicaments d'une valeur potentielle pouvant atteindre 1.2 milliard de dollars. L'accord, qui verra Sanofi payer 20 millions de dollars d'avance, se concentre sur l'exploitation de la plateforme AtomNet de la société américaine pour rechercher de petites molécules pour jusqu'à cinq cibles médicamenteuses sélectionnées par Sanofi. Un AtomNet basé sur un réseau de neurones convolutifs excelle dans la conception de médicaments basés sur la structure, permettant "la recherche rapide, alimentée par l'IA, de la bibliothèque propriétaire d'Atomwise de plus de 3 billions de composés synthétisables", selon le annonce.
Plus tôt en 2019, Atomwise a collaboré avec le leader chimique ukrainien Enamine pour mener « le premier et le plus grand criblage virtuel de 10 milliards de composés au monde », visant à identifier les succès pour l'oncologie pédiatrique.
Enfin, un certain nombre d'entreprises utilisent des stratégies de réorientation pour la découverte de médicaments basés sur l'IA. Les entreprises de cette catégorie, notamment Healx, BenevolentAI, BioXcel Therapeutics, utilisent largement des modèles de traitement du langage naturel (PNL) et l'apprentissage automatique et fonctionnent en analysant d'énormes quantités de données textuelles non structurées - articles de recherche et brevets, dossiers de santé électroniques (DSE), comme ainsi que d'autres types de données - pour créer et rechercher des « graphiques de connaissances ». Ces ontologies interrogeables activées par l'IA permettent de sélectionner de nouvelles indications ou populations de patients pour des candidats-médicaments déjà connus ou même des médicaments approuvés.
Par exemple, Lantern Pharma, une société de biotechnologie au stade clinique basée aux États-Unis, s'est concentrée sur l'innovation du processus de développement de médicaments anticancéreux en utilisant la génomique avancée, l'apprentissage automatique et l'intelligence artificielle.
La plate-forme d'intelligence artificielle de la société, RADR®️, comprend actuellement plus de 25 milliards de points de données et utilise l'analyse de mégadonnées et l'apprentissage automatique pour découvrir rapidement des signatures génomiques biologiquement pertinentes corrélées à la réponse aux médicaments, puis pour identifier les sous-groupes de patients atteints de cancer pertinents pour bénéficier des candidats-médicaments de Lantern. . RADR ®️ est également utilisé par Lantern et ses collaborateurs pour développer et positionner de nouveaux médicaments ainsi que pour le repurposing de médicaments.
EN RELATION: Dévoilement de la réussite de Lantern Pharma dans le domaine de l'oncologie de précision alimentée par l'IA
L'IA rencontre les bibliothèques codées par l'ADN
Une approche quelque peu unique de la conception de médicaments consiste à utiliser des bibliothèques codées par ADN (DEL) comme source de nouvelles molécules à rechercher. Étant donné que la technologie DEL offre un accès essentiellement au plus grand espace chimique disponible sur le marché, cette technologie de mégadonnées est un complément naturel pour les outils basés sur l'IA.
Un notable affaire a eu lieu en 2020, lorsque Insitro, l'un des acteurs notables de l'application de l'apprentissage automatique pour la découverte de médicaments, fondé par Daphne Koller, a acquis Haystack Sciences. La plate-forme basée sur l'apprentissage automatique de Haystack combinait plusieurs éléments de sa technologie DEL, y compris la capacité de synthétiser des collections larges et diverses de petites molécules, la capacité d'exécuter un suivi itératif et une technologie de criblage semi-quantitative exclusive appelée nDexer™, qui génère ensembles de données à plus haute résolution.
À son tour, ZebiAI a été acquis en 2021 par un autre développeur notable d'une plateforme de découverte de médicaments basée sur l'intelligence artificielle, une biotechnologie au stade clinique Relay Therapeutics, où Relay a payé 85 millions de dollars à l'avance. Cette acquisition a permis à Relay d'intégrer la technologie DEL basée sur l'apprentissage automatique de ZebiAI dans sa plateforme de ciblage des protéines Dynamo.
EN RELATION: Un examen du marché de la technologie des bibliothèques codées par ADN dans la découverte de médicaments
En octobre 2021, X-Chem a acquis Glamorous AI, un développeur d'une solution d'intelligence artificielle modulaire à multiples facettes pour la découverte de médicaments RosalindAI, comprenant des capacités d'ingénierie et de caractérisation des données, d'analyse prédictive, de calcul haute performance et de conception de médicaments de novo.
Conception de médicaments basée sur l'IA au-delà des petites molécules
Considérant que les outils d'intelligence artificielle modernes appliqués à la découverte de médicaments ont de profondes racines historiques dans la chimioinformatique et les premiers modèles QSAR basés sur l'apprentissage automatique du siècle dernier, il n'est pas surprenant que l'écrasante majorité des startups d'IA dans la découverte de médicaments se concentrent sur les petites molécules. .
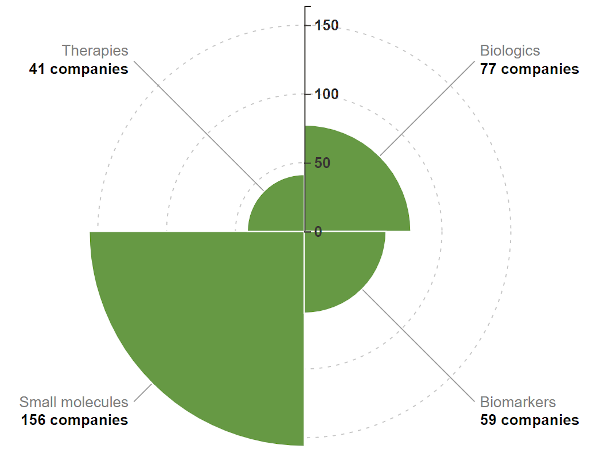
Répartition des entreprises de découverte de médicaments IA par catégorie de produits. Source: Rapport sur l'IA BiopharmaTrend.
Cependant, les médicaments biomoléculaires (alias « produits biologiques ») et les nouvelles modalités chimiques sont de plus en plus abondants dans l'espace pharmaceutique, tout comme les nouvelles sociétés de biotechnologie qui appliquent des méthodes basées sur l'IA pour les découvrir. Après que les scientifiques ont craqué le génome humain en 2003, l'espace de la pharmacogabilité et de la développabilité a rapidement évolué. Au cours du siècle dernier, la règle des cinq de Lipinski (Ro5) servait de « lumière directrice » pour la conception de molécules de type médicament pour une administration orale dans l'espace cible médicamenteux « traditionnel ».
En revanche, de nouveaux types de cibles, telles que les interactions protéine-protéine, les cibles avec de grandes zones de contact, les interactions protéine-acide nucléique et les cibles de nouvelle génération, telles que l'exploitation de la machinerie de dégradation des protéines cellulaires, sont à l'origine de l'avènement d'une variété d'approches émergentes. modalités moléculaires, à savoir au-delà du Ro5 (bRo5) les petites molécules (telles que les modulateurs d'interaction protéine-protéine, les chimères ciblées par les protéines (PROTAC), les anticorps monoclonaux (mAb), les peptides et les peptidomimétiques, et les modalités à base d'acide nucléique (ARN et ADN- basé), sont devenus un élément clé dans la découverte de médicaments.
EN RELATION: L'"explosion" des modalités thérapeutiques : petites molécules, produits biologiques et tout le reste,
Par exemple, un nombre croissant d'entreprises appliquent des méthodes d'IA pour découvrir de nouveaux anticorps monoclonaux - la modalité biologique la plus réussie sur le plan commercial à ce jour. Notamment, en avril 2022, la société israélienne Biolojic Design a annoncé son tout premier anticorps conçu par ordinateur entré dans l'essai clinique. L'entreprise s'appuie sur une stratégie de conception basée sur la structure. Son modèle d'IA est formé sur des millions de paires anticorps-antigène pour identifier un anticorps matrice contre la cible d'intérêt à partir d'anticorps humains existants. Un modèle d'apprentissage automatique supplémentaire est utilisé pour prédire les mutations et guider l'optimisation du modèle pour améliorer ses propriétés.
En novembre 2022, la société canadienne AbCellera Biologics a annoncé que Regeneron avait choisi d'exercer son droit de faire avancer le premier des anticorps thérapeutiques candidats d'AbCellera ciblant un récepteur couplé aux protéines G (GPCR) non divulgué dans un développement préclinique plus poussé. Le partenariat, qui a débuté en mars 2020 et permet quatre programmes de découverte sélectionnés par Regeneron, s'appuie sur le moteur de découverte d'anticorps basé sur l'IA d'AbCellera et sur les souris VelocImmune® de Regeneron pour identifier de nouveaux anticorps thérapeutiques.
Deux douzaines d'autres sociétés de découverte d'anticorps utilisent l'IA, notamment la société américaine AbSci, BigHat Biosciences, Totient, Nabla Bio et Generate Biomedicine ; la société canadienne Deep Biologics ; NeoX basé en Chine ; Deep CDR, Natural Antibody et MabSilico basés dans l'UE, etc.
La société américaine au nom accrocheur Creyon Bio applique une approche d'ingénierie pour créer de nouveaux médicaments à base d'oligonucléotides (OBM). La société a été fondée en 2019 et a levé 40 millions de dollars de financement en mars 2022. Fondée en 2014 en tant que spin-out du Cold Spring Harbor Laboratory, Envisagenics est une société basée à New York qui se concentre sur la découverte de thérapies à base d'ARN. Selon leur mission déclarée, ils visent à réduire la complexité des données biomédicales à l'aide des technologies AI/ML. Tout récemment, en août 2022, ils ont reçu une subvention du National Cancer Institute, ce qui a entraîné un financement total de 27.1 millions de dollars.
La technologie basée sur l'IA d'Envisagenics, SpliceCore, est une plate-forme basée sur le cloud validée expérimentalement pour prédire les cibles de médicaments et les biomarqueurs grâce à la découverte d'épissage à partir de données de séquençage d'ARN. Selon l'entreprise, cela garantit une précision et une vitesse supérieures par rapport aux méthodes traditionnelles.
La stratégie d'Innophore axée sur l'IA pour concevoir de nouvelles enzymes thérapeutiques est réalisée en couplant leur technologie brevetée Catalophore™ à des approches bioinformatiques conventionnelles de pointe et à l'intelligence artificielle. Innophore peut exploiter des bases de données structurales et séquentielles à l'aide de modèles de recherche tridimensionnels (3D) appelés « catalophores » (c'est-à-dire porteurs de la fonction catalytique) définis par des nuages de points de caractéristiques physico-chimiques. Les nouvelles enzymes identifiées par cette technique ne partagent pas nécessairement une structure ou une base de séquence commune avec leurs homologues employés. Par conséquent, ils présentent potentiellement des propriétés protéiques modifiées, telles que la thermostabilité, la robustesse, le spectre du substrat, la sélectivité et la spécificité.
Outre la conception de nouvelles enzymes, la technologie d'Innophore peut potentiellement changer la donne pour les applications épidémiologiques, en protégeant les mutations potentiellement dangereuses des virus. En 2021, Innophore a lancé le projet virus.watch en coopération avec l'AWS Diagnostic Development Initiative. L'objectif de ce projet était la mise en œuvre d'un système de surveillance et d'évaluation des variantes émergentes de médicaments et de coronavirus (SARS-CoV-2). Le premier document commun, publié dans Nature en août 2022, décrit l'analyse bioinformatique des variants du SRAS-CoV-2 révélant une affinité de liaison au récepteur hACE2 plus élevée pour le pic RBD d'Omicron B.1.1.529 par rapport à une référence de type sauvage.

Le suivi de l'évolution du virus au fil du temps à l'aide de la technologie Innophore et d'AWS montre un taux élevé de mutations survenant avec la variante Omicron. Les sphères représentent les atomes alpha-C du résidu d'acide aminé correspondant. La couleur et la taille sont en corrélation avec le nombre de mutations à chaque position.
Fondée en 2008, Evaxion Biotech, basée au Danemark, est une société axée sur l'IA, qui se consacre au développement de vaccins contre le cancer et les maladies infectieuses. Ils possèdent une plateforme d'IA-Immunologie au stade clinique, combinant la technologie de l'IA avec leur expertise en ingénierie pour générer des modèles prédictifs, aidant à identifier des immunothérapies uniques pour les patients. Evaxion Biotech a attiré un total de 57 millions de dollars, entrant dans le cycle de financement par actions post-introduction en bourse en juin 2022 d'une valeur de 40 millions de dollars, dirigé par un seul investisseur Lincoln Park Capital Fund.
EN RELATION: 10 entreprises appliquant l'IA pour concevoir des produits biologiques
Certaines sociétés d'IA du «club des modalités chimiques», comme Exscientia, se lancent maintenant dans la découverte de produits biologiques. En novembre 2022, la société a annoncé que sa plateforme d'IA inclurait la conception d'anticorps humains. Exscientia met également en place un laboratoire de produits biologiques automatisé à Oxford pour générer et profiler en interne de nouveaux anticorps.
Une tendance croissante consiste à exploiter le système de dégradation des protéines des cellules humaines pour se débarrasser des protéines malignes et guérir les maladies. Une modalité ici qui gagne en popularité est la protéolyse ciblant la chimère (PROTAC) a été introduite en 2001, et elle se compose de deux ligands reliés par un lieur flexible. L'architecture chimique primaire des PROTAC modernes est la même : un ligand cible l'enzyme E3, qui est un composant qui envoie des protéines obsolètes au protéasome, et un autre ligand cible une protéine d'intérêt (POI) qui doit être dégradée. Un PROTAC lie E3 et POI, les rapprochant pour former un complexe de proximité induit. Dans certains cas, lorsque les protéines s'alignent de manière appropriée, le POI devient ubiquitiné, ce qui le marque de la dégradation par le protéasome.
Une autre approche large de la dégradation des protéines comprend les « colles moléculaires », un domaine de recherche en pleine croissance. Contrairement aux PROTAC, étant des petites molécules bifonctionnelles relativement grandes avec deux sites actifs et un lieur, les colles moléculaires sont des molécules plus petites et plus semblables à des médicaments. Ces derniers se lient à une poche protéique agrégée résultant de la proximité de deux protéines distinctes sous l'effet de la molécule de colle moléculaire.
Il existe une vague d'entreprises dans le domaine de la dégradation des protéines (et, plus largement, de la modulation), y compris Arvinas, Nurix Thérapeutique, Thérapeutique Kymera, C4 Therapeutics, Roivant Discovery, Cedilla Therapeutics et Lycia Therapeutics, pour n'en nommer que quelques-uns.
Certaines entreprises appliquent des algorithmes d'IA de pointe pour concevoir des composés induisant la proximité. Par exemple, la société autrichienne et américaine Celeris Therapeutics a construit la plate-forme Celeris One, comprenant trois systèmes de zones de travail : Xanthos, Hephaistos et Hades. Les systèmes intègrent des réseaux de neurones graphiques pour prédire les interactions et des modèles génératifs pour créer de nouvelles matières chimiques, telles que l'optimisation des liens et des objectifs multiples pour améliorer les propriétés moléculaires, la dynamique moléculaire et les calculs d'énergie libre. Le flux de travail utilise également des capacités d'apprentissage profond géométrique et de rétrosynthèse basées sur l'apprentissage automatique. Celeris Therapeutics gère un laboratoire automatisé pour générer des données biologiques et effectuer une synthèse chimique personnalisée.

Le flux de travail de laboratoire sec de la plateforme Xanthos pilotée par l'IA de Celeris Therapeutics.
Nous avons récemment publié un large aperçu du marché de la dégradation des protéines dans un article Les dégradeurs de protéines prennent d'assaut l'industrie, comprenant plusieurs études de cas avec un aperçu technique des plates-formes de calcul impliquées.
La première vague de candidats-médicaments développés par l'IA devient clinique
Bien qu'il soit probablement tôt pour dire que l'adoption de l'IA dans l'industrie pharmaceutique a complètement révolutionné la découverte de médicaments, plusieurs entreprises « natives de l'IA » ont réussi à gagner en efficacité dans la construction rapide de leurs pipelines thérapeutiques. Quelle est la caractéristique commune de ces entreprises ? Chacun a construit une plate-forme d'IA spécialisée et hautement intégrée, comprenant de nombreux modèles et sources de données. Certaines plateformes sont également disponibles en tant que logiciel en tant que service pour des partenaires de R&D externes, tels que Chemistry42.
Moderna Therapeutics, qui a non seulement réussi à intégrer des analyses d'IA de pointe dans ses recherches, mais a numérisé et intégré tous les aspects de son flux de travail de R&D, y compris fabrication et diffusion. Lorsque la pandémie de COVID-19 a frappé le monde au début de 2020, Moderna a été parmi les premières entreprises à être en mesure de proposer un vaccin efficace à base d'ARNm en seulement 2 jours (!) Et de le mettre sur le marché en un an .
Une vague de succès dans la découverte de produits thérapeutiques rendue possible par l'IA démontre la capacité des entreprises natives de l'IA à proposer des candidats-médicaments plus rapidement qu'elles ne le prenaient généralement pour des programmes similaires.

Voir « La feuille de route des candidats-médicaments conçus par l'IA »,
L'anticorps monoclonal LY-CoV555 d'AbCellera a été développé en trois mois et a obtenu l'autorisation d'utilisation d'urgence de la FDA.
Le Knowledge Graph de BenevolentAI a aidé l'entreprise à identifier le baricitinib comme un antiviral COVID-19 efficace en quelques jours (maintenant approuvé pour une utilisation par la FDA). Une autre petite molécule BEN-8744, un nouvel inhibiteur pour traiter la rectocolite hémorragique et la dermatite, a fait l'objet d'études précliniques tardives en moins de 24 mois.
La petite molécule inhibitrice EXS-21546 d'Exscientia a été la première molécule conçue par l'IA pour l'immuno-oncologie à entrer dans des essais cliniques humains (maintenant en phase I) et a été découverte en seulement huit mois. La société a plusieurs autres molécules en essais cliniques.
L'inhibiteur à petite molécule ISM001-055 d'Insilico Medicine, pour traiter la fibrose pulmonaire idiopathique, a été conçu de novo et avancé dans des études précliniques tardives en 18 mois (maintenant en phase I).
Schrodinger, basé à New York, a développé une petite molécule SGR-1505 pour traiter le lymphome à cellules B en dix mois et est actuellement en cours de demande d'IND.
Recursion Pharmaceuticals, basée à Salt Lake City, a développé un médicament candidat pour une maladie rare non précisée en 18 mois. La société dispose d'un portefeuille large et diversifié de candidats-médicaments précliniques et cliniques conçus à l'aide de sa plateforme de biologie numérique.
Deep Genomics, basée à Toronto, a utilisé sa plateforme AI Workbench pour développer une nouvelle cible génétique et un candidat-médicament oligonucléotidique correspondant DG12P1 pour traiter une maladie de Wilson héréditaire rare.
Pour suivre les principaux candidats-médicaments cliniques développés par l'IA, nous avons créé « La feuille de route des candidats-médicaments conçus par l'IA », qui sera mis à jour régulièrement.
Il convient de noter que l'attention continue des médias sur l'IA pour la découverte de médicaments doit être considérée avec prudence. Par exemple, le plan de BenevolentAI visant à accorder une licence à son candidat-médicament contre la dermatite atopique, BEN-2293, a subi un revers car l'inhibiteur pan-Trk activé par l'IA n'a pas réussi à améliorer les symptômes de l'eczéma ou les démangeaisons dans un essai de phase 2a. La société avait précédemment identifié les récepteurs kinases de la tropomyosine (Trk) comme médiateurs des démangeaisons et de l'inflammation dans la dermatite atopique, conduisant au développement d'inhibiteurs de Trk. Bien que BEN-2293 ait démontré une tendance vers un effet cliniquement significatif dans un essai de phase 1b, l'essai de phase 2a a révélé qu'il n'était pas meilleur qu'un placebo pour améliorer la sévérité de l'eczéma ou les démangeaisons. Le résultat soulève des questions sur la plate-forme activée par l'IA qui a proposé l'approche. Malgré le revers, BenevolentAI n'a pas abandonné le médicament candidat, citant des preuves que le traitement était plus efficace chez les patients présentant une plus grande étendue de la maladie au départ. La société examine actuellement les données avant de déterminer ses prochaines étapes.
Les vingt entreprises d'IA les plus "productives" dans le domaine de la découverte de médicaments
Après avoir présélectionné environ 130 entreprises parmi plus de 380 entreprises d'IA dans le rapport BiopharmaTrend AI, nous avons en outre sélectionné 20 entreprises - en utilisant une formule d'évaluation simple mais robuste prenant en compte les pipelines cliniques et précliniques d'entreprises, la capacité de découverte de cibles et le temps dans les affaires. Les 20 entreprises sélectionnées formaient le BPT20 : Intelligence artificielle dans l'indice de productivité de la découverte de médicaments - le premier point de référence de l'industrie pour mettre en évidence les entreprises qui défendent l'application de l'IA pour la conception de novo de médicaments, le dépistage virtuel ou la réutilisation de médicaments.

IA et laboratoires robotisés du futur
Les modèles d'apprentissage en profondeur (par exemple, basés sur des réseaux de neurones profonds) sont extrêmement « gourmands en données », ce qui signifie que, quelle que soit la qualité de l'IA, c'est la qualité et la taille des données qui sont tout aussi importantes pour des prédictions de recherche significatives. Le moyen le plus efficace de générer des données biologiques de haute qualité consiste à utiliser la robotique. Si nous considérons la transformation moderne de la découverte de médicaments basée sur l'IA comme un processus étape par étape, largement disponible et relativement rentable rl'obotics-as-a-service serait l'élément final et critique de l'intelligence artificielle industrialisation de la recherche pharmaceutique et biotechnologique. Selon un rapport d'Arctoris, "la robotique est essentielle pour permettre au paradigme de la découverte en boucle fermée de devenir une réalité - ce qui sera un espace passionnant à surveiller au cours des prochaines années".
Certaines entreprises construisent des installations de laboratoire standardisées, hautement automatisées, évolutives et de plus en plus compatibles, guidées par des systèmes de contrôle d'expériences basés sur l'IA et complétées par des capacités d'exploration et d'analyse de données basées sur l'IA. Ces installations de laboratoire « nouvelle génération » deviennent accessibles à distance aux expérimentateurs de la recherche préclinique sur les médicaments, faisant de l'expérimentation préclinique une routine plus évolutive et standardisée. Les principaux fournisseurs de laboratoires à distance figurant sur la liste sont Automata Labs, Strateos, Emerald Labs et Culture Biosciences, pour n'en nommer que quelques-uns.
L'espace attire des fonds de capital-risque et des clients. Par exemple, en février 2022, Automata Labs, basé au Royaume-Uni, a levé 50 millions de dollars pour automatiser le processus de recherche en laboratoire. En juillet 2021, Strateos a levé 56 millions de dollars pour améliorer encore sa plateforme SmartLab et sa technologie robotisée et automatisée à distance, disponible pour les chercheurs précliniques du monde entier. Culture Biosciences a levé un total de plus de 100 millions de dollars, avec la dernière série B de 80 millions de dollars annoncée en novembre 2021. Emerald Cloud Labs (ECL), basé à San Francisco, a levé plus de 90 millions de dollars au fil des ans. Les premiers utilisateurs de la plate-forme robotique de suppression d'ECL ont signalé des améliorations de 300 % à 700 % dans la productivité de la recherche. En juin 2022, MegaRobo, basée à Pékin, a levé 300 millions de dollars pour étendre sa gamme diversifiée de services de laboratoire à distance automatisés et d'installations robotisées.
La montée en puissance des laboratoires robotisés à distance est une tendance à long terme de l'industrie, une nouvelle façon d'offrir des services de recherche sous contrat qui seraient extrêmement bénéfiques pour l'adoption à long terme de stratégies de recherche centrées sur les données « AI-first ».
Plusieurs sociétés de découverte de médicaments axées sur l'IA, telles qu'Arctoris, Recursion Pharmaceuticals, Insitro et Generative Bio, abordent cette tendance via un modèle commercial différent - elles ont construit des installations de laboratoire robotisées internes pour améliorer leurs capacités de génération de données internes pour former leur Modèles d'IA et création de pipelines de candidats-médicaments thérapeutiques.
Par exemple, Arctoris, basée à Oxford, fondée en 2016, a construit un laboratoire humide entièrement automatisé qui génère des données de qualité supérieure à grande échelle, alimentant le lac de données d'Arctoris et alimentant la plate-forme de prise de décision basée sur l'IA de l'entreprise, Ulysses, qui alimente la recherche de l'entreprise à partir de cible à atteindre, à mener et à l'étape de l'application IND.
Le pipeline d'Arctoris comprend désormais plusieurs programmes précliniques en oncologie et en neurologie. Arctoris a levé un total de 10.3 millions de dollars en plusieurs tours de table auprès d'investisseurs, dont Future Planet Capital, RT Ventures et Formic Ventures.
Certaines grandes sociétés de découverte de médicaments IA, telles qu'Exscientia et Insilico Medicine, construisent désormais également des laboratoires robotisés internes pour développer leurs «muscles» de génération de données internes.
Recursion Pharmaceuticals, basée à Salt Lake City, est l'un des leaders de l'espace d'expérimentation biologique robotisée. L'infrastructure basée sur l'IA de la société, appelée Recursion Operation System, est un système intégré en boucle fermée combinant la génération de données internes exclusives et des outils de calcul avancés pour générer de nouvelles informations pour lancer ou accélérer des programmes thérapeutiques. La société automatise l'expérimentation biologique préclinique à grande échelle. Par exemple, les images de microscopie cellulaire capturent les changements composites de la morphologie cellulaire et sont traitées par les systèmes de vision par ordinateur alimentés par l'IA de la société. Depuis 2017, Recursion Pharmaceuticals a approximativement doublé la capacité de la plate-forme phénomique chaque année et a augmenté le nombre d'expériences phénomiques exécutées jusqu'à 2.2 millions chaque semaine, ce qui a entraîné environ 19 pétaoctets de données exclusives de haute dimension.
Surmonter les goulots d'étranglement des essais cliniques avec l'IA
L'essai clinique est une étape critique du flux de travail de développement de médicaments, avec un taux de réussite moyen estimé à environ 11% pour les candidats-médicaments passant de la phase 1 vers l'approbation. Même si le candidat-médicament est sûr et efficace, les essais cliniques peuvent échouer en raison de financement insuffisant, inscription insuffisante ou mauvaise conception des études.
L'intelligence artificielle (IA) est de plus en plus perçue comme une source d'opportunités améliorer l'efficacité opérationnelle des essais cliniques et minimiser les coûts de développement clinique. En règle générale, les fournisseurs d'IA proposent leurs services et leur expertise dans trois domaines principaux. Les start-ups d'IA du premier domaine aident à déverrouiller des informations provenant de sources de données disparates, telles que des articles scientifiques, des dossiers médicaux, des registres de maladies et même des réclamations médicales, en appliquant le traitement du langage naturel (TAL). Cela peut soutenir le recrutement et la stratification des patients, la sélection des sites et améliorer la conception des études cliniques et la compréhension des mécanismes de la maladie. A titre d'exemple, environ 18 % des études cliniques échouent en raison d'un recrutement insuffisant, comme une étude 2015 signalé.
Un autre aspect du succès des essais cliniques est l'amélioration de la stratification des patients. Étant donné que les patients des essais coûtent cher - le coût moyen de l'inscription d'un patient était $ 15,700-26,000 en 2017 — il est essentiel de pouvoir prédire quel patient bénéficiera ou risquera le plus d'un traitement. Les entreprises axées sur l'IA fonctionnent avec plusieurs types de données, tels que les dossiers de santé électroniques (DSE), les omiques et les données d'imagerie, afin de réduire l'hétérogénéité de la population et d'augmenter la puissance des études cliniques. Les fournisseurs pourraient utiliser des biomarqueurs de la parole pour identifier la progression de la maladie neurologique, des analyses d'imagerie pour suivre la progression du traitement ou des biomarqueurs génétiques pour identifier les patients présentant des symptômes plus graves.
AI rationalise également les processus opérationnels des essais cliniques. Les fournisseurs d'IA aident à suivre la santé des patients depuis leur domicile, à surveiller la réponse au traitement et l'adhésion des patients aux procédures d'essai. Ce faisant, les entreprises d'IA réduisent le risque d'abandon des patients, ce qui représentait 30% en moyenne. Habituellement, l'étape de l'étude clinique de phase 3 nécessite 1000-3000 participants, une partie d'entre eux prenant un placebo. C'est pourquoi le développement de bras de contrôle synthétiques – Les modèles d'IA qui pourraient remplacer les groupes d'individus témoins placebo, réduisant ainsi le nombre d'individus requis pour les essais cliniques – pourraient devenir une nouvelle tendance.
Selon le rapport BiopharmaTrend AI, il existe plus de 80 entreprises dans les trois catégories, notamment Owkin, PathAI, GNS Healthcare, Neurcuit, AICure et Unlearn.ai.
EN RELATION: 8 sociétés d'IA notables en recherche clinique à surveiller en 2022
La demande de plateformes d'essais cliniques basées sur l'IA est élevée, ainsi que les investissements dans ce domaine, malgré le climat d'investissement globalement froid dans la biotechnologie.
En mars 2022, ConcertAI a obtenu une valorisation de 1.9 milliard de dollars après avoir encaissé un tour de table de série C de 150 millions de dollars pour faire évoluer ses solutions logicielles et de données du monde réel (RWD) pour la recherche sur le cancer.
Saama est une société basée dans la Silicon Valley fondée en 1997, mais elle a levé son premier capital-risque en 2015. La société a levé plus de 500 millions de dollars en capital-risque, y compris le dernier méga-tour de 430 millions de dollars en août 2022 – de Carlyle et fonds de capital-risque de Merck, Pfizer, Amgen, McKesson et autres.
Saama est l'un des principaux acteurs de l'espace d'analyse des essais cliniques axé sur l'IA, offrant une suite diversifiée de solutions : essais cliniques accélérés via un centre d'analyse et de contrôle des données centralisé, y compris des capacités de traitement des données en temps réel ; capacités automatisées de qualité des données ; capacités de soumission réglementaires simplifiées, y compris les analyses et les soumissions de pharmacovigilance.
En avril 2022, Unlearn.AI, une startup développant un service de "jumeau numérique" pour les essais cliniques, a levé 50 millions de dollars.
En juin 2022, Bristol Myers Squib investi $ 80 millions dans OWKIN - pour aider à améliorer la conception des essais de médicaments cardiovasculaires, avec des améliorations des définitions des critères d'évaluation, l'identification des sous-groupes de patients et l'estimation des effets du traitement. OWKIN, la « licorne » basée à Paris et à New York, s'appuie sur son accès aux données multimodales de haute qualité et son apprentissage automatique de pointe pour prédire avec précision divers effets du traitement sur les sous-populations de patients afin d'améliorer la conception et les résultats des essais cliniques. OWKIN applique également sa plateforme d'IA pour la découverte de médicaments.
En août 2022, Bristol Myers Squibb a également annoncé un accord de collaboration élargi pluriannuel avec PathAI, spécialiste de la pathologie de l'IA. Le travail initial dans le cadre de cet accord prolongé se concentrera sur la recherche translationnelle clé en oncologie, fibrose et immunologie, avec un objectif global de les transmettre dans des essais cliniques. Deux mois plus tôt, PathAI a conclu un partenariat stratégique pluriannuel avec GlaxoSmithKline pour accélérer les programmes de recherche scientifique et de développement de médicaments en oncologie et dans la stéatohépatite non alcoolique (NASH) en tirant parti des technologies de PathAI en pathologie numérique, y compris l'utilisation de l'outil AIM-NASH de PathAI.
Notamment, Akkure Genomics de Dublin Vient d'être annoncé il a financé 1 million d'euros en une semaine pour soutenir les essais cliniques via sa plateforme d'IA, qui aide les gens à participer aux essais cliniques les plus pertinents en fonction de données sur eux-mêmes et leur état.
L'IA dans l'industrie de la recherche contractuelle
L'émergence de nouvelles sociétés de recherche sous contrat natives de l'IA dans les espaces précliniques et cliniques remet en question le statu quo des principales organisations de recherche sous contrat (CRO) bien établies. Ils répondent en intégrant l'IA dans leurs offres de services à l'industrie pharmaceutique ou en s'associant à des sociétés d'IA pour compléter leur capacité de recherche.
EN RELATION: L'évolution de l'industrie de l'externalisation de la R&D pharmaceutique : une vue d'ensemble.
Par exemple, Charles River Labs, une organisation de recherche sous contrat en phase de démarrage basée aux États-Unis, plonge plus profondément dans l'IA en établissant un partenariat pluriannuel avec Valo Health. Charles River ajoute la technologie Opal de Valo qui apprend activement au fur et à mesure que les programmes sont développés. Charles River espère que son utilisation de la plate-forme d'apprentissage en profondeur Opal se traduira par un processus plus rapide et plus efficace, de la conception de molécules de novo à l'optimisation des pistes. L'année dernière, Charles River a établi un partenariat stratégique avec Valence Discovery qui a permis aux clients du CRO d'accéder à la plateforme d'intelligence artificielle de Valence pour la prédiction des propriétés moléculaires, la chimie générative et l'optimisation multiparamètre.
IQVIA investit depuis des années dans les capacités d'IA pour ajouter de la valeur aux essais cliniques et aux activités commerciales qu'elle propose à ses clients. Pour améliorer les essais cliniques, par exemple, IQVIA lancé Avacare Clinical Research Network™ en 2020, qui a permis aux sites de faire correspondre les patients aux essais plus rapidement et plus efficacement. La plate-forme est alimentée par des algorithmes d'IA et peut fonctionner dans 19 domaines pathologiques. Auparavant, une autre plate-forme Linguamatics Natural Language Processing (NLP) d'IQVIA avait remporté les Fierce Innovation Awards 2019 de Questex. La plate-forme peut avoir de vastes applications dans les soins de santé et les sciences de la vie, notamment l'identification de cibles, la cartographie génétique, la prédiction des résultats pour les patients, etc.
Une tendance importante dans l'industrie de la recherche clinique est en marche essais cliniques virtuels, un marché de 8 milliards de dollars. La pandémie de COVID-19 a forcé les sociétés pharmaceutiques à passer à la surveillance à distance, à l'amélioration du recrutement des patients, aux applications pour suivre l'engagement des patients, à la télémédecine, à la décentralisation et à d'autres mesures pour maintenir les essais en cours. Étant donné que la demande pour de telles solutions a considérablement augmenté, les CRO se sont précipités pour ajouter des capacités virtuelles et décentralisées à leurs offres de services. La technologie de l'IA s'est avérée inestimable dans la création et l'exécution de tels projets pour aider à synthétiser les données et accélérer les processus d'essais cliniques.
Les géants de la technologie s'attaquent à la découverte de médicaments et à la biotechnologie
Les succès mentionnés précédemment de DeepMind et Meta de l'Alphabet dans la résolution des énigmes de la recherche fondamentale en biologie, comme la prédiction des structures protéiques à grande échelle à l'aide de modèles d'apprentissage en profondeur et de langage, ne sont que la pointe de l'iceberg : presque tous les géants technologiques de premier plan sont désormais dans le secteur des sciences de la vie. , d'une manière ou d'une autre.
Alphabet (une société mère de Google) a des dizaines d'investissements dans des projets de sciences de la vie, y compris le moteur de recherche de réactifs basé sur l'IA BenchSci, l'IA basée en Chine et la physique quantique dans la société de découverte de médicaments XtalPi, la société de génomique personnelle 23andMe et le développement de médicaments axé sur l'IA. licorne OWKIN pour n'en nommer que quelques-uns. En 2021, Alphabet, en collaboration avec DeepMind, a lancé Isomorphic Labs pour se concentrer sur l'application de l'intelligence artificielle pour déchiffrer la biologie fondamentale et la découverte de médicaments.
Outre de multiples autres projets et activités dans la recherche pharmaceutique et la biotechnologie, Alphabet dispose d'une entité à grande échelle, Verily, dédiée aux sciences de la vie et à la MedTech.
Microsoft, un développeur mondial de logiciels, a une empreinte profonde dans les sciences de la vie, avec des dizaines de collaborations de recherche avec des grandes sociétés pharmaceutiques, fournissant ses infrastructures pour gérer les mégadonnées à l'aide de modèles d'apprentissage automatique à grande échelle. Parmi les dernières initiatives de Microsoft figure Modèle MoLeR, un nouvel outil développé par l'équipe de chimie générative de l'entreprise en collaboration avec Novartis. Le modèle MoLeR, contrairement à d'autres outils génératifs, utilise l'apprentissage en profondeur pour créer de nouvelles structures basées sur un échafaudage donné qui sert de base initiale au processus génératif. Un autre exemple est AI4Science, une nouvelle entreprise de Microsoft combinant la chimie computationnelle, la physique quantique, l'apprentissage automatique, la biologie moléculaire, la dynamique des fluides et le génie logiciel pour concrétiser une vision du soi-disant « cinquième paradigme » de la science.
EN RELATION: Comment la "Big Tech" gagne lentement les marchés pharmaceutiques
Une entreprise particulièrement active dans ce contexte est un producteur de matériel pour l'industrie du jeu et des ordinateurs personnels, NVIDIA. Cette société technologique a lancé Clara Discovery, qui est une collection de cadres, d'applications et de modèles d'IA permettant la découverte de médicaments accélérés par GPU, avec un soutien pour la recherche en génomique, protéomique, microscopie, dépistage virtuel, chimie computationnelle, visualisation, imagerie clinique et traitement du langage naturel (TAL). Et en mars 2022, la société a présenté Clara Holoscan MGX™, une plate-forme permettant à l'industrie des dispositifs médicaux de développer et de déployer des applications d'IA en temps réel à la périphérie, spécialement conçues pour répondre aux normes réglementaires requises. Clara Holoscan vise une architecture de référence tout-en-un de qualité médicale, ainsi qu'un support logiciel à long terme, pour accélérer l'innovation dans l'industrie des dispositifs médicaux.
L'avenir de l'IA dans la découverte de médicaments : tout ce qui est « quantique »
La plupart des outils logiciels utilisés pour la découverte de médicaments et la recherche en biologie reposent sur la mécanique moléculaire - une représentation simplifiée des molécules, les réduisant essentiellement à des "boules et des bâtons": des atomes et des liaisons entre eux. De cette façon, il est plus facile à calculer, mais la précision en souffre grandement. Pour obtenir une précision adéquate, il faut tenir compte du comportement électronique des atomes et des molécules, c'est-à-dire considérer les particules subatomiques — les électrons et les protons. C'est à cela que servent les méthodes de mécanique quantique (QM) - et la théorie n'est pas nouvelle, remontant aux premières décennies du 20e siècle.
Cependant, les méthodes quantiques sont exceptionnellement coûteuses en calcul – et jusqu'à ces dernières décennies, c'était un obstacle prohibitif pour la théorie quantique d'influencer le côté pratique des choses. En raison de la croissance exponentielle de la puissance de calcul disponible, les méthodes quantiques deviennent enfin des outils précieux entre les mains des scientifiques.
Plusieurs entreprises fusionnent l'apprentissage automatique et la théorie quantique pour améliorer considérablement les capacités de modélisation de leurs systèmes de découverte de médicaments. Par exemple, les scientifiques de XtalPi, une société technologique basée en Chine et aux États-Unis, soutenue par Sequoia China, Tencent et Google, ont construit leur plate-forme de découverte et de développement de médicaments numériques intelligents (ID4), intégrant la mécanique quantique, l'intelligence artificielle et la haute performance. algorithmes de cloud computing. ID4 permet de prédire avec une grande précision les propriétés physico-chimiques et pharmaceutiques des candidats-médicaments à petites molécules, ainsi que leurs structures cristallines - éléments critiques dans la R&D des médicaments.
Aqemia, basée à Paris, est une autre entreprise qui fait avancer ce domaine. La société se concentre sur la conception de novo, basée sur la structure, de molécules de type plomb en combinant l'intelligence quantique et artificielle (IA). Un algorithme unique de mécanique statistique d'inspiration quantique qui prédit l'affinité entre un composé et une cible thérapeutique avec précision et 10,000 XNUMX fois plus rapidement que la concurrence. L'IA d'Aqemia peut générer des composés avec une précision croissante en obtenant une rétroaction du prédicteur d'affinité.
Enfin, il y a Pharmacelera, basée à Barcelone, une société informatique qui applique la théorie quantique pour stimuler la conception de médicaments via ses deux progiciels principaux : PharmScreen et PharmQSAR. Le premier outil permet un criblage virtuel précis basé sur les ligands à l'aide d'un algorithme d'alignement de ligands 3D de haute précision basé sur les champs d'interaction. Elle peut générer un taux de diversité parmi les prospects plus élevé que les méthodes et outils classiques. Le second, PharmQSAR, est un outil de relation quantitative structure-activité (QSAR) 3D qui permet de combiner plusieurs champs d'interaction pour effectuer des études CoMFA/CoMSIA.
EN RELATION: 12 entreprises utilisant la théorie quantique pour accélérer la découverte de médicaments
Une autre tendance technologique, plus futuriste, exploitant la théorie quantique, concerne la création d'un ordinateur quantique. Avec plusieurs décennies d'avancées dans la théorie quantique et des progrès simultanés dans plusieurs domaines logiciels et matériels, nous entrons enfin dans l'ère des ordinateurs quantiques devenant pratiquement viables.
Alors que nous en sommes aux débuts de l'informatique quantique, plusieurs entreprises intègrent déjà des éléments de l'informatique quantique dans la découverte de médicaments informatiques.
Par exemple, POLARISqb est un développeur basé au Royaume-Uni du premier logiciel de découverte de médicaments au monde conçu pour les ordinateurs quantiques, combinant l'intelligence artificielle et une approche quantique. Au cœur de la technologie POLARISqb se trouve la plate-forme de conception de médicaments Tachyon, utilisée pour exécuter des travaux de conception moléculaire distribués dans le cloud, gérée par un processus automatisé qui permet de rechercher de grandes bibliothèques chimiques tout en exécutant plusieurs projets en parallèle. En développant un logiciel propriétaire pour les systèmes quantiques, la société affirme qu'elle peut considérablement accélérer la conception de médicaments et obtenir des pistes de meilleure qualité. En raison de « l'agnosticisme » inhérent au système Tachyon, il peut fonctionner dans de multiples maladies et indications.
Menten AI est une start-up canadienne fondée en 2018 qui développe une plateforme logicielle pour la conception de protéines alimentée par l'apprentissage automatique et l'informatique quantique. La société utilise des algorithmes d'optimisation quantique exclusifs, qui, selon elle, peuvent améliorer considérablement la précision de la découverte de médicaments tout en réduisant les coûts et le temps de développement.
Pour résumer cet article, référons-nous à une prédiction du Dr Christopher Savoie, co-fondateur et PDG de Zapata Computing, une société américaine de logiciels quantiques, sur la recherche de pointe dans ce domaine, qu'il a exprimée dans une interview pour BiopharmaTrend :
« À l'avenir, le quantum fera partie de tous ou presque tous les workflows de science des données et d'apprentissage automatique dans le secteur biopharmaceutique. Je pense qu'il en fera partie intégrante. Si vous pouvez obtenir un modèle plus précis en utilisant la technologie quantique, pourquoi ne le feriez-vous pas, après tout ? »
Les grands modèles de langage font des progrès dans la découverte de médicaments
Les grands modèles de langage (LLM) comme ChatGPT d'OpenAI sont utilisés par des sociétés de biotechnologie, telles que Médecine Insilico, Une innocenceet Exscientia, pour aider à la découverte de médicaments.
ChatGPT aide les scientifiques à interagir avec les outils d'IA et d'apprentissage automatique, rendant les données plus accessibles. Par exemple, Insilico Medicine utilise ChatGPT pour interagir avec sa plateforme de découverte de cibles, PandaOmics, tandis que le fondateur d'Ainnocence Lurong P. envisage des versions spécialisées comme Bio ChatGPT ou Med ChatGPT. Exscientia utilise des LLM pour générer des assertions structurées et mécanistes pour leurs graphes de connaissances.
Les LLM servent également de moteurs de recherche avancés en sciences biologiques. Google et DeepMindLe chatbot Med-PaLM de fournit des réponses aux questions médicales, tandis que BienveillanteAI semble enthousiasmé par la fonction de plug-in de récupération de ChatGPT, qui pourrait aider à personnaliser la fonction de chat en fonction de ses propres données.
Malgré le potentiel des LLM dans la découverte de médicaments, certaines entreprises comme BioXcel Therapeutics, Inc. ainsi que Entérôme restent prudents quant à l'adoption de la technologie, invoquant des préoccupations concernant l'exactitude et la confidentialité.
Ce qui est clair, c'est que la montée en puissance de ChatGPT et d'autres modèles d'IA générative, tels que l'AlphaFold de DeepMind, a accru la prise de conscience de leurs applications potentielles dans la biotechnologie, encourageant les entreprises à explorer leurs avantages dans la découverte et le développement de médicaments.
Sujets: Tendances de l'industrie
- Contenu propulsé par le référencement et distribution de relations publiques. Soyez amplifié aujourd'hui.
- PlatoData.Network Ai générative verticale. Autonomisez-vous. Accéder ici.
- PlatoAiStream. Intelligence Web3. Connaissance Amplifiée. Accéder ici.
- PlatonESG. Automobile / VE, Carbone, Technologie propre, Énergie, Environnement, Solaire, La gestion des déchets. Accéder ici.
- Décalages de bloc. Modernisation de la propriété des compensations environnementales. Accéder ici.
- La source: https://www.biopharmatrend.com/post/615-pharmaceutical-artificial-intelligence-key-developments-in-2022/



