Si al principi no tens èxit, aleshores el paracaigudisme no és per a tu.
->
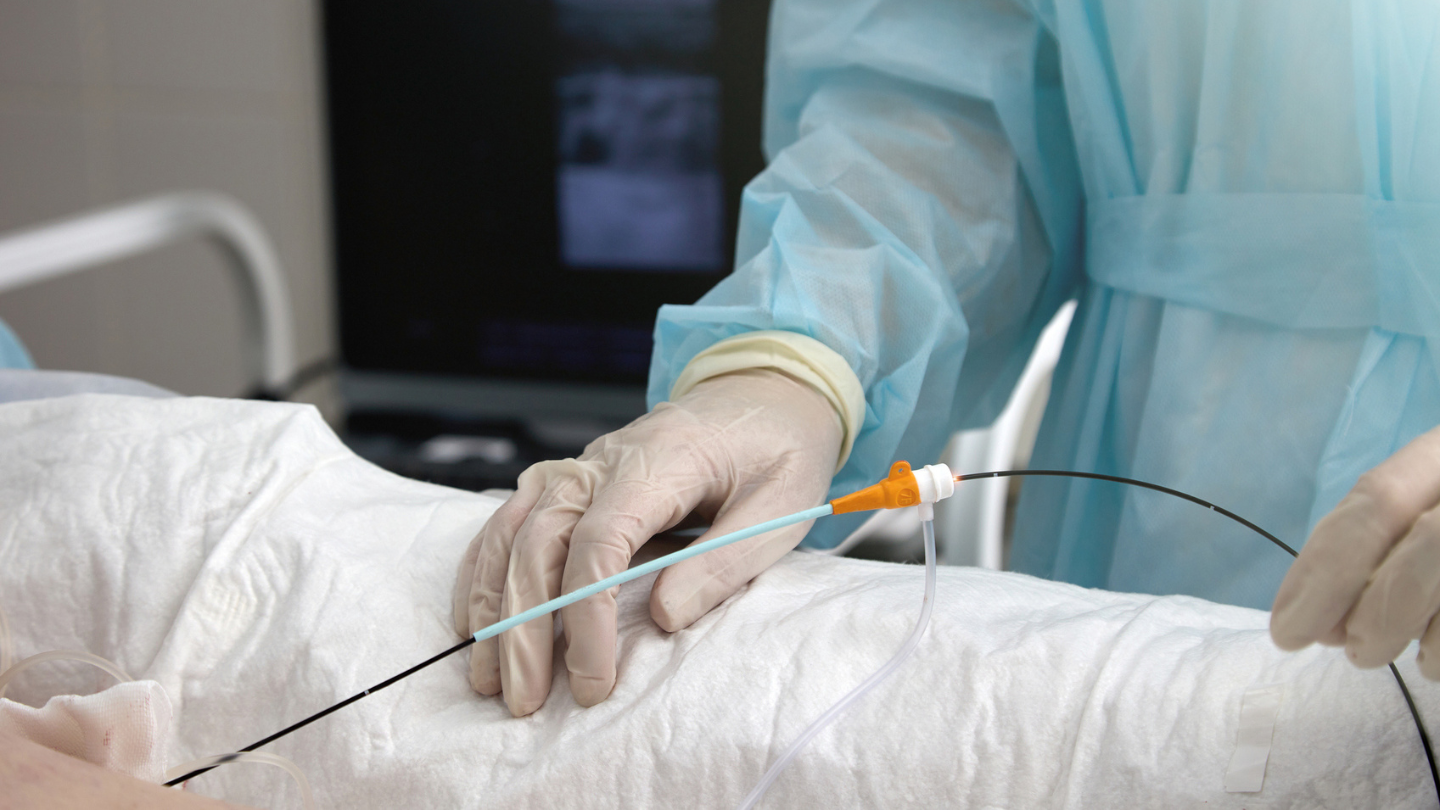
Η Citius Pharmaceuticals έχει φτάσει σε ένα σημαντικό ορόσημο στην κλινική δοκιμή για τη θεραπεία με Mino-Lok (MLT), μια λύση κλειδώματος αντιβιοτικών για τη διάσωση καθετήρων σε ασθενείς με λοιμώξεις της κυκλοφορίας του αίματος που σχετίζονται με καθετήρες.
Η Citius πιστεύει ότι και τα 92 συμβάντα που απαιτούνται για την ολοκλήρωση της δοκιμής έχουν επιτευχθεί, ωστόσο, αυτό εκκρεμεί επιβεβαίωση από ανεξάρτητους αναθεωρητές. Ορισμένοι ασθενείς παραμένουν σε ενεργό θεραπεία.
MLT είναι μια νέα αντιβιοτική θεραπεία κλειδώματος που συνδυάζει τη μινοκυκλίνη με το δινάτριο edetate για τη θεραπεία ασθενών με λοιμώξεις του αίματος που σχετίζονται με τον καθετήρα. Η τρέχουσα θεραπεία περιλαμβάνει την κλινική αφαίρεση και αντικατάσταση ενός κεντρικού φλεβικού καθετήρα (CVC), στον οποίο η θεραπεία παρέχει μια εναλλακτική λύση.
Εάν εγκριθεί, MLT, Το οποίο Με άδεια Citius από το Πανεπιστήμιο του Τέξας MD Anderson Cancer Centre, θα ήταν η πρώτη και μοναδική εγκεκριμένη από τον FDA θεραπεία που διασώζει κεντρικούς φλεβικούς καθετήρες που προκαλούν λοιμώξεις του αίματος που σχετίζονται με την κεντρική γραμμή. Το MLT έλαβε πιστοποιημένο προϊόν μολυσματικής νόσου και ονομασίες ταχείας διαδρομής από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA). Το έχει προστασία ευρεσιτεχνίας έως το 2024 και προστασία με δίπλωμα ευρεσιτεχνίας σύνθεσης έως το 2036.
Ο πρόεδρος και διευθύνων σύμβουλος Leonard Mazur δήλωσε: «Αυτό είναι ένα σημαντικό ορόσημο για τη Citius καθώς πλησιάζουμε στην ολοκλήρωση της δοκιμής Φάσης III Mino-Lok. Καθώς ολοκληρώνουμε τη θεραπεία για ασθενείς σε ενεργό θεραπεία, θα συνεχίσουμε να εγγράφουμε ασθενείς στη διαδικασία και να ξεκινήσουμε δραστηριότητες διακοπής λειτουργίας».
Δοκιμαστική σχεδίαση φάσης III Mino-Lok
Η δοκιμή Φάσης ΙΙΙ MLT (NCT02901717), η οποία διεξάγεται στις ΗΠΑ και την Ινδία, είναι μια πολυκεντρική, τυχαιοποιημένη, ανοιχτή, τυφλή μελέτη για τον προσδιορισμό της αποτελεσματικότητας και της ασφάλειας της MLT. Το πρωταρχικό τελικό σημείο είναι ο χρόνος για την αποτυχία του καθετήρα. Πρόσθετα δευτερεύοντα μέτρα έκβασης περιλαμβάνουν τη συνολική επιτυχία, τη μικροβιολογική εκρίζωση και την κλινική θεραπεία.
Οι ασθενείς που πληρούν όλα τα απαραίτητα κριτήρια για τη μελέτη τυχαιοποιούνται σε αναλογία 1:1 για να λάβουν είτε MLT είτε αντιβιοτική θεραπεία κλειδώματος τυπικής φροντίδας. Οι ασθενείς στο σκέλος MLT λαμβάνουν μια ημερήσια δόση για επτά ημέρες. Για τα άτομα στο σκέλος ελέγχου, ο ερευνητής καθορίζει το αντιβιοτικό που χρησιμοποιείται στην κλειδαριά, τη δόση, τον χρόνο παραμονής και τον αριθμό των ημερών χορήγησης με βάση τα πρότυπα του ιδρύματος ή τις οδηγίες της Εταιρείας Λοιμωδών Νοσημάτων της Αμερικής (IDSA).
<!– GPT AdSlot 3 για ενότητα διαφημίσεων 'Verdict/Verdict_In_Article' ### Μέγεθος: [[670,220]] —
!– Τέλος AdSlot 3 –>
- SEO Powered Content & PR Distribution. Ενισχύστε σήμερα.
- PlatoData.Network Vertical Generative Ai. Ενδυναμώστε τον εαυτό σας. Πρόσβαση εδώ.
- PlatoAiStream. Web3 Intelligence. Ενισχύθηκε η γνώση. Πρόσβαση εδώ.
- PlatoESG. Αυτοκίνητο / EVs, Ανθρακας, Cleantech, Ενέργεια, Περιβάλλον, Ηλιακός, Διαχείριση των αποβλήτων. Πρόσβαση εδώ.
- PlatoHealth. Ευφυΐα βιοτεχνολογίας και κλινικών δοκιμών. Πρόσβαση εδώ.
- ChartPrime. Ανεβάστε το Trading Game σας με το ChartPrime. Πρόσβαση εδώ.
- BlockOffsets. Εκσυγχρονισμός της περιβαλλοντικής αντιστάθμισης ιδιοκτησίας. Πρόσβαση εδώ.
- πηγή: https://www.clinicaltrialsarena.com/news/citius-reaches-milestone-mino-lok/



